1 . 中国首次实现了利用二氧化碳人工合成淀粉,为全球的“碳达峰”、“碳中和”起到重大的支撑作用。其中最关键的一步是以CO2为原料制CH3OH。在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应有:
I.CO2(g)+H2(g) CO(g)+H2O(g) ΔH1=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH1=+41.1kJ·mol-1
II.CO(g)+2H2(g) CH3OH(g) ΔH2=-90.0kJ·mol-1
CH3OH(g) ΔH2=-90.0kJ·mol-1
(1)CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH=
CH3OH(g)+H2O(g)ΔH=___ 。
(2)5Mpa时,往某密闭容器中按投料比n(H2)∶n(CO2)=3∶1充入H2和CO2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图1所示。
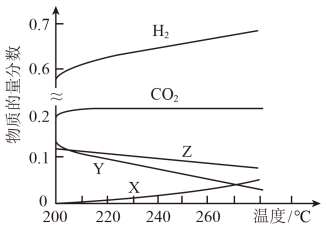
①图中X代表___ 。(填化学式)。
②体系中H2的物质的量分数随温度的增大而升高,试分析原因___ 。
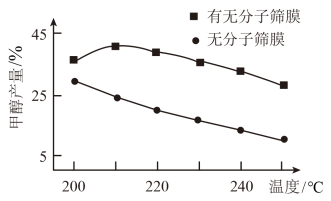
(3)H2和CO2起始物质的量比为3∶1时,该反应在有、无分子筛膜时甲醇的平衡产率随温度的变化如图2所示,其中分子筛膜能选择性分离出H2O。温度低于210℃时,随着温度升高,有分子筛膜的甲醇产率升高的可能原因是___ 。
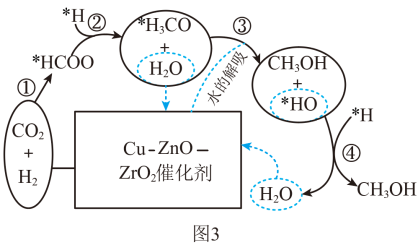
(4)我国科研人员研究出在Cu—ZnO—ZrO2催化剂上CO2氢化合成甲醇的反应历程如图3所示。反应③的化学方程式为___ ;分析在反应气中加入少量的水能够提升甲醇产率的可能原因是___ 。
I.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH1=+41.1kJ·mol-1II.CO(g)+2H2(g)
 CH3OH(g) ΔH2=-90.0kJ·mol-1
CH3OH(g) ΔH2=-90.0kJ·mol-1(1)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)ΔH=
CH3OH(g)+H2O(g)ΔH=(2)5Mpa时,往某密闭容器中按投料比n(H2)∶n(CO2)=3∶1充入H2和CO2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图1所示。

①图中X代表
②体系中H2的物质的量分数随温度的增大而升高,试分析原因
(3)H2和CO2起始物质的量比为3∶1时,该反应在有、无分子筛膜时甲醇的平衡产率随温度的变化如图2所示,其中分子筛膜能选择性分离出H2O。温度低于210℃时,随着温度升高,有分子筛膜的甲醇产率升高的可能原因是

(4)我国科研人员研究出在Cu—ZnO—ZrO2催化剂上CO2氢化合成甲醇的反应历程如图3所示。反应③的化学方程式为

您最近一年使用:0次
2 . 随着科技的进步,合理利用资源保护环境成为当今社会关注的焦点。甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g)ΔH=?已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g)ΔH=?已知该反应中相关化学键的键能数据如下:
则该反应的ΔH=_______ kJ·mol-1。
(2)上述反应中所需的甲醇工业上有多种方法合成。用电解法也可实现CO2加氢制甲醇(稀硫酸作电解质溶液)。电解时,阴极上的电极反应为_______ 。
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,则每生成3molPbI2的反应中,转移电子的物质的量为_______ 。
(4)分解HI曲线和液相法制备HI反应曲线分别如下图1和图2所示:
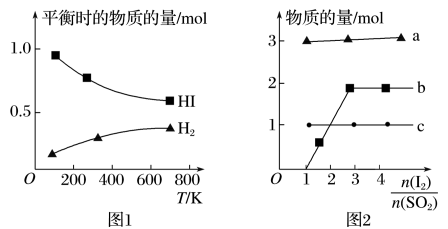
①反应H2(g)+I2(g) 2HI(g)的ΔH
2HI(g)的ΔH_______ 0(填“大于”或“小于”)。
②将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O=3H++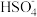 +2I-,I2+I-
+2I-,I2+I-
 ,图2中曲线c代表的微粒是
,图2中曲线c代表的微粒是_______ (填微粒符号),由图2可知,要提高碘的还原率,除控制温度外,还可以采取的措施是_______ 。
(1)制取甲胺的反应为CH3OH(g)+NH3(g)
 CH3NH2(g)+H2O(g)ΔH=?已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g)ΔH=?已知该反应中相关化学键的键能数据如下:共价键 | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 |
(2)上述反应中所需的甲醇工业上有多种方法合成。用电解法也可实现CO2加氢制甲醇(稀硫酸作电解质溶液)。电解时,阴极上的电极反应为
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,则每生成3molPbI2的反应中,转移电子的物质的量为
(4)分解HI曲线和液相法制备HI反应曲线分别如下图1和图2所示:

①反应H2(g)+I2(g)
 2HI(g)的ΔH
2HI(g)的ΔH②将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O=3H++
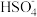 +2I-,I2+I-
+2I-,I2+I-
 ,图2中曲线c代表的微粒是
,图2中曲线c代表的微粒是
您最近一年使用:0次



