1 . 已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在平衡:[Co(H2O)6]2++4Cl-⇌[CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:

| A.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为3:2 |
| B.由实验①可推知∆H>0 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性: [ZnCl4]2->[CoCl4]2- |
您最近半年使用:0次
2010高三·湖北·竞赛
2 . 在一个体积可变的密闭容器中,通入2molHI气体,在一定条件下建立如下平衡:2HI(g)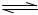 I2(g)+H2(g) △H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
I2(g)+H2(g) △H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
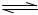 I2(g)+H2(g) △H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
I2(g)+H2(g) △H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是| A.保持容器体积不变,升高温度,混合气体的颜色逐渐变浅 |
| B.保持容器体积与温度不变,充入一定量氦气(不参与反应),则正反应速率和逆反应速率均增大 |
| C.保持温度不变,缓慢压缩容器,使容器体积恒定为0.2L,一定时间后,测得c(I2)=2.5mol/L |
| D.保持容器压强和温度不变,再通入2molHI气体,到达平衡状态后,测得HI的转化率为60% |
您最近半年使用:0次



