名校
解题方法
1 . 中国科学家首次实现了二氧化碳到淀粉的从头合成,相关成果由国际知名学术期刊《科学》在线发表,因此CO2的捕集及其资源化利用成为科学家研究的重要课题。
I.二氧化碳合成“合成气”
(1)捕获的高浓度CO2能与CH4制备合成气(CO、H2),该过程主要涉及以下反应:
①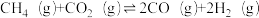 ;△H1
;△H1
②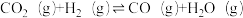 ;△H2
;△H2
③ ;△H3
;△H3
④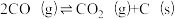 ;△H4
;△H4
根据盖斯定律,反应①的△H1=_____________ (写出代数式即可)。
Ⅱ.二氧化碳合成低碳烯烃
(2)用可再生能源电还原CO2时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图1所示。阴极发生的反应为____________ ;
每转移1mol电子,阳极生成____________ L气体(标准状况)。
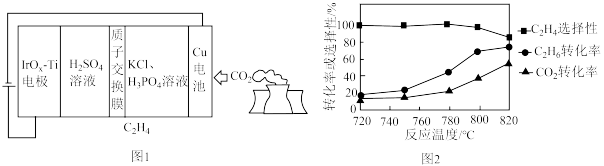
(3)以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
A.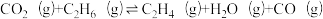 ;
; (主反应)
(主反应)
B.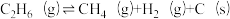 ;
;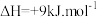 (副反应)
(副反应)
其中,反应A的反应历程可分为如下两步:
A. ;△H1(反应速率较快)
;△H1(反应速率较快)
B. ;
;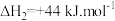 (反应速率较慢)
(反应速率较慢)
相比于提高c(C2H6),则提高c(CO2)对反应A速率影响更大,原因是____________ 。
向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂KFeMn/Si2性能的影响如图2所示,工业生产综合各方面的因素,反应选择800℃的原因是____________ 。
Ⅲ.二氧化碳合成甲醇
主反应: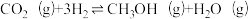 ;
;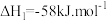
副反应: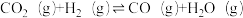 ;
;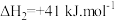
某一刚性容器中充入1molCO2和3molH2,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图3所示。已知:CH3OH选择性=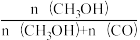
(4)240℃平衡时,生成的CH3OH的物质的量是____________ 。

Ⅳ、新型二氧化碳固定法
(5)某课题组设计一种新型的固定CO2方法,如图4所示。若原料用 ,则产物为
,则产物为____________ 。
I.二氧化碳合成“合成气”
(1)捕获的高浓度CO2能与CH4制备合成气(CO、H2),该过程主要涉及以下反应:
①
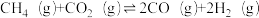 ;△H1
;△H1②
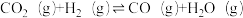 ;△H2
;△H2③
 ;△H3
;△H3④
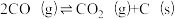 ;△H4
;△H4根据盖斯定律,反应①的△H1=
Ⅱ.二氧化碳合成低碳烯烃
(2)用可再生能源电还原CO2时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图1所示。阴极发生的反应为
每转移1mol电子,阳极生成
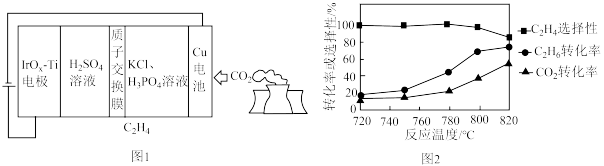
(3)以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
A.
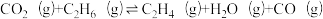 ;
; (主反应)
(主反应)B.
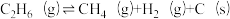 ;
;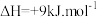 (副反应)
(副反应)其中,反应A的反应历程可分为如下两步:
A.
 ;△H1(反应速率较快)
;△H1(反应速率较快)B.
 ;
;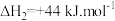 (反应速率较慢)
(反应速率较慢)相比于提高c(C2H6),则提高c(CO2)对反应A速率影响更大,原因是
向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂KFeMn/Si2性能的影响如图2所示,工业生产综合各方面的因素,反应选择800℃的原因是
Ⅲ.二氧化碳合成甲醇
主反应:
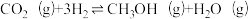 ;
;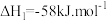
副反应:
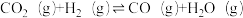 ;
;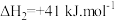
某一刚性容器中充入1molCO2和3molH2,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图3所示。已知:CH3OH选择性=
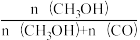
(4)240℃平衡时,生成的CH3OH的物质的量是

Ⅳ、新型二氧化碳固定法
(5)某课题组设计一种新型的固定CO2方法,如图4所示。若原料用
 ,则产物为
,则产物为
您最近一年使用:0次



