1 . 氮的氧化物(如 、
、 、
、 等)应用很广,一定条件下可以相互转化。
等)应用很广,一定条件下可以相互转化。
(1)已知: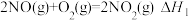
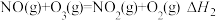

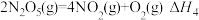
则反应 的
的
_______ 。
(2) 与
与 之间存在反应
之间存在反应 。将一定量的
。将一定量的 放入恒容密闭容器中,测得其平衡转化率
放入恒容密闭容器中,测得其平衡转化率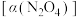 随温度变化如图1所示:
随温度变化如图1所示:
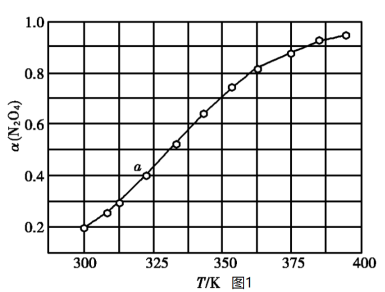
①图1中a点对应温度下,已知 的起始压强
的起始压强 为
为 ,计算该温度下反应的平衡常数
,计算该温度下反应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;计算结果保留至小数点后一位)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;计算结果保留至小数点后一位)。
②由图1推测 正向是
正向是_______ (填“吸热反应”或“放热反应”),说明理由:_______ 。
③对于反应 ,在一定条件下
,在一定条件下 与
与 的消耗速率与自身压强存在关系:
的消耗速率与自身压强存在关系: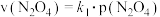 ,
,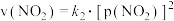 。其中,
。其中, 、
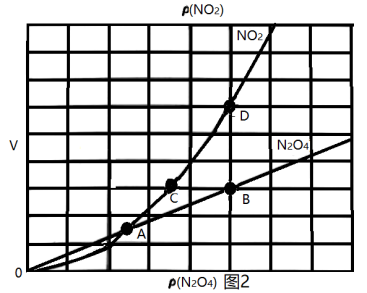
、 是与反应及温度有关的常数。相应的速率-压强关系如图2所示,一定温度下,
是与反应及温度有关的常数。相应的速率-压强关系如图2所示,一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是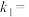
_______ ,在图2标出的点中,指出能表示反应达到平衡状态的点是:_______ 。
(3)以 为原料可以制得新型绿色硝化剂
为原料可以制得新型绿色硝化剂 ,原理是先将
,原理是先将 转化为
转化为 ,然后采用电解法制备
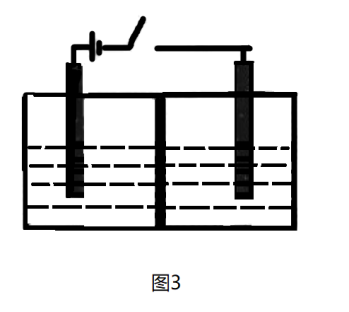
,然后采用电解法制备 ,其装置如图3所示,两端电极为石墨电极,中间隔膜只允许离子通过,不允许水分子通过。已知两室中加入的试剂分别为:a.硝酸;b.
,其装置如图3所示,两端电极为石墨电极,中间隔膜只允许离子通过,不允许水分子通过。已知两室中加入的试剂分别为:a.硝酸;b. 和无水硝酸,则左室中电极反应式为
和无水硝酸,则左室中电极反应式为_______ 。
 、
、 、
、 等)应用很广,一定条件下可以相互转化。
等)应用很广,一定条件下可以相互转化。(1)已知:
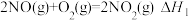
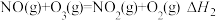

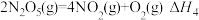
则反应
 的
的
(2)
 与
与 之间存在反应
之间存在反应 。将一定量的
。将一定量的 放入恒容密闭容器中,测得其平衡转化率
放入恒容密闭容器中,测得其平衡转化率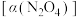 随温度变化如图1所示:
随温度变化如图1所示:


①图1中a点对应温度下,已知
 的起始压强
的起始压强 为
为 ,计算该温度下反应的平衡常数
,计算该温度下反应的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;计算结果保留至小数点后一位)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;计算结果保留至小数点后一位)。②由图1推测
 正向是
正向是③对于反应
 ,在一定条件下
,在一定条件下 与
与 的消耗速率与自身压强存在关系:
的消耗速率与自身压强存在关系: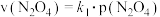 ,
,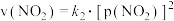 。其中,
。其中, 、
、 是与反应及温度有关的常数。相应的速率-压强关系如图2所示,一定温度下,
是与反应及温度有关的常数。相应的速率-压强关系如图2所示,一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是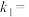
(3)以
 为原料可以制得新型绿色硝化剂
为原料可以制得新型绿色硝化剂 ,原理是先将
,原理是先将 转化为
转化为 ,然后采用电解法制备
,然后采用电解法制备 ,其装置如图3所示,两端电极为石墨电极,中间隔膜只允许离子通过,不允许水分子通过。已知两室中加入的试剂分别为:a.硝酸;b.
,其装置如图3所示,两端电极为石墨电极,中间隔膜只允许离子通过,不允许水分子通过。已知两室中加入的试剂分别为:a.硝酸;b. 和无水硝酸,则左室中电极反应式为
和无水硝酸,则左室中电极反应式为
您最近一年使用:0次



