2023高三·全国·专题练习
解题方法
1 . 计算 时下列溶液的
时下列溶液的
(1)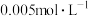 的
的 溶液的
溶液的
________ 。
(2) 的
的 溶液的
溶液的
_______ 。
(3) 的盐酸加水稀释到1000倍,溶液的
的盐酸加水稀释到1000倍,溶液的
________ 。
(4)将 的
的 溶液与
溶液与 的
的 溶液等体积混合,混合溶液的
溶液等体积混合,混合溶液的
__________ 。
(5)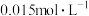 的硫酸与
的硫酸与 的
的 溶液等体积混合,混合溶液的
溶液等体积混合,混合溶液的
_________ 。
 时下列溶液的
时下列溶液的
(1)
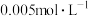 的
的 溶液的
溶液的
(2)
 的
的 溶液的
溶液的
(3)
 的盐酸加水稀释到1000倍,溶液的
的盐酸加水稀释到1000倍,溶液的
(4)将
 的
的 溶液与
溶液与 的
的 溶液等体积混合,混合溶液的
溶液等体积混合,混合溶液的
(5)
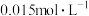 的硫酸与
的硫酸与 的
的 溶液等体积混合,混合溶液的
溶液等体积混合,混合溶液的
您最近一年使用:0次
2 . 25℃时,醋酸电离平衡常数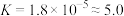 ,
,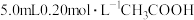 溶液与
溶液与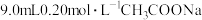 溶液混合均匀(混合后溶液体积不变)。请计算:
溶液混合均匀(混合后溶液体积不变)。请计算:
(1)求混合液的
_______ (保留2位有效数字,下同)。
(2)向混合液中加0.10mL(2滴) 盐酸,求此时溶液中
盐酸,求此时溶液中
_______  。(写出计算过程)
。(写出计算过程)
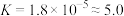 ,
,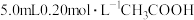 溶液与
溶液与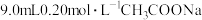 溶液混合均匀(混合后溶液体积不变)。请计算:
溶液混合均匀(混合后溶液体积不变)。请计算:(1)求混合液的

(2)向混合液中加0.10mL(2滴)
 盐酸,求此时溶液中
盐酸,求此时溶液中
 。(写出计算过程)
。(写出计算过程)
您最近一年使用:0次
2021-05-16更新
|
419次组卷
|
2卷引用:浙江省普通高中强基联盟协作体2021届高三下学期统测化学试题
解题方法
3 . 为测定市售食用白醋的醋酸浓度,室温下取10mL市售白醋样品,稀释并定容至100 mL,取20.00 mL溶液,滴定至终点时共用去0.1000 mol·L-1NaOH标准溶液16.00ml。
(1)计算市售白醋中醋酸浓度为_______ moL•L-1。
(2)实验过程中当醋酸与NaOH的物质的量之比为1:1时,溶液中的 =
= 求此时溶液的pH=
求此时溶液的pH=_______ (已知室温下醋酸的Ka=1.8×10-5)。
(1)计算市售白醋中醋酸浓度为
(2)实验过程中当醋酸与NaOH的物质的量之比为1:1时,溶液中的
 =
= 求此时溶液的pH=
求此时溶液的pH=
您最近一年使用:0次
解题方法
4 . 现有浓度均为0.1mol•L-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵。请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)__ 。
(2)已知T℃,KW=1×10-13,则t℃___ 25℃(填“>”、“<”或“=”)。在T℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=_ 。
(3)25℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与bL该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=__ (填数据);
②若x+y>14,则a/b=__ (填表达式);
③该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为__ (填表达式)。
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)
(2)已知T℃,KW=1×10-13,则t℃
(3)25℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与bL该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=
②若x+y>14,则a/b=
③该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为
您最近一年使用:0次



