1 . I.某研究小组进行 的沉淀溶解平衡的实验探究。
的沉淀溶解平衡的实验探究。
【查阅资料】25℃时,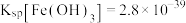 ,
,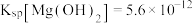
【制备试剂】向2支均盛有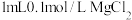 溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量
溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量 沉淀。
沉淀。
(1)分别向两支试管中加入不同试剂,请填写下表中的实验现象、反应离子方程式。
(2)同学们猜想产生试管II中现象的主要原因有以下两种。
猜想1: 结合
结合 电离出的
电离出的 ,使
,使 的沉淀溶解平衡正向移动。
的沉淀溶解平衡正向移动。
猜想2:___________ 。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁固体盛放在两支试管中,一支试管中加入VmL醋酸铵溶液(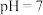 ),另一支试管中加入
),另一支试管中加入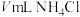 和氨水混合液(
和氨水混合液(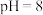 ),两支试管中氢氧化镁均溶解。该实验证明(2)中
),两支试管中氢氧化镁均溶解。该实验证明(2)中___________ (填“猜想1”或“猜想2”)正确。
II.工业上常用惰性电极电解硫酸钠溶液联合生产硫酸和烧碱,生产装置如图所示。测得同温同压下,气体甲、乙的体积比约为1:2。
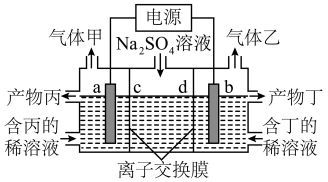
(4)b电极反应式是___________ ,离子交换膜d为___________ (填“阳”或“阴”)离子交换膜,产物丙为___________ 溶液(填“名称”)
III.某些弱酸在25°C时的电离常数如下:
(5)下列反应可以发生的是___________(填标号)。
 的沉淀溶解平衡的实验探究。
的沉淀溶解平衡的实验探究。【查阅资料】25℃时,
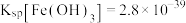 ,
,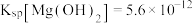
【制备试剂】向2支均盛有
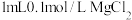 溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量
溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量 沉淀。
沉淀。(1)分别向两支试管中加入不同试剂,请填写下表中的实验现象、反应离子方程式。
| 试管编号 | 加入试剂 | 实验现象 | 反应离子方程式 |
| I | 2滴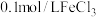 溶液 溶液 | ① | ② |
| II | 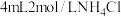 溶液 溶液 | 白色沉淀溶解,得无色溶液 |
猜想1:
 结合
结合 电离出的
电离出的 ,使
,使 的沉淀溶解平衡正向移动。
的沉淀溶解平衡正向移动。猜想2:
(3)为验证猜想,同学们取少量相同质量的氢氧化镁固体盛放在两支试管中,一支试管中加入VmL醋酸铵溶液(
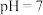 ),另一支试管中加入
),另一支试管中加入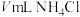 和氨水混合液(
和氨水混合液(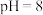 ),两支试管中氢氧化镁均溶解。该实验证明(2)中
),两支试管中氢氧化镁均溶解。该实验证明(2)中II.工业上常用惰性电极电解硫酸钠溶液联合生产硫酸和烧碱,生产装置如图所示。测得同温同压下,气体甲、乙的体积比约为1:2。

(4)b电极反应式是
III.某些弱酸在25°C时的电离常数如下:
| 弱电解质 |  | HSCN | HCN | HClO |  |
 |  | 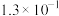 |  |  |   |
A. |
B. |
C. |
D.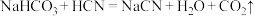 |
您最近一年使用:0次
2022-01-17更新
|
173次组卷
|
2卷引用:山西省怀仁市2021-2022学年高二上学期期末调研化学试题



