解题方法
1 . 化学消毒剂能够有效阻断病毒的传播与扩散。本题中,将探讨2种常见的消毒剂:
Ⅰ.二氧化氯 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于 就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)某小组按照文献中制备 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。
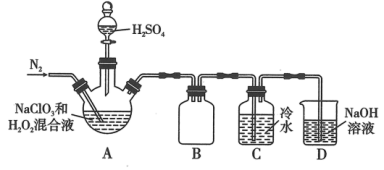
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是_______ 。
②装置A中,装 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)测定装置 中
中 溶液的浓度:取
溶液的浓度:取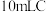 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化(
酸化( ),然后加入
),然后加入_______ 作指示剂,用 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液(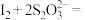 2I-+S4O
2I-+S4O ),当看到
),当看到_______ 现象时,测得标准液消耗的体积为 ,通过计算可知
,通过计算可知 中
中 溶液的浓度为
溶液的浓度为_______  。
。
Ⅱ.84消毒液在生活中有广泛的应用,其主要成分是 和
和 。
。
资料: 的电离常数
的电离常数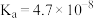 ;
; 的电离常数
的电离常数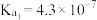 ,
,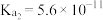 ;
; 的氧化性和杀菌消毒效果强于
的氧化性和杀菌消毒效果强于 。
。
(3)84消毒液溶液呈_______ (填“酸性”或“碱性”)。
(4)84消毒液可由氯气与 溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的
溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的 ,请运用平衡移动原理解释
,请运用平衡移动原理解释 的作用
的作用_______ 。
(5)待消杀物品喷洒上84消毒液后,露置于空气中10~30分钟可增强消毒效果,该过程中发生反应的离子方程式为_______ 。
Ⅰ.二氧化氯
 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于 就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:(1)某小组按照文献中制备
 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
②装置A中,装
 溶液的仪器名称为
溶液的仪器名称为(2)测定装置
 中
中 溶液的浓度:取
溶液的浓度:取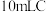 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化(
酸化( ),然后加入
),然后加入 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液(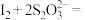 2I-+S4O
2I-+S4O ),当看到
),当看到 ,通过计算可知
,通过计算可知 中
中 溶液的浓度为
溶液的浓度为 。
。Ⅱ.84消毒液在生活中有广泛的应用,其主要成分是
 和
和 。
。资料:
 的电离常数
的电离常数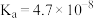 ;
; 的电离常数
的电离常数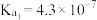 ,
,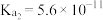 ;
; 的氧化性和杀菌消毒效果强于
的氧化性和杀菌消毒效果强于 。
。(3)84消毒液溶液呈
(4)84消毒液可由氯气与
 溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的
溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的 ,请运用平衡移动原理解释
,请运用平衡移动原理解释 的作用
的作用(5)待消杀物品喷洒上84消毒液后,露置于空气中10~30分钟可增强消毒效果,该过程中发生反应的离子方程式为
您最近半年使用:0次
名校
2 . “消洗灵”是具有消毒、杀菌、漂白和洗涤等综合功效的固体粉末,消毒原理与“84消毒液”相似,化学组成可以表示为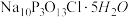 (磷酸三钠次氯酸钠)。实验室制备装置和过程如图:
(磷酸三钠次氯酸钠)。实验室制备装置和过程如图:
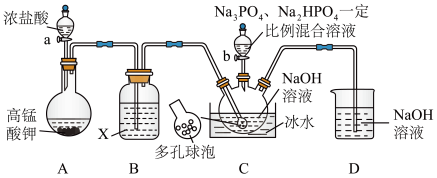
回答下列问题:
(1)仪器a的名称为___________ ,C中采用多孔球泡的目的是___________ 。
(2)磷酸是三元弱酸,常温下三级电离常数分别是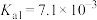 ,
, ,
,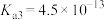 ,常温下同浓度
,常温下同浓度 、
、 的混合溶液pH
的混合溶液pH_______ (填“>”“<”或“=”)7。
(3)“消洗灵”消毒时对金属腐蚀性小,原因是在金属表面形成一种不溶性磷酸盐膜,对金属有良好的保护作用,在空气中对镁合金消毒,磷酸钠溶液使镁合金表面形成含有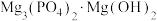 的保护层,写出反应的化学方程式:
的保护层,写出反应的化学方程式:___________ 。
(4)产品纯度测定(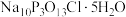 的摩尔质量为656.5
的摩尔质量为656.5  )。
)。
①取a g待测试样溶于蒸馏水配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2 稀硫酸、25 mL 0.1
稀硫酸、25 mL 0.1  碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;
③滴入3滴5%淀粉溶液,用0.05 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。
已知: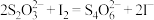 ,达到滴定终点的现象为
,达到滴定终点的现象为___________ ,产品的纯度为___________ (用含a的代数式表示)。若滴定前滴定管中含有气泡,滴定结束无气泡会造成纯度测定值___________ (填“偏大”“偏小”或“不变”)。
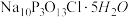 (磷酸三钠次氯酸钠)。实验室制备装置和过程如图:
(磷酸三钠次氯酸钠)。实验室制备装置和过程如图: 
回答下列问题:
(1)仪器a的名称为
(2)磷酸是三元弱酸,常温下三级电离常数分别是
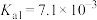 ,
, ,
,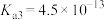 ,常温下同浓度
,常温下同浓度 、
、 的混合溶液pH
的混合溶液pH(3)“消洗灵”消毒时对金属腐蚀性小,原因是在金属表面形成一种不溶性磷酸盐膜,对金属有良好的保护作用,在空气中对镁合金消毒,磷酸钠溶液使镁合金表面形成含有
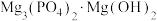 的保护层,写出反应的化学方程式:
的保护层,写出反应的化学方程式:(4)产品纯度测定(
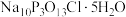 的摩尔质量为656.5
的摩尔质量为656.5  )。
)。①取a g待测试样溶于蒸馏水配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2
 稀硫酸、25 mL 0.1
稀硫酸、25 mL 0.1  碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;③滴入3滴5%淀粉溶液,用0.05
 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。已知:
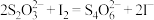 ,达到滴定终点的现象为
,达到滴定终点的现象为
您最近半年使用:0次
名校
3 . “84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法并测定相关反应的平衡常数。
资料:i.HClO的电离常数为Ka=4.7×10-8;H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11
ii.碘的化合物主要以I-和 的形式存在,
的形式存在, +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-
 (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。
I制备消毒液(夹持装置略)
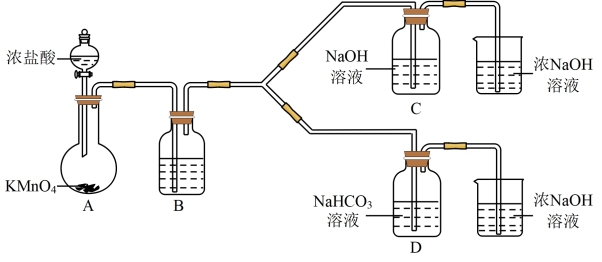
(1)制备NaClO的离子反应方程式___________ 。
(2)结合资料i,写出D中反应的化学方程式___________ 。
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(3)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为 。
。
设计实验a证实了假设1成立。NaClO氧化I2生成 的离子方程式是
的离子方程式是___________ 。
假设2:生成的I2在碱性溶液中不能存在。
设计实验b证实了假设2成立,实验b的操作及现象是___________ 。
(4)某小组检验烧杯3所得溶液中含 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由___________ 。
(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据___________ 。
资料:i.HClO的电离常数为Ka=4.7×10-8;H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11
ii.碘的化合物主要以I-和
 的形式存在,
的形式存在, +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。iii.碘单质能与I-反应:I2+I-

 (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。I制备消毒液(夹持装置略)

(1)制备NaClO的离子反应方程式
(2)结合资料i,写出D中反应的化学方程式
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9gKI固体 | |溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9gKI固体,再加入1mol/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
假设1:过量的NaClO将反应生成的I2氧化为
 。
。设计实验a证实了假设1成立。NaClO氧化I2生成
 的离子方程式是
的离子方程式是假设2:生成的I2在碱性溶液中不能存在。
设计实验b证实了假设2成立,实验b的操作及现象是
(4)某小组检验烧杯3所得溶液中含
 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
您最近半年使用:0次
2022-05-31更新
|
507次组卷
|
3卷引用:北京市第一六六中学2022届高三下学期三模化学试题
4 . I.某研究小组进行 的沉淀溶解平衡的实验探究。
的沉淀溶解平衡的实验探究。
【查阅资料】25℃时,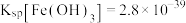 ,
,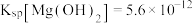
【制备试剂】向2支均盛有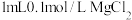 溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量
溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量 沉淀。
沉淀。
(1)分别向两支试管中加入不同试剂,请填写下表中的实验现象、反应离子方程式。
(2)同学们猜想产生试管II中现象的主要原因有以下两种。
猜想1: 结合
结合 电离出的
电离出的 ,使
,使 的沉淀溶解平衡正向移动。
的沉淀溶解平衡正向移动。
猜想2:___________ 。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁固体盛放在两支试管中,一支试管中加入VmL醋酸铵溶液(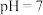 ),另一支试管中加入
),另一支试管中加入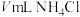 和氨水混合液(
和氨水混合液(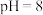 ),两支试管中氢氧化镁均溶解。该实验证明(2)中
),两支试管中氢氧化镁均溶解。该实验证明(2)中___________ (填“猜想1”或“猜想2”)正确。
II.工业上常用惰性电极电解硫酸钠溶液联合生产硫酸和烧碱,生产装置如图所示。测得同温同压下,气体甲、乙的体积比约为1:2。
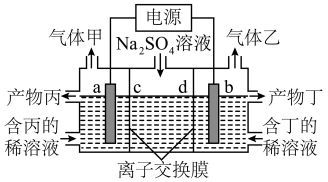
(4)b电极反应式是___________ ,离子交换膜d为___________ (填“阳”或“阴”)离子交换膜,产物丙为___________ 溶液(填“名称”)
III.某些弱酸在25°C时的电离常数如下:
(5)下列反应可以发生的是___________(填标号)。
 的沉淀溶解平衡的实验探究。
的沉淀溶解平衡的实验探究。【查阅资料】25℃时,
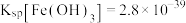 ,
,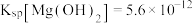
【制备试剂】向2支均盛有
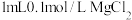 溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量
溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量 沉淀。
沉淀。(1)分别向两支试管中加入不同试剂,请填写下表中的实验现象、反应离子方程式。
| 试管编号 | 加入试剂 | 实验现象 | 反应离子方程式 |
| I | 2滴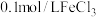 溶液 溶液 | ① | ② |
| II | 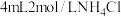 溶液 溶液 | 白色沉淀溶解,得无色溶液 |
猜想1:
 结合
结合 电离出的
电离出的 ,使
,使 的沉淀溶解平衡正向移动。
的沉淀溶解平衡正向移动。猜想2:
(3)为验证猜想,同学们取少量相同质量的氢氧化镁固体盛放在两支试管中,一支试管中加入VmL醋酸铵溶液(
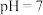 ),另一支试管中加入
),另一支试管中加入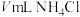 和氨水混合液(
和氨水混合液(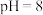 ),两支试管中氢氧化镁均溶解。该实验证明(2)中
),两支试管中氢氧化镁均溶解。该实验证明(2)中II.工业上常用惰性电极电解硫酸钠溶液联合生产硫酸和烧碱,生产装置如图所示。测得同温同压下,气体甲、乙的体积比约为1:2。

(4)b电极反应式是
III.某些弱酸在25°C时的电离常数如下:
| 弱电解质 |  | HSCN | HCN | HClO |  |
 |  | 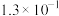 |  |  |   |
A. |
B. |
C. |
D.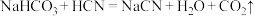 |
您最近半年使用:0次
2022-01-17更新
|
173次组卷
|
2卷引用:山西省怀仁市2021-2022学年高二上学期期末调研化学试题
5 . “84消毒液”因1984年北京某医院研制使用而得名,在2020年抗击新型冠状病毒肺炎中被广泛用于消毒,其有效成分是NaClO。某校化学研究性学习小组在实验室制备NaClO溶液,并进行性质探究和成分测定。
已知:①室温下,饱和NaClO溶液pH为11
②25℃时,H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8
I.制备NaClO溶液
该学习小组按下图装置进行实验(部分夹持装置省去)

(1)上图中A为实验室制备Cl2的发生装置,可以选用下列图中_ (填代号)装置,用该装置制备Cl2反应的化学方程式为__ 。
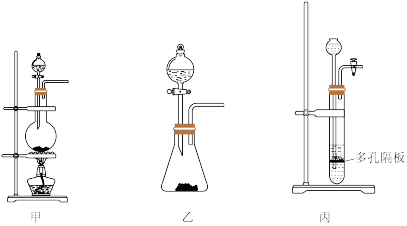
(2)B装置中仪器a的名称是____ ,B装置可除去氯气中氯化氢杂质, 此外还有______ 作用(写出一点)。
II.NaClO性质探究
按上图装置进行实验,一段时间后,取C瓶中的溶液进行实验,如下表:
(3)C瓶溶液中的溶质除NaCl外,还有______ (填化学式)。
(4)将C瓶中NaOH溶液换成NaHCO3溶液,反应一段时间后,取C瓶中的溶液按上表实验内容进行实验。现象为:实验l中紫色石蕊试液立即褪色,实验2中溶液的pH=7。结合平衡移动原理解释紫色石蕊试液立即褪色的原因是________ 。
III.测定C瓶溶液中NaClO含量(单位:g·L-1)
i.取C瓶溶液10.00mL于锥形瓶中,加入适量硫酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
ii.用0.1000mol•L-1Na2S2O3标准溶液滴定上述锥形瓶中的溶液至终点,重复操作2~3次,消耗Na2S2O3溶液的平均用量为12.00mL。(已知:I2+2 =2I-+
=2I-+ )
)
(5)i中主要发生反应的离子方程式为_______ ,ii中用_______ 作指示剂。
(6)盖紧瓶塞并在暗处反应的原因是________ 。
(7)C瓶溶液中NaClO含量是______ g·L-1(保留2位小数)。
已知:①室温下,饱和NaClO溶液pH为11
②25℃时,H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8
I.制备NaClO溶液
该学习小组按下图装置进行实验(部分夹持装置省去)

(1)上图中A为实验室制备Cl2的发生装置,可以选用下列图中

(2)B装置中仪器a的名称是
II.NaClO性质探究
按上图装置进行实验,一段时间后,取C瓶中的溶液进行实验,如下表:
| 实验内容 | 实验现象 | |
| 实验l | 取样,滴加紫色石蕊试液 | 变蓝,不褪色 |
| 实验2 | 测定溶液的pH | 12 |
(4)将C瓶中NaOH溶液换成NaHCO3溶液,反应一段时间后,取C瓶中的溶液按上表实验内容进行实验。现象为:实验l中紫色石蕊试液立即褪色,实验2中溶液的pH=7。结合平衡移动原理解释紫色石蕊试液立即褪色的原因是
III.测定C瓶溶液中NaClO含量(单位:g·L-1)
i.取C瓶溶液10.00mL于锥形瓶中,加入适量硫酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
ii.用0.1000mol•L-1Na2S2O3标准溶液滴定上述锥形瓶中的溶液至终点,重复操作2~3次,消耗Na2S2O3溶液的平均用量为12.00mL。(已知:I2+2
 =2I-+
=2I-+ )
)(5)i中主要发生反应的离子方程式为
(6)盖紧瓶塞并在暗处反应的原因是
(7)C瓶溶液中NaClO含量是
您最近半年使用:0次
2020-07-11更新
|
309次组卷
|
3卷引用:福建省南平市2020届高三第三次综合质量检测理科综合化学试题
名校
6 . 硫酸和醋酸都是重要的化工原料,在生产、科研中用途广泛。回答下列问题:
(1)①某温度(t℃)时,水的离子积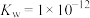 ,则t℃
,则t℃___________ 25℃(填“>”“<”或“=”)。此温度下, 的氨水中
的氨水中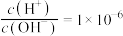 ,则该氨水溶液的pH=
,则该氨水溶液的pH=___________ ;
②将室温下pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得混合溶液的pH=3,则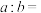
___________ 。
(2)某兴趣小组设计了如下实验,探究不同条件对KI溶液(硫酸酸化)被空气中O2氧化反应速率的影响:
①请完成下表(硫酸、KI溶液体积均为5mL,淀粉溶液用量相同):
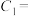
___________ ,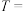
___________ 。
②该实验中通过观察___________ 实验现象判断反应的快慢。为此,该实验中三种溶液混合的顺序不合理的是___________ 。
a.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
b.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
c.先将KI溶液与硫酸溶液混合,然后再加入淀粉溶液
(3)25℃时,某Na2SO4溶液中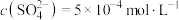 ,取该溶液1mL加水稀释至100mL,则稀释后溶液中
,取该溶液1mL加水稀释至100mL,则稀释后溶液中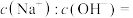
___________ 。
(4)在室温下,蒸馏水稀释0.01mol/LHA(HA为弱酸)溶液时,下列呈减小趋势的是___________。
(1)①某温度(t℃)时,水的离子积
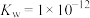 ,则t℃
,则t℃ 的氨水中
的氨水中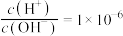 ,则该氨水溶液的pH=
,则该氨水溶液的pH=②将室温下pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得混合溶液的pH=3,则
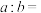
(2)某兴趣小组设计了如下实验,探究不同条件对KI溶液(硫酸酸化)被空气中O2氧化反应速率的影响:
①请完成下表(硫酸、KI溶液体积均为5mL,淀粉溶液用量相同):
| 实验编号 | T/K |  | 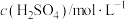 | 实验目的 |
| I | 298 | 1 | 0.1 | 实验I和II探究温度对该反应速率的影响;实验I和III探究反应物浓度对该反应速率的影响 |
| II | 308 |  |  | |
| III | T | 1 | 0.2 |
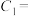
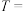
②该实验中通过观察
a.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
b.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
c.先将KI溶液与硫酸溶液混合,然后再加入淀粉溶液
(3)25℃时,某Na2SO4溶液中
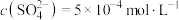 ,取该溶液1mL加水稀释至100mL,则稀释后溶液中
,取该溶液1mL加水稀释至100mL,则稀释后溶液中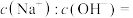
(4)在室温下,蒸馏水稀释0.01mol/LHA(HA为弱酸)溶液时,下列呈减小趋势的是___________。
| A.水的电离程度 | B. |
C.溶液中 和 和 的乘积 的乘积 | D.溶液中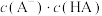 的值 的值 |
您最近半年使用:0次
名校
7 . 下列实验操作或做法正确且能达到目的的是
| 选项 | 实验操作或实验做法 | 实验目的 |
| A | 将过量 通入溴水中,溴水褪色 通入溴水中,溴水褪色 | 证明 具有漂白性 具有漂白性 |
| B | 向 溶液中通入少量的 溶液中通入少量的 生成白色沉淀 生成白色沉淀 | 证明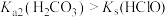 |
| C | 向盛有2  溶液的试管中滴加浓的维生素C溶液,观察颜色变化 溶液的试管中滴加浓的维生素C溶液,观察颜色变化 | 探究维生素C的还原性 |
| D | 向2支盛有5 不同浓度 不同浓度 溶液的试管中同时加入2 溶液的试管中同时加入2 0.2 0.2  溶液,观察实验现象 溶液,观察实验现象 | 探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-11-26更新
|
244次组卷
|
4卷引用:黑龙江省海伦市第一中学2022-2023学期高三上学期期中考试化学试卷题
黑龙江省海伦市第一中学2022-2023学期高三上学期期中考试化学试卷题(已下线)云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题山东省菏泽市鄄城县第一中学2023-2024学年高三上学期1月月考化学试题
8 . 为实现相关实验目的,选用的试剂、装置和操作均合理的是
| 实验目的 | 实验内容 | |
| A | 证明氨水中存在一水合氨的电离平衡 | 向含有酚酞的氨水中加入少量NaOH固体 |
| B | 配制100mL1.0 mol • L-1 NaOH 溶液 | 向100 mL容量瓶中加入4. 0 g NaOH固体,加水到刻度线 |
| C | 模拟利用牺牲阳极的阴极保护法保护铁 | 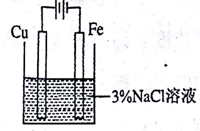 |
| D | 比较Cl-和I-的还原性 | 将少量Cl2通入滴有淀粉溶液的KI溶液中 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 生活处处有化学,化学知识无处不在。用所学知识解释工业、生产、生活与科研中的相关现象。
(1)写出H2C2O4在溶液中发生第一步电离的方程式:_______ ,写出该步电离常数的表达式Ka1=_______ 。
(2)水的离子积表达式Kw=_______ 。常温下0.01 mol/L HCl 溶液的水电离出的 c(H +)=_______ pH=11的CH3 COONa 溶液中由水电离产生的 c(OH-)=_______ 。
(3)CH3COONa溶液呈碱性的原因_______ (用离子方程式)。
(4)将饱和FeCl3的水溶液加入沸水中可以制备胶体,原因是:_______ (用离子方程式表示)。如果加热制备所得胶体,观察到颜色变化为_______ 。
(5)学过的平衡常数有化学平衡常数(K)、电离平衡常数(Ka\Kb)、水的离子积常数(Kw)、盐的水解常数(Kh),后面还会学习沉淀溶解平衡,其常数叫溶度积Ksp。其实这些常数有很多相似之处。任写一点_______ 。(符合题意的答案,均可给分)
(6)如除去MgCl2溶液中Fe3+需要的除杂试剂是_______ 。
(7)泡沫灭火器中筒体内的硫酸铝酸性溶液与碳酸氢钠碱性溶液混合发生化学反应,将生成的泡沫压出喷嘴, 喷射出去进行灭火的。写出对应的离子方程式_______ 。
(1)写出H2C2O4在溶液中发生第一步电离的方程式:
(2)水的离子积表达式Kw=
(3)CH3COONa溶液呈碱性的原因
(4)将饱和FeCl3的水溶液加入沸水中可以制备胶体,原因是:
(5)学过的平衡常数有化学平衡常数(K)、电离平衡常数(Ka\Kb)、水的离子积常数(Kw)、盐的水解常数(Kh),后面还会学习沉淀溶解平衡,其常数叫溶度积Ksp。其实这些常数有很多相似之处。任写一点
(6)如除去MgCl2溶液中Fe3+需要的除杂试剂是
(7)泡沫灭火器中筒体内的硫酸铝酸性溶液与碳酸氢钠碱性溶液混合发生化学反应,将生成的泡沫压出喷嘴, 喷射出去进行灭火的。写出对应的离子方程式
您最近半年使用:0次
10 . 填空
(1)25℃时,亚碲酸( )的
)的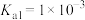 ,
,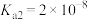 。常温下,
。常温下, 溶液的pH
溶液的pH______ (填“<”“>”或“=”)7。
(2)已知25℃时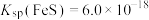 ,要使溶液中
,要使溶液中 沉淀完全[
沉淀完全[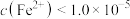 mol⋅L
mol⋅L ],则需控制溶液中
],则需控制溶液中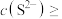
______ 。
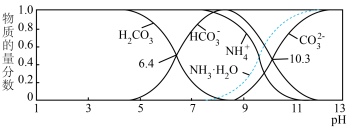
(3)室温下,测得用氨水吸收 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中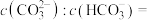
______ (已知) )。
)。
(4)若向浓烧碱溶液中通入 气体,使所得溶液
气体,使所得溶液 ,则此时溶液中的
,则此时溶液中的
______ mol⋅L (室温下,
(室温下, 的
的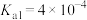 ,
,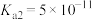 )。
)。
(5)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数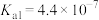 ,
, ,
, 的电离常数
的电离常数 ,则所得的
,则所得的 溶液中
溶液中
______ (填“>”“<”或“=”) 。
。
(6) 是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
①根据实验现象写出 和
和 反应的化学方程式:
反应的化学方程式:____________ 。
②利用 制备无水
制备无水 时,可用
时,可用 和
和 混合共热,试解释原因:
混合共热,试解释原因:____________ 。
(1)25℃时,亚碲酸(
 )的
)的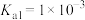 ,
,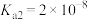 。常温下,
。常温下, 溶液的pH
溶液的pH(2)已知25℃时
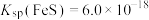 ,要使溶液中
,要使溶液中 沉淀完全[
沉淀完全[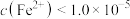 mol⋅L
mol⋅L ],则需控制溶液中
],则需控制溶液中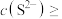
(3)室温下,测得用氨水吸收
 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中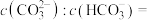
 )。
)。
(4)若向浓烧碱溶液中通入
 气体,使所得溶液
气体,使所得溶液 ,则此时溶液中的
,则此时溶液中的
 (室温下,
(室温下, 的
的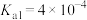 ,
,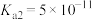 )。
)。(5)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体
 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数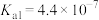 ,
, ,
, 的电离常数
的电离常数 ,则所得的
,则所得的 溶液中
溶液中
 。
。(6)
 是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。①根据实验现象写出
 和
和 反应的化学方程式:
反应的化学方程式:②利用
 制备无水
制备无水 时,可用
时,可用 和
和 混合共热,试解释原因:
混合共热,试解释原因:
您最近半年使用:0次



