名校
解题方法
1 . 纳米铁酸锰(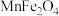 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
步骤1:按 ,称取
,称取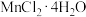 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
步骤2:配制浓度为 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;
步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为___________  。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是___________ (填字母)。___________ 。
②回流时的加热方式为___________ 。
③写出形成铁酸锰反应的离子方程式:___________ 。
(3)步骤4分离出铁酸锰的简单方法是___________ ,检验蒸馏水将铁酸锰洗涤干净的操作是___________ ,乙醇洗涤的目的是___________ 。
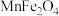 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:步骤1:按
 ,称取
,称取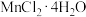 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;步骤2:配制浓度为
 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为
 。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是

②回流时的加热方式为
③写出形成铁酸锰反应的离子方程式:
(3)步骤4分离出铁酸锰的简单方法是
您最近一年使用:0次
2024-01-22更新
|
110次组卷
|
4卷引用:四川省内江市第三中学2023-2024学年高三1月月考理综试卷-高中化学
2 . 严谨的实验设计能有效规避实验风险,能重复实验并得到相同的结果。由粗盐制备试剂级的NaCl的相关实验步骤和装置如下:
【粗盐的提纯】
第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。
第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3,过滤,再用3.0mol/L HCl调节pH至1~2。
第III步,加热浓缩至溶液刚刚出现微晶膜。
(1)第I步加入BaCl2时,证明SO 已经除净的实验方法是
已经除净的实验方法是___________ 。
(2)第II步加入Na2CO3可以除去的离子为___________ 。
(3)第III步加热浓缩时所用到的硅酸盐材质的仪器有酒精灯、___________ ;已知:Ksp(BaCO3)=5.0×10-9、Ksp(BaSO4)=1.1×10-10;如果省略第I步“倾析法分离”,所得氯化钠溶液的纯度将___________ (填“升高”、“降低”或“不受影响”)。
【试剂级的NaCl的制备】
第IV步,将第III步浓缩溶液转移至下图装置C中继续实验。
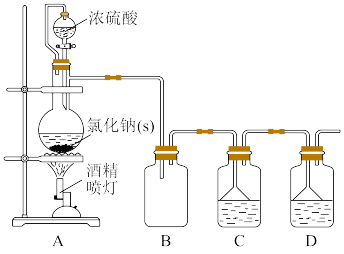
(4)装置A中发生的化学反应方程式为___________ ,控制该反应速率可采取的措施___________ (任答一点即可)。
(5)装置B中的广口瓶和装置C、D中的漏斗,其共同作用是___________ ,装置C的溶液中能观察到的实验现象是___________ 。装置D中盛放的试剂为___________ (填“NaOH溶液”、“NaHSO3溶液”或“浓H2SO4”)。
【粗盐的提纯】
第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。
第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3,过滤,再用3.0mol/L HCl调节pH至1~2。
第III步,加热浓缩至溶液刚刚出现微晶膜。
(1)第I步加入BaCl2时,证明SO
 已经除净的实验方法是
已经除净的实验方法是(2)第II步加入Na2CO3可以除去的离子为
(3)第III步加热浓缩时所用到的硅酸盐材质的仪器有酒精灯、
【试剂级的NaCl的制备】
第IV步,将第III步浓缩溶液转移至下图装置C中继续实验。

(4)装置A中发生的化学反应方程式为
(5)装置B中的广口瓶和装置C、D中的漏斗,其共同作用是
您最近一年使用:0次
2022-03-25更新
|
506次组卷
|
5卷引用:四川省内江市2022届高三下学期第二次模拟考试理科综合化学试题



