1 .  是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含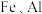 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下: )时的
)时的 如下表:
如下表:
② 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。
(1)“酸浸”时提高浸取率的措施有___________ (写出两条)。
(2)滤渣I的主要成分是___________ (填化学式)。
(3)操作 为调节溶液的
为调节溶液的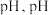 的最佳范围是
的最佳范围是___________ ,加入的物质X可以是___________ ( (填字母标号)。
A. B.
B.  C.
C.  D.
D.  溶液
溶液
(4)往滤液 中加入食盐并通入
中加入食盐并通入 可生成
可生成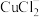 ,反应I的离子方程式为
,反应I的离子方程式为___________ ;在反应I中加入食盐并加热的目的是___________ 。
(5)实验室可以使用铜电极电解饱和食盐水得到 ,阳极的电极反应式为
,阳极的电极反应式为___________ 。
 是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含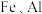 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下:
 )时的
)时的 如下表:
如下表:| 物质 |  |  |  |
开始沉淀时的 | 1.6 | 3.2 | 5.2 |
完全沉淀时的 | 3.1 | 4.7 | 6.7 |
 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。(1)“酸浸”时提高浸取率的措施有
(2)滤渣I的主要成分是
(3)操作
 为调节溶液的
为调节溶液的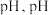 的最佳范围是
的最佳范围是A.
 B.
B.  C.
C.  D.
D.  溶液
溶液(4)往滤液
 中加入食盐并通入
中加入食盐并通入 可生成
可生成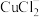 ,反应I的离子方程式为
,反应I的离子方程式为(5)实验室可以使用铜电极电解饱和食盐水得到
 ,阳极的电极反应式为
,阳极的电极反应式为
您最近半年使用:0次
2 . 常温时, 的溶度积
的溶度积 ,
, 在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是
在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是


 的溶度积
的溶度积 ,
, 在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是
在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是

A.常温时, 在 在 溶液中的 溶液中的 比在水中的小 比在水中的小 |
B.常温时, 的溶度积 的溶度积 |
C.向含等浓度 、 、 的混合溶液中滴加 的混合溶液中滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
D.向Y点溶液中加入 溶液,可使Y点移到Z点 溶液,可使Y点移到Z点 |
您最近半年使用:0次
名校
解题方法
3 . 相关物质的溶度积常数见下表(25℃):
下列有关说法不正确的是
| 物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
 | 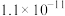 | 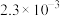 |  | 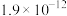 |
| A.浓度均为0.2mol/L的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.在其他条件不变的情况下,向饱和AgCl溶液中加入NaCl溶液,Ksp(AgCl)不变 |
| C.0.11mol/L的MgCl2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 |
| D.将0.001mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L的K2CrO4混合溶液中,先产生Ag2CrO4沉淀 |
您最近半年使用:0次
名校
解题方法
4 . 纳米铁酸锰(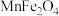 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
步骤1:按 ,称取
,称取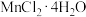 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
步骤2:配制浓度为 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;
步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为___________  。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是___________ (填字母)。___________ 。
②回流时的加热方式为___________ 。
③写出形成铁酸锰反应的离子方程式:___________ 。
(3)步骤4分离出铁酸锰的简单方法是___________ ,检验蒸馏水将铁酸锰洗涤干净的操作是___________ ,乙醇洗涤的目的是___________ 。
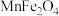 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:步骤1:按
 ,称取
,称取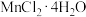 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;步骤2:配制浓度为
 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为
 。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是

②回流时的加热方式为
③写出形成铁酸锰反应的离子方程式:
(3)步骤4分离出铁酸锰的简单方法是
您最近半年使用:0次
2024-01-22更新
|
102次组卷
|
4卷引用:四川省内江市第三中学2023-2024学年高三1月月考理综试卷-高中化学
5 . 用沉淀溶解平衡原理解释不正确的是
A.误食钡盐[ 或 或 ]后,常用 ]后,常用 的 的 溶液解毒 溶液解毒 |
| B.升高温度,沉淀溶解平衡一定正向移动 |
C.向饱和 溶液中通入 溶液中通入 ,会看到有白色晶体析出 ,会看到有白色晶体析出 |
D.向浓度均为 的 的 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液,出现淡黄色沉淀,说明 溶液,出现淡黄色沉淀,说明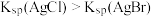 |
您最近半年使用:0次
名校
解题方法
6 . 以硅藻土为载体的五氧化二钒( )是接触法生产硫酸的催化剂。从废矾催化剂中回收
)是接触法生产硫酸的催化剂。从废矾催化剂中回收 既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为______ ,同时 转化成
转化成 。
。
(2)“废渣1”的主要成分是______ 。
(3)“氧化”中欲使3mol的 变为
变为 ,则需要氧化剂
,则需要氧化剂 至少为
至少为______ mol。
(4)“中和”作用之一是使钒以 形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有
形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有______ 。
(5)“离子交换”和“洗脱”可简单表示为 (ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈______ 性(填“酸”、“碱”或“中”)。
(6)“流出液”中阳离子最多的是______ 。
(7)“沉钒”得到偏钒酸铵( )沉淀,写出“煅烧”中发生反应的化学方程式
)沉淀,写出“煅烧”中发生反应的化学方程式______ 。
 )是接触法生产硫酸的催化剂。从废矾催化剂中回收
)是接触法生产硫酸的催化剂。从废矾催化剂中回收 既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为| 物质 |  |  |  |  |  |  |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时
 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为 转化成
转化成 。
。(2)“废渣1”的主要成分是
(3)“氧化”中欲使3mol的
 变为
变为 ,则需要氧化剂
,则需要氧化剂 至少为
至少为(4)“中和”作用之一是使钒以
 形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有
形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有(5)“离子交换”和“洗脱”可简单表示为
 (ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈(6)“流出液”中阳离子最多的是
(7)“沉钒”得到偏钒酸铵(
 )沉淀,写出“煅烧”中发生反应的化学方程式
)沉淀,写出“煅烧”中发生反应的化学方程式
您最近半年使用:0次
7 . 常温下, 在水中的沉淀溶解平衡曲线如图所示。已知:
在水中的沉淀溶解平衡曲线如图所示。已知: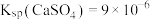 ,下列说法正确的是
,下列说法正确的是

 在水中的沉淀溶解平衡曲线如图所示。已知:
在水中的沉淀溶解平衡曲线如图所示。已知: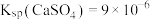 ,下列说法正确的是
,下列说法正确的是
A.在任何溶液中,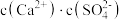 均相等 均相等 |
| B.d点溶液通过蒸发可以变到c点 |
C.b点对应的 大于a点对应的 大于a点对应的 |
D.b点将有沉淀生成,平衡后溶液中 一定小于 一定小于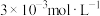 |
您最近半年使用:0次
2023-04-05更新
|
548次组卷
|
6卷引用:四川省内江市第六中学2022-2023学年高二下学期期中考试化学试题
四川省内江市第六中学2022-2023学年高二下学期期中考试化学试题2017届湖南省株洲市高三上教学质检一化学试卷四川省德阳市广汉中学2022-2023学年高二下学期第一次月考化学试题(已下线)专题五 沉淀溶解平衡图象(练)(已下线)T13-溶液中的离子平衡云南省保山市高(完)中C、D类学校2022-2023学年高二下学期6月份联考化学试题
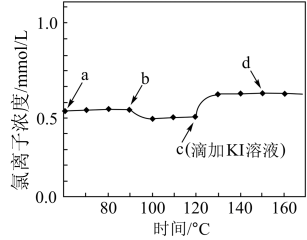
8 . 常温下,某研究小组用数字传感器探究 的沉淀溶解平衡。实验测得悬浊液中氯离子浓度变化如图所示,其中a点表示
的沉淀溶解平衡。实验测得悬浊液中氯离子浓度变化如图所示,其中a点表示 溶于
溶于 溶液形成的悬浊液。下列说法正确的是
溶液形成的悬浊液。下列说法正确的是
 的沉淀溶解平衡。实验测得悬浊液中氯离子浓度变化如图所示,其中a点表示
的沉淀溶解平衡。实验测得悬浊液中氯离子浓度变化如图所示,其中a点表示 溶于
溶于 溶液形成的悬浊液。下列说法正确的是
溶液形成的悬浊液。下列说法正确的是
A.图中b点可能是滴加 溶液 溶液 | B.图中c点后无黄色沉淀生成 |
C.图中d点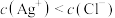 | D.由图可知: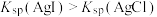 |
您最近半年使用:0次
2023-02-07更新
|
512次组卷
|
10卷引用:四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题
四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题广东省茂名市2021届高三第二次综合测试(4月)化学试题(已下线)2021年高考化学押题预测卷(福建卷)(01)(含考试版、答题卡、参考答案、全解全析)(已下线)难点8 水溶液中的四大平衡常数-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)第6周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)考向27 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点微专题湖南省长沙市雅礼书院中学2021-2022学年高三下学期第五次月考化学试题广东省江门市2022-2023学年高二化学上学期期末调研考试化学试题广东省深圳市深圳实验学校高中部2022-2023学年高二上学期第三阶段考试化学试题(已下线)题型27 沉淀溶解平衡常数及其应用图象
名校
解题方法
9 .  常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为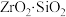 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。

已知:① 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的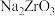 ,
,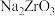 与酸反应生成
与酸反应生成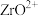 。
。
②部分金属离子在实验条件下开始沉淀和完全沉淀的 如表。
如表。
(1)熔融时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,滤渣Ⅰ的化学式为_______ 。
(2)滤液Ⅰ中除 外还含金属的阳离子有
外还含金属的阳离子有_______ ,为使滤液Ⅰ的杂质离子沉淀完全,需用氨水调 ,则a的范围是
,则a的范围是_______ 。
(3)继续加氨水至 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为_______ 。
(4)向过滤Ⅲ所得滤液中加入 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为_______ 。
(5)为得到纯净的 ,
,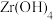 需要洗涤,检验
需要洗涤,检验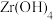 是否洗涤干净的方法是
是否洗涤干净的方法是_______ 。
 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为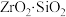 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。
已知:①
 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的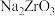 ,
,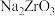 与酸反应生成
与酸反应生成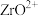 。
。②部分金属离子在实验条件下开始沉淀和完全沉淀的
 如表。
如表。| 金属离子 |  | 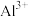 | 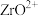 |
开始沉淀时 | 1.9 | 3.3 | 6.2 |
沉淀完全时 | 3.2 | 5.2 | 8.0 |
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ中除
 外还含金属的阳离子有
外还含金属的阳离子有 ,则a的范围是
,则a的范围是(3)继续加氨水至
 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为(4)向过滤Ⅲ所得滤液中加入
 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为(5)为得到纯净的
 ,
,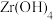 需要洗涤,检验
需要洗涤,检验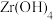 是否洗涤干净的方法是
是否洗涤干净的方法是
您最近半年使用:0次
名校
10 . 下列说法正确的是
A.向氢氟酸溶液中适当加热或加水,均能使溶液中 增大 增大 |
B.室温下,向 悬浊液中加少量水,达到新平衡后 悬浊液中加少量水,达到新平衡后 浓度减小 浓度减小 |
C.100℃时,将 的硫酸与 的硫酸与 的 的 等体积混合后,溶液显中性 等体积混合后,溶液显中性 |
D.为除去 酸性溶液中混有的 酸性溶液中混有的 杂质,可加入 杂质,可加入 溶液充分反应后过滤 溶液充分反应后过滤 |
您最近半年使用:0次



