名校
解题方法
1 . 下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某无色溶液中通入过量的CO2气体,有白色沉淀产生 | 该溶液中一定含有SiO |
| B | 向浓度均为0.1mol·L-1的MgCl2和CuCl2的混合溶液中逐滴加入氨水,先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| C | 在MgSO4溶液中加入一小块Na,金属Na溶解,并生成固体 | 该固体为Mg |
| D | 将浓硫酸滴到蔗糖表面固体变黑膨胀 | 浓硫酸只表现脱水性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-12更新
|
351次组卷
|
2卷引用:四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题
2 . 严谨的实验设计能有效规避实验风险,能重复实验并得到相同的结果。由粗盐制备试剂级的NaCl的相关实验步骤和装置如下:
【粗盐的提纯】
第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。
第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3,过滤,再用3.0mol/L HCl调节pH至1~2。
第III步,加热浓缩至溶液刚刚出现微晶膜。
(1)第I步加入BaCl2时,证明SO 已经除净的实验方法是
已经除净的实验方法是___________ 。
(2)第II步加入Na2CO3可以除去的离子为___________ 。
(3)第III步加热浓缩时所用到的硅酸盐材质的仪器有酒精灯、___________ ;已知:Ksp(BaCO3)=5.0×10-9、Ksp(BaSO4)=1.1×10-10;如果省略第I步“倾析法分离”,所得氯化钠溶液的纯度将___________ (填“升高”、“降低”或“不受影响”)。
【试剂级的NaCl的制备】
第IV步,将第III步浓缩溶液转移至下图装置C中继续实验。
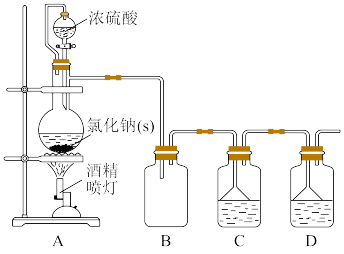
(4)装置A中发生的化学反应方程式为___________ ,控制该反应速率可采取的措施___________ (任答一点即可)。
(5)装置B中的广口瓶和装置C、D中的漏斗,其共同作用是___________ ,装置C的溶液中能观察到的实验现象是___________ 。装置D中盛放的试剂为___________ (填“NaOH溶液”、“NaHSO3溶液”或“浓H2SO4”)。
【粗盐的提纯】
第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。
第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3,过滤,再用3.0mol/L HCl调节pH至1~2。
第III步,加热浓缩至溶液刚刚出现微晶膜。
(1)第I步加入BaCl2时,证明SO
 已经除净的实验方法是
已经除净的实验方法是(2)第II步加入Na2CO3可以除去的离子为
(3)第III步加热浓缩时所用到的硅酸盐材质的仪器有酒精灯、
【试剂级的NaCl的制备】
第IV步,将第III步浓缩溶液转移至下图装置C中继续实验。

(4)装置A中发生的化学反应方程式为
(5)装置B中的广口瓶和装置C、D中的漏斗,其共同作用是
您最近一年使用:0次
2022-03-25更新
|
506次组卷
|
5卷引用:四川省内江市2022届高三下学期第二次模拟考试理科综合化学试题
名校
3 . 化学与社会、生活密切相关。下列说法不正确的是
| A.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
| B.含重金属离子的电镀废液不能随意排放 |
| C.进行胃镜透视时,不能用碳酸钡代替硫酸钡作为钡餐 |
| D.用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠 |
您最近一年使用:0次
名校
解题方法
4 . Zn是一种应用广泛的金属。用闪锌矿(主要成分为ZnS,还含有SiO2和少量FeS、CdS、PbS、砷化合物杂质等)为原料制备金属Zn和ZnSO4·7H2O的流程如图所示:
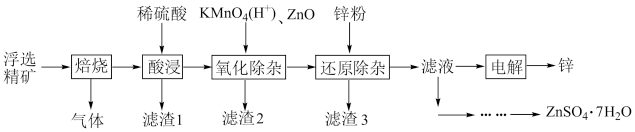
①相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
②FeAsO4难溶于水;ZnSO4·7H2O易溶于水,难溶于酒精。
回答下列问题:
(1)滤渣1的主要成分除SiO2外还有______ ,焙烧后产生的气体对环境造成的常见危害为______ 。
(2)氧化除杂工序中加入ZnO的作用是___________ 。
(3)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用的试剂为____________ 。
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为___________ 。不能省去“还原除杂”步骤,直接在“氧化除杂”步骤中除去Cd2+,理由是________ 。
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为_____________ ;沉积锌后的电解液可返回______ 工序继续使用。
(6)酸浸液中砷元素以AsO 存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,写出该反应的离子方程式为
存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,写出该反应的离子方程式为___________ 。

①相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
②FeAsO4难溶于水;ZnSO4·7H2O易溶于水,难溶于酒精。
回答下列问题:
(1)滤渣1的主要成分除SiO2外还有
(2)氧化除杂工序中加入ZnO的作用是
(3)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用的试剂为
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为
(6)酸浸液中砷元素以AsO
 存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,写出该反应的离子方程式为
存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,写出该反应的离子方程式为
您最近一年使用:0次
2020-02-10更新
|
765次组卷
|
3卷引用:2019年四川省内江市高三上学期第一次模拟考试化学试题
名校
5 . 25℃时,下列有关叙述中不正确的是
| A.pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH<7 |
B.沉淀溶解平衡:BaSO4(s) Ba2+(aq)+SO42-(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质 Ba2+(aq)+SO42-(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质 |
| C.在0.10mol•L﹣1的NH3•H2O溶液中加入少量NH4Cl晶体,则NH3•H2O电离被抑制,溶液pH减少 |
| D.0.1mol • L-1的HA溶液pH=1,该溶液中由水电离的c(OH-)=l×10-13mol·L-1 |
您最近一年使用:0次



