1 . CoCO3可用作选矿剂、催化剂及涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
(1)“酸浸”时需控制温度在40℃左右,原因是___________ 。
(2)“除铝”时发生反应的离子方程式为___________ 。
(3)上述“萃取”过程可表示为 。
。
①下列说法不正确的是___________ 。
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。___________
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因___________ 。
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有___________ 。
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为___________ 。
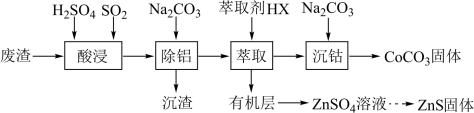
(1)“酸浸”时需控制温度在40℃左右,原因是
(2)“除铝”时发生反应的离子方程式为
(3)上述“萃取”过程可表示为
 。
。①下列说法不正确的是
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为
您最近半年使用:0次
解题方法
2 . 一种废旧磷酸铁锂正极片(主要成分为 、
、 、Al和石墨)的闭环回收工艺流程如图所示:
、Al和石墨)的闭环回收工艺流程如图所示:

已知:① 为抗坏血酸,具有较强的还原性。
为抗坏血酸,具有较强的还原性。
②滤饼成分为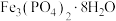 。
。
回答下列问题:
(1)碱溶前,可将废电池正极片进行机械活化处理,使颗粒直径减小,目的是_______ 。
(2)向滤液①中通入过量二氧化碳,可以回收铝,该反应的离子方程式为_______ 。
(3)酸浸过程中加入 的目的是
的目的是_______ 。
(4)将不同pH下得到的滤饼溶于盐酸,稀释至一定比例后测算Fe、P物质的量比 ,结果见下表,由此得出,沉淀的最佳pH为
,结果见下表,由此得出,沉淀的最佳pH为_______ 。
(5)调节pH时,氨水不宜加入过量,原因是随着氨水浓度的增大,会产生_______ 杂质;若该步骤中Fe元素沉淀完全,滤液③中除H、O外,还大量含有的元素有_______ 。
(6)真空管烧结时,加入葡萄糖的作用是_______ 。
 、
、 、Al和石墨)的闭环回收工艺流程如图所示:
、Al和石墨)的闭环回收工艺流程如图所示:
已知:①
 为抗坏血酸,具有较强的还原性。
为抗坏血酸,具有较强的还原性。②滤饼成分为
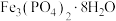 。
。回答下列问题:
(1)碱溶前,可将废电池正极片进行机械活化处理,使颗粒直径减小,目的是
(2)向滤液①中通入过量二氧化碳,可以回收铝,该反应的离子方程式为
(3)酸浸过程中加入
 的目的是
的目的是(4)将不同pH下得到的滤饼溶于盐酸,稀释至一定比例后测算Fe、P物质的量比
 ,结果见下表,由此得出,沉淀的最佳pH为
,结果见下表,由此得出,沉淀的最佳pH为| pH | 6.0 | 6.5 | 7.0 | 8.0 | 9.0 |
 | 1.54 | 1.50 | 1.49 | 1.47 | 1.47 |
(5)调节pH时,氨水不宜加入过量,原因是随着氨水浓度的增大,会产生
(6)真空管烧结时,加入葡萄糖的作用是
您最近半年使用:0次
解题方法
3 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含 、
、 、
、 、
、 、
、 、
、 等元素的氧化物)制备,工艺如图所示。回答下列问题:
等元素的氧化物)制备,工艺如图所示。回答下列问题:

相关金属离子[起始浓度为 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如表:
范围如表:
(1)“滤渣1”含有 和
和___________ 。
(2)“氧化”中添加适量的 的作用是将
的作用是将 氧化为
氧化为 ,写出该反应的离子方程式为
,写出该反应的离子方程式为___________ 。
(3)调 范围为4.7~6,滤渣2成分的化学式为
范围为4.7~6,滤渣2成分的化学式为___________ 。
(4)“除杂1”的目的是除去 和
和 ,“滤渣3”的主要成分是
,“滤渣3”的主要成分是___________ 。
(5)“除杂2”的目的是生成 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是___________ (从沉淀溶解平衡角度解释)。
(6)写出“沉锰”的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 等元素的氧化物)制备,工艺如图所示。回答下列问题:
等元素的氧化物)制备,工艺如图所示。回答下列问题:
相关金属离子[起始浓度为
 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如表:
范围如表:| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有
 和
和(2)“氧化”中添加适量的
 的作用是将
的作用是将 氧化为
氧化为 ,写出该反应的离子方程式为
,写出该反应的离子方程式为(3)调
 范围为4.7~6,滤渣2成分的化学式为
范围为4.7~6,滤渣2成分的化学式为(4)“除杂1”的目的是除去
 和
和 ,“滤渣3”的主要成分是
,“滤渣3”的主要成分是(5)“除杂2”的目的是生成
 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是(6)写出“沉锰”的离子方程式
您最近半年使用:0次
解题方法
4 . 火法炼铜中产生的白烟尘常含ZnO、 、CuO、CdO、
、CuO、CdO、 、PdO等,其中Cu、Zn、Pb、Cd等是潜在的金属资源,As有潜在环境威胁,可综合利用变废为宝,流程如下:
、PdO等,其中Cu、Zn、Pb、Cd等是潜在的金属资源,As有潜在环境威胁,可综合利用变废为宝,流程如下:

(1)溶解度:

 (填“>”“<”或“=”)。在浸出液中,砷元素主要以
(填“>”“<”或“=”)。在浸出液中,砷元素主要以 的形式存在,写出“酸浸”生成
的形式存在,写出“酸浸”生成 的化学方程式
的化学方程式(2)表1和表2是在其他条件一定时,铁铜摩尔置换比[
 ]、温度分别对铜的置换率和品位(矿石中所含某种金属或有用成分的多少)的影响,浸出液置换铜的最佳
]、温度分别对铜的置换率和品位(矿石中所含某种金属或有用成分的多少)的影响,浸出液置换铜的最佳 比值是
比值是表1  对铜置换率和品味的影响
对铜置换率和品味的影响
| 置换率/% | Cu品位/% |
1.2 | 74.87 | 51.22 |
1.4 | 92.17 | 72.82 |
1.6 | 99.92 | 72.08 |
表2温度对铜置换率和品味的影响
温度/℃ | 置换率/% | Cu品位/% |
30 | 99.92 | 72.08 |
60 | 99.93 | 70.34 |
80 | 99.86 | 69.98 |
(3)随着pH增大,沉砷率将
(4)金属活动性顺序为Zn>Cd>Cu,“电解”主要回收到的金属中,首先析出的是
您最近半年使用:0次
5 . 下列反应的离子方程式错误的是
A.用惰性电极电解氯化镁溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
B.硫酸铵溶液显酸性: +H2O +H2O NH3•H2O+H+ NH3•H2O+H+ |
C.二元弱酸亚磷酸(H3PO3)溶液中滴加足量的NaOH溶液:H3PO3+2OH-=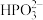 +2H2O +2H2O |
D.硫酸铜溶液遇到难溶的PbS转变为更难溶的CuS:Cu2+(aq)+ (aq)+PbS(s)=CuS(s)+PbSO4(s) (aq)+PbS(s)=CuS(s)+PbSO4(s) |
您最近半年使用:0次
6 . 某温度时, 在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是

 在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.向 溶液中滴加 溶液中滴加 溶液不一定会生成沉淀 溶液不一定会生成沉淀 |
B.该温度下, 的溶度积常数 的溶度积常数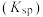 的数量级是 的数量级是 |
| C.可以通过改变温度或加入硫酸银固体使a点移动到b点 |
D.含有大量 的溶液中肯定不存在 的溶液中肯定不存在 |
您最近半年使用:0次
7 . 下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某无色溶液中通入过量的 气体,产生白色沉淀 气体,产生白色沉淀 | 该溶液中一定含有 |
| B | 向浓度均为 的 的 和 和 的混合溶液中逐滴加入等浓度的 的混合溶液中逐滴加入等浓度的 溶液,先出现淡黄色沉淀 溶液,先出现淡黄色沉淀 |  |
| C | 在 溶液中加入一小块 溶液中加入一小块 ,金属 ,金属 溶解,并生成大量固体 溶解,并生成大量固体 | 该固体为 |
| D | 将浓硫酸滴到蔗糖表面,固体变黑膨胀 | 浓硫酸只表现脱水性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 常温时, 的溶度积
的溶度积 ,
, 在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是
在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是


 的溶度积
的溶度积 ,
, 在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是
在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是

A.常温时, 在 在 溶液中的 溶液中的 比在水中的小 比在水中的小 |
B.常温时, 的溶度积 的溶度积 |
C.向含等浓度 、 、 的混合溶液中滴加 的混合溶液中滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
D.向Y点溶液中加入 溶液,可使Y点移到Z点 溶液,可使Y点移到Z点 |
您最近半年使用:0次
名校
解题方法
9 . 下列有关AgCl的沉淀溶解平衡的说法中,正确的是
| A.AgCl的生成和溶解不断进行,但速率相等 |
B.AgCl难溶于水,溶液中没有 和 和 |
| C.升高温度,AgCl的溶解度不变 |
| D.向AgCl的沉淀溶解平衡体系中加入NaCl固体,AgCl溶解的量不变 |
您最近半年使用:0次
2024-02-08更新
|
84次组卷
|
14卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题
四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题(已下线)2019年11月11日《每日一题》人教版(选修4)—— 沉淀溶解平衡的理解福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)第四节 沉淀溶解平衡 第1课时 难溶电解质的沉淀溶解平衡天津市河北区2022-2023学年高二上学期期末考试化学试题黑龙江省哈尔滨市德强学校2022-2023学年高二上学期期末考试化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)3.4.1沉淀溶解平衡原理 课前(已下线)专题07 沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第二次月考化学试题天津北京师范大学静海附属学校2023-2024学年高二上学期第三次月考化学试题
名校
10 . 下列实验对应的反应方程式书写正确的是
A.泡沫灭火器原理:2Al3++3 +3H2O=2Al(OH)3 ↓+ 3CO2↑ +3H2O=2Al(OH)3 ↓+ 3CO2↑ |
B.FeS除去废水中的Hg2+:FeS(s) + Hg2+(aq)  Fe2+(aq) + HgS(s) Fe2+(aq) + HgS(s) |
C.用铁电极电解饱和食盐水:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
D.Fe2(SO4)3溶液中加入足量Ba(OH)2溶液:Fe3++ +Ba2++3OH-=Fe(OH)3↓+BaSO4↓ +Ba2++3OH-=Fe(OH)3↓+BaSO4↓ |
您最近半年使用:0次
2024-02-07更新
|
226次组卷
|
3卷引用:四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷



