名校
解题方法
1 . 碳酸锌在工业上用途广泛。利用某种浸锌渣(主要含有 )制备
)制备 的一种流程如下:
的一种流程如下: ;
;
②室温下,部分离子浓度的对数 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体 中主要成分是
中主要成分是______ (填化学式)。
(2)“碱浸”后,浸出液中含有金属元素的离子主要是 和
和______ (填离子符号);欲使浸出液中的含锌微粒完全沉淀,应调节 的范围是
的范围是______ 。
(3)浸渣回收银的过程中有配合物 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为______ 。
(4)“除杂”时滤渣的主要成分是______ (填化学式)。
(5)“沉锌”时发生反应的离子方程式为______ ;此过程不宜用碳酸钠代替碳酸氢铵,原因是______ 。
 )制备
)制备 的一种流程如下:
的一种流程如下: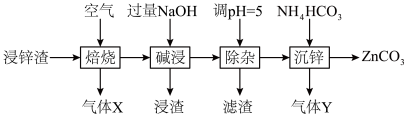
 ;
;②室温下,部分离子浓度的对数
 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):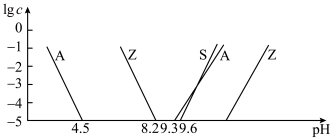
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体
 中主要成分是
中主要成分是(2)“碱浸”后,浸出液中含有金属元素的离子主要是
 和
和 的范围是
的范围是(3)浸渣回收银的过程中有配合物
 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为(4)“除杂”时滤渣的主要成分是
(5)“沉锌”时发生反应的离子方程式为
您最近一年使用:0次
昨日更新
|
158次组卷
|
2卷引用:2024届四川省射洪中学校高三下学期二模理综试题-高中化学
2 .  是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含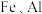 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下: )时的
)时的 如下表:
如下表:
② 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。
(1)“酸浸”时提高浸取率的措施有___________ (写出两条)。
(2)滤渣I的主要成分是___________ (填化学式)。
(3)操作 为调节溶液的
为调节溶液的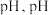 的最佳范围是
的最佳范围是___________ ,加入的物质X可以是___________ ( (填字母标号)。
A. B.
B.  C.
C.  D.
D.  溶液
溶液
(4)往滤液 中加入食盐并通入
中加入食盐并通入 可生成
可生成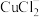 ,反应I的离子方程式为
,反应I的离子方程式为___________ ;在反应I中加入食盐并加热的目的是___________ 。
(5)实验室可以使用铜电极电解饱和食盐水得到 ,阳极的电极反应式为
,阳极的电极反应式为___________ 。
 是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含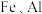 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下:
 )时的
)时的 如下表:
如下表:| 物质 |  |  |  |
开始沉淀时的 | 1.6 | 3.2 | 5.2 |
完全沉淀时的 | 3.1 | 4.7 | 6.7 |
 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。(1)“酸浸”时提高浸取率的措施有
(2)滤渣I的主要成分是
(3)操作
 为调节溶液的
为调节溶液的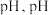 的最佳范围是
的最佳范围是A.
 B.
B.  C.
C.  D.
D.  溶液
溶液(4)往滤液
 中加入食盐并通入
中加入食盐并通入 可生成
可生成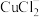 ,反应I的离子方程式为
,反应I的离子方程式为(5)实验室可以使用铜电极电解饱和食盐水得到
 ,阳极的电极反应式为
,阳极的电极反应式为
您最近一年使用:0次
解题方法
3 . 一种废旧磷酸铁锂正极片(主要成分为 、
、 、Al和石墨)的闭环回收工艺流程如图所示:
、Al和石墨)的闭环回收工艺流程如图所示:

已知:① 为抗坏血酸,具有较强的还原性。
为抗坏血酸,具有较强的还原性。
②滤饼成分为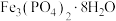 。
。
回答下列问题:
(1)碱溶前,可将废电池正极片进行机械活化处理,使颗粒直径减小,目的是_______ 。
(2)向滤液①中通入过量二氧化碳,可以回收铝,该反应的离子方程式为_______ 。
(3)酸浸过程中加入 的目的是
的目的是_______ 。
(4)将不同pH下得到的滤饼溶于盐酸,稀释至一定比例后测算Fe、P物质的量比 ,结果见下表,由此得出,沉淀的最佳pH为
,结果见下表,由此得出,沉淀的最佳pH为_______ 。
(5)调节pH时,氨水不宜加入过量,原因是随着氨水浓度的增大,会产生_______ 杂质;若该步骤中Fe元素沉淀完全,滤液③中除H、O外,还大量含有的元素有_______ 。
(6)真空管烧结时,加入葡萄糖的作用是_______ 。
 、
、 、Al和石墨)的闭环回收工艺流程如图所示:
、Al和石墨)的闭环回收工艺流程如图所示:
已知:①
 为抗坏血酸,具有较强的还原性。
为抗坏血酸,具有较强的还原性。②滤饼成分为
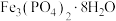 。
。回答下列问题:
(1)碱溶前,可将废电池正极片进行机械活化处理,使颗粒直径减小,目的是
(2)向滤液①中通入过量二氧化碳,可以回收铝,该反应的离子方程式为
(3)酸浸过程中加入
 的目的是
的目的是(4)将不同pH下得到的滤饼溶于盐酸,稀释至一定比例后测算Fe、P物质的量比
 ,结果见下表,由此得出,沉淀的最佳pH为
,结果见下表,由此得出,沉淀的最佳pH为| pH | 6.0 | 6.5 | 7.0 | 8.0 | 9.0 |
 | 1.54 | 1.50 | 1.49 | 1.47 | 1.47 |
(5)调节pH时,氨水不宜加入过量,原因是随着氨水浓度的增大,会产生
(6)真空管烧结时,加入葡萄糖的作用是
您最近一年使用:0次
解题方法
4 . 火法炼铜中产生的白烟尘常含ZnO、 、CuO、CdO、
、CuO、CdO、 、PdO等,其中Cu、Zn、Pb、Cd等是潜在的金属资源,As有潜在环境威胁,可综合利用变废为宝,流程如下:
、PdO等,其中Cu、Zn、Pb、Cd等是潜在的金属资源,As有潜在环境威胁,可综合利用变废为宝,流程如下:

(1)溶解度:

 (填“>”“<”或“=”)。在浸出液中,砷元素主要以
(填“>”“<”或“=”)。在浸出液中,砷元素主要以 的形式存在,写出“酸浸”生成
的形式存在,写出“酸浸”生成 的化学方程式
的化学方程式(2)表1和表2是在其他条件一定时,铁铜摩尔置换比[
 ]、温度分别对铜的置换率和品位(矿石中所含某种金属或有用成分的多少)的影响,浸出液置换铜的最佳
]、温度分别对铜的置换率和品位(矿石中所含某种金属或有用成分的多少)的影响,浸出液置换铜的最佳 比值是
比值是表1  对铜置换率和品味的影响
对铜置换率和品味的影响
| 置换率/% | Cu品位/% |
1.2 | 74.87 | 51.22 |
1.4 | 92.17 | 72.82 |
1.6 | 99.92 | 72.08 |
表2温度对铜置换率和品味的影响
温度/℃ | 置换率/% | Cu品位/% |
30 | 99.92 | 72.08 |
60 | 99.93 | 70.34 |
80 | 99.86 | 69.98 |
(3)随着pH增大,沉砷率将
(4)金属活动性顺序为Zn>Cd>Cu,“电解”主要回收到的金属中,首先析出的是
您最近一年使用:0次
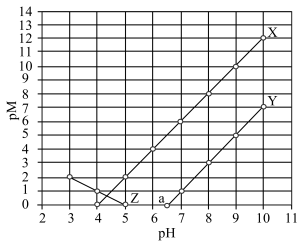
5 . 常温下,向 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如图所示。知:
的关系如图所示。知: 代表
代表 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述错误的是
时,认为该离子已沉淀完全。下列叙述错误的是
 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如图所示。知:
的关系如图所示。知: 代表
代表 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述错误的是
时,认为该离子已沉淀完全。下列叙述错误的是
A.X、Z分别代表 与 与 的关系 的关系 |
B.常温下,弱酸 的电离常数 的电离常数 |
C.图中 点对应溶液的 点对应溶液的 为6.5,此时溶液中 为6.5,此时溶液中 |
D.向浓度均为 的 的 和 和 的混合溶液中逐滴加入 的混合溶液中逐滴加入 溶液,能通过沉淀的方式将两种离子分离 溶液,能通过沉淀的方式将两种离子分离 |
您最近一年使用:0次
23-24高三上·黑龙江·期中
名校
解题方法
6 . 氧化钴(Co2O3)常用作超耐热合金和磁性材料及化学工业的催化剂。一种以钴矿渣(含有Co、Fe、Ca、Mg、Mn、Ni等元素的化合物及 )制备
)制备 的工艺流程如下。
的工艺流程如下。

已知:①钴矿渣浸出后溶液中金属元素以+2价离子形式存在。
② 、
、 可溶于水。
可溶于水。
回答下列问题:
(1)“浸出”时,为了加快浸出速率,可采取的措施有___________ (任写两点);滤渣1的主要成分为___________ (填化学式)。
(2)“除铁”过程中, 参与反应的离子方程式为
参与反应的离子方程式为___________ 。
(3)“萃取”“反萃取”步骤的目的是___________ ;“煅烧”时主要反应的化学方程式为___________ 。
(4)以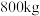 钴矿渣(Co的质量分数为12.5%)为原料提取出
钴矿渣(Co的质量分数为12.5%)为原料提取出 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为___________ (计算结果保留三位有效数字)。
 )制备
)制备 的工艺流程如下。
的工艺流程如下。
已知:①钴矿渣浸出后溶液中金属元素以+2价离子形式存在。
②
 、
、 可溶于水。
可溶于水。回答下列问题:
(1)“浸出”时,为了加快浸出速率,可采取的措施有
(2)“除铁”过程中,
 参与反应的离子方程式为
参与反应的离子方程式为(3)“萃取”“反萃取”步骤的目的是
(4)以
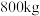 钴矿渣(Co的质量分数为12.5%)为原料提取出
钴矿渣(Co的质量分数为12.5%)为原料提取出 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为
您最近一年使用:0次
名校
7 . 由软锰矿(主要成分是MnO2,还含有Al2O3、MgO、SiO2等杂质)制备高纯碳酸锰、硫酸锰的一种工艺流程如图所示。
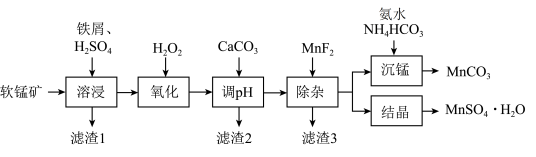
已知:①25℃时,Ksp(MnCO3)=1.8 10-11,Ksp(CaF2)=1.5
10-11,Ksp(CaF2)=1.5 10-10,Ksp(MgF2)=7.4
10-10,Ksp(MgF2)=7.4 10-11。
10-11。
②一定条件下,一些金属氢氧化物沉淀时的pH如表所示。
回答下列问题:
(1)除去铁屑表面油污,可采用的方法是___________ 。
(2)已知“溶浸”时,Fe不能还原MnO2,但Fe2+能还原MnO2得到Mn2+。Fe2+还原MnO2的离子方程式是___________ 。
(3)“氧化”时,过氧化氢的实际消耗量远大于理论消耗量,其原因可能是___________ 。
(4)用CaCO3 “调pH”虽然成本较低,但会引入Ca2+等杂质,若使用___________ (填化学式) “调pH”可避免此问题;调节pH步骤中,应控制的pH范围是___________ 。
(5)滤渣3的主要成分是___________ (填化学式)。
(6)“沉锰”时发生反应的离子方程式为___________ 。
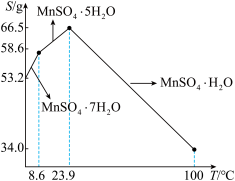
(7)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。“结晶”是从“除杂”后过滤所得的滤液中获得MnSO4·H2O。其操作是___________ ,___________ ,洗涤,真空干燥。

已知:①25℃时,Ksp(MnCO3)=1.8
 10-11,Ksp(CaF2)=1.5
10-11,Ksp(CaF2)=1.5 10-10,Ksp(MgF2)=7.4
10-10,Ksp(MgF2)=7.4 10-11。
10-11。②一定条件下,一些金属氢氧化物沉淀时的pH如表所示。
| 金属氢氧化物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 6.8 | 2.3 | 8.1 | 3.4 |
| 完全沉淀的pH | 8.3 | 3.2 | 10 | 4.7 |
(1)除去铁屑表面油污,可采用的方法是
(2)已知“溶浸”时,Fe不能还原MnO2,但Fe2+能还原MnO2得到Mn2+。Fe2+还原MnO2的离子方程式是
(3)“氧化”时,过氧化氢的实际消耗量远大于理论消耗量,其原因可能是
(4)用CaCO3 “调pH”虽然成本较低,但会引入Ca2+等杂质,若使用
(5)滤渣3的主要成分是
(6)“沉锰”时发生反应的离子方程式为
(7)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。“结晶”是从“除杂”后过滤所得的滤液中获得MnSO4·H2O。其操作是

您最近一年使用:0次
2023-11-05更新
|
300次组卷
|
2卷引用:四川省成都市实验外国语学校2023-2024学年高三上学期10月检测理综化学试题
解题方法
8 . 七水合硫酸镁(MgSO4•7H2O)在印染、造纸等领域应用广泛。以化工废弃物盐泥(主要成分为MgCO3•CaCO3,含少量NaCl与含铁化合物)为原料可制取七水合硫酸镁,回答下列问题:
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加3.0mol•L-1H2SO4溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为________ ;配制3.0mol•L-1H2SO4溶液时,用到的实验仪器除烧杯、玻璃棒、量筒外,还必须使用的仪器有________ (填标号)。
A. B.
B.  C.
C.  D.
D.
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,继续加热煮沸,趁热过滤,滤渣的主要成分是________ 、________ ,继续加热煮沸的目的是________ 。
(3)要证明铁元素已除尽,实验操作及现象是:________ 。
(4)向(2)所得滤液中加入6mol•L-1NaOH溶液至沉淀完全,过滤,该操作的目的是________ ,将滤渣完全溶于3.0mol•L-1H2SO4溶液,经如下实验操作:加热蒸发、________ 、过滤、洗涤、干燥,得到七水合硫酸镁。
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中MgCO3•CaCO3的含量为________ %,将产品加热至77℃,测得固体失重率为43.9%,该温度下固体的化学式为________ 。
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加3.0mol•L-1H2SO4溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为
A.
 B.
B.  C.
C.  D.
D.
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,继续加热煮沸,趁热过滤,滤渣的主要成分是
(3)要证明铁元素已除尽,实验操作及现象是:
(4)向(2)所得滤液中加入6mol•L-1NaOH溶液至沉淀完全,过滤,该操作的目的是
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中MgCO3•CaCO3的含量为
您最近一年使用:0次
名校
9 . 草酸镍晶体( )可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
)可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:

已知:
①相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为 计算):
计算):
② ,
,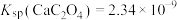 。
。
回答下列问题:
(1)基态镍原子的价层电子排布式为___________ 。
(2)试剂X可以是___________ ,
(3)调节pH的范围是___________ 。
(4)滤渣1的成分是___________ (写化学式),加入适量NH4F溶液的目的是___________ 。
(5)“沉镍”的离子方程式为___________ 。
(6)称取一定质量某镀镍试剂,配成100mL溶液,溶液中存在的离子为 、
、 、
、 ;准确量取10.00mL溶液,用
;准确量取10.00mL溶液,用 的EDTA标准溶液滴定其中的
的EDTA标准溶液滴定其中的 ,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
①配制EDTA标准溶液需要注意蒸馏水的水质,水中若含 、
、 会使滴定时消耗的EDTA的体积
会使滴定时消耗的EDTA的体积___________ (填“偏大”“不变”或“偏小”)。
②该镀镍试剂中 的物质的量浓度为
的物质的量浓度为___________ mol/L。
 )可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
)可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
已知:
①相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为
 计算):
计算):| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 1.1 | 3.2 |
 | 5.8 | 8.8 |
 | 3.0 | 5.0 |
 | 6.7 | 9.5 |
 ,
,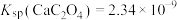 。
。回答下列问题:
(1)基态镍原子的价层电子排布式为
(2)试剂X可以是
(3)调节pH的范围是
(4)滤渣1的成分是
(5)“沉镍”的离子方程式为
(6)称取一定质量某镀镍试剂,配成100mL溶液,溶液中存在的离子为
 、
、 、
、 ;准确量取10.00mL溶液,用
;准确量取10.00mL溶液,用 的EDTA标准溶液滴定其中的
的EDTA标准溶液滴定其中的 ,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。①配制EDTA标准溶液需要注意蒸馏水的水质,水中若含
 、
、 会使滴定时消耗的EDTA的体积
会使滴定时消耗的EDTA的体积②该镀镍试剂中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
10 . 铟(In)是一种稀散金属,常与其他金属矿石伴生,回收氧化锌烟尘(主要成分是ZnO,还含少量PbO、FeS、FeSiO3、 In2O3、 In2S3等)中的金属铟的工艺流程如下:
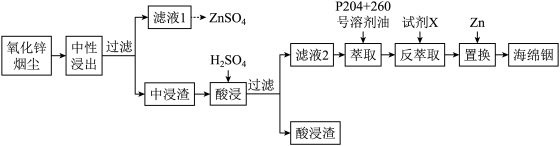
已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)In2O3中In的化合价是_______________________ 。
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为____________________________________________ 。
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为 ,该反应的离子方程式为
,该反应的离子方程式为____________________ 。
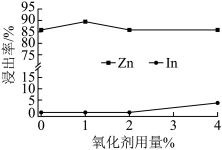
③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为_________________ 。
④“中浸渣”的主要成分为In(OH)3、________________ 。 (写化学式)
(3)萃取时,发生反应In3+ +3H2A2 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。
①反萃取时,宜选用的试剂X为_____________________ (写化学式)
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有_________________________ 。
(4)“置换”后的滤液可返回________________________ (填“滤液 1”或“滤液2”)中利用。
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉___ _kg (结果保留1位小数)

已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子 | Fe3+ | Fe2+ | In3+ |
开始沉淀pH(离子浓度为0.1mol·L-1时) | 1.3 | 6 | 3 |
完全沉淀pH | 2.7 | 8 | 4.3 |
(1)In2O3中In的化合价是
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为

④“中浸渣”的主要成分为In(OH)3、
(3)萃取时,发生反应In3+ +3H2A2
 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。①反萃取时,宜选用的试剂X为
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有
(4)“置换”后的滤液可返回
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉
您最近一年使用:0次



