名校
1 . 过氧化钙是一种比较稳定的金属过氧化物,它的氧化反应缓和,安全无毒,可用于环保、食品及化学工业。利用大理石制过氧化钙的实验步骤如下:
一、制取纯的
①称取5g大理石,溶于 硝酸溶液中,充分反应后,将溶液加热至沸腾;
硝酸溶液中,充分反应后,将溶液加热至沸腾;
②在①溶液中加50mL水稀释,加氨水调节溶液至弱碱性后再煮沸,趁热过滤,弃去沉淀;
③在②滤液中加入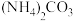 溶液,搅拌后静置,减压过滤,洗涤,干燥得到
溶液,搅拌后静置,减压过滤,洗涤,干燥得到 固体。
固体。
二、制取
④将新制的 置于烧杯中,逐滴加入
置于烧杯中,逐滴加入 盐酸,直到剩余极少量
盐酸,直到剩余极少量 固体为止,将溶液煮沸,趁热过滤,保留滤液;
固体为止,将溶液煮沸,趁热过滤,保留滤液;
⑤另取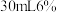
 溶液,与
溶液,与 氨水混合,制得
氨水混合,制得 溶液;
溶液;
⑥将④、⑤中的溶液置于冰水中冷却后,再混合,并将混合液置于冰水中放置30min;
⑦减压过滤,洗涤,干燥,得到 晶体。
晶体。
回答下列问题
(1)①中配置 硝酸溶液,需要用量筒量取
硝酸溶液,需要用量筒量取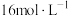 浓硝酸
浓硝酸___________ mL。
(2)下列仪器中,属于②中“趁热过滤”所需的仪器是___________ 。过滤时,“趁热”的目的是___________ ,大理石中常含有Fe、Al等杂质元素,则沉淀的主要成分是___________ (填化学式)。缺少步骤②,对后续实验造成的影响是___________ 。

(3)⑥中发生反应的化学方程式是___________ ,氨水的作用是___________ 。
(4)⑦中“减压过滤”的优点是___________ ,产品可用___________ 洗涤。
(5)对产品 (相对分子质量为216)进行热重分析,得到数据如图。400℃时,得到的产品的化学式是
(相对分子质量为216)进行热重分析,得到数据如图。400℃时,得到的产品的化学式是___________ 。

一、制取纯的

①称取5g大理石,溶于
 硝酸溶液中,充分反应后,将溶液加热至沸腾;
硝酸溶液中,充分反应后,将溶液加热至沸腾;②在①溶液中加50mL水稀释,加氨水调节溶液至弱碱性后再煮沸,趁热过滤,弃去沉淀;
③在②滤液中加入
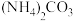 溶液,搅拌后静置,减压过滤,洗涤,干燥得到
溶液,搅拌后静置,减压过滤,洗涤,干燥得到 固体。
固体。二、制取

④将新制的
 置于烧杯中,逐滴加入
置于烧杯中,逐滴加入 盐酸,直到剩余极少量
盐酸,直到剩余极少量 固体为止,将溶液煮沸,趁热过滤,保留滤液;
固体为止,将溶液煮沸,趁热过滤,保留滤液;⑤另取
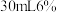
 溶液,与
溶液,与 氨水混合,制得
氨水混合,制得 溶液;
溶液;⑥将④、⑤中的溶液置于冰水中冷却后,再混合,并将混合液置于冰水中放置30min;
⑦减压过滤,洗涤,干燥,得到
 晶体。
晶体。回答下列问题
(1)①中配置
 硝酸溶液,需要用量筒量取
硝酸溶液,需要用量筒量取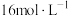 浓硝酸
浓硝酸(2)下列仪器中,属于②中“趁热过滤”所需的仪器是

(3)⑥中发生反应的化学方程式是
(4)⑦中“减压过滤”的优点是
(5)对产品
 (相对分子质量为216)进行热重分析,得到数据如图。400℃时,得到的产品的化学式是
(相对分子质量为216)进行热重分析,得到数据如图。400℃时,得到的产品的化学式是
您最近一年使用:0次
2023-08-15更新
|
265次组卷
|
2卷引用:新疆乌鲁木齐市等3地2022-2023学年高三上学期第一次联考(一模)化学试题
解题方法
2 . 常温下,CaCO3和CaF2的沉淀溶解平衡曲线如图[ pX=-lgc(Xn-)、pCa=-lgc( Ca2+)],已知Ksp( CaCO3)>Ksp( CaF2),下列说法正确的是
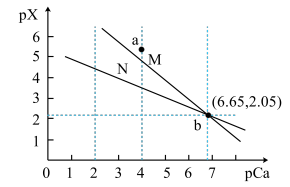

| A.曲线M为CaF2的沉淀溶解平衡曲线 |
B.常温下,CaCO3(s) +2F-(aq)  CaF2(s) + CaF2(s) +  (aq)的化学平衡常数K= 10-2.05 (aq)的化学平衡常数K= 10-2.05 |
C.在CaCl2溶液中加碳酸钠溶液,当溶液中c( )的浓度大于1. 0 ×10-3时,可以确定Ca2+沉淀完全 )的浓度大于1. 0 ×10-3时,可以确定Ca2+沉淀完全 |
| D.a点为悬浊液,过滤可得固体 |
您最近一年使用:0次
解题方法
3 . 锌是一种应用广泛的金属。一种以闪锌矿(主要成分为ZnS,还含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
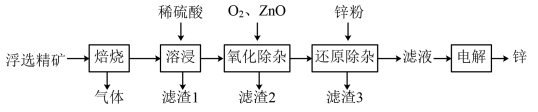
相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为____ 。
(2)滤渣1的主要成分除SiO2外还有____ 。
(3)氧化除杂工序中通入氧气的作用是____ ,ZnO的作用是____ 。
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为____ 。为什么不能省去“还原除杂”步骤,直接在“氧化除杂”步骤中除去Cd2+____ 。
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为____ ;沉积锌后的电解液可返回___ 工序继续使用。
(6)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,“氧压酸浸”中发生的主要反应的离子方程式为____ 。

相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中主要反应的化学方程式为
(2)滤渣1的主要成分除SiO2外还有
(3)氧化除杂工序中通入氧气的作用是
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为
(6)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,“氧压酸浸”中发生的主要反应的离子方程式为
您最近一年使用:0次
4 . 工业上应用两矿法漫出软锰矿(主要成分MnO2)和方铅矿(主要成分PbS、FeS2)制备PbSO4和Mn3O4转化流程如图:
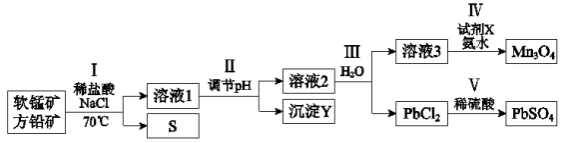
已知:PbCl2微溶于水,溶液中存在可逆反应:PbCl2+2Cl-
 。下列说法正确的是
。下列说法正确的是

已知:PbCl2微溶于水,溶液中存在可逆反应:PbCl2+2Cl-

 。下列说法正确的是
。下列说法正确的是| A.I中可使用浓盐酸代替稀盐酸和NaCl的混合溶液 |
| B.II中生成的沉淀Y是Fe(OH)3 |
| C.IV中试剂X可能作氧化剂 |
D.V中发生反应:Pb2++ = PbSO4 = PbSO4 |
您最近一年使用:0次
2021-05-21更新
|
743次组卷
|
11卷引用:新疆吾尔自治区乌鲁木齐市第七十中学2021届高三上学期第一次月考(9月)化学试题
新疆吾尔自治区乌鲁木齐市第七十中学2021届高三上学期第一次月考(9月)化学试题北京市西城区2020届高三第二次模拟化学试题北京市首都师范大学附属中学2021届高三上学期开学(线上)考试化学试题安徽省安庆市怀宁县怀宁中学2021届高三年级第一次质量检测化学试题重庆市第二十九中学2021届高三上学期10月月考化学试题(已下线)【浙江新东方】高中化学20210513-044【2021】【高二下】河南省南阳市第一中学校2022届高三上学期第四次月考化学试题山东省济南外国语学校(三箭分校)2021-2022学年高三上学期模拟考试化学试题河南省示范性高中2021-2022学年高三上学期阶段性调研联考二化学试题北京一零一中学2021-2022学年高三下学期入学考试化学试题山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题
名校
解题方法
5 . 25℃时,用Na2S沉淀Cu2+、Zn2+两种金属阳离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法不正确的是( )
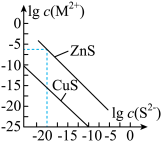

| A.向Cu2+浓度为1×10-5mol·L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
| B.25℃时,Ksp(CuS)约为1×10-35 |
| C.向100mLZn2+、Cu2+浓度均为1×10-5 mol·L-1的混合溶液中逐滴加入1×10-4mol·L-1的Na2S溶液,Cu2+先沉淀 |
| D.Na2S溶液中:c(H+)+c(HS-)+c(H2S)=c(OH-) |
您最近一年使用:0次
6 . 当氢氧化镁固体在水中达到溶解平衡 Mg(OH)2(s) Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
 Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的| A.NH3 ·H2O | B.NaOH | C.MgSO4 | D.NaHSO4 |
您最近一年使用:0次
2017-07-24更新
|
258次组卷
|
2卷引用:新疆昌吉州教育共同体2020-2021学年高二上学期期末质量检测化学试题



