名校
解题方法
1 .  常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为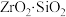 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。

已知:① 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的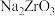 ,
,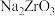 与酸反应生成
与酸反应生成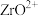 。
。
②部分金属离子在实验条件下开始沉淀和完全沉淀的 如表。
如表。
(1)熔融时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,滤渣Ⅰ的化学式为_______ 。
(2)滤液Ⅰ中除 外还含金属的阳离子有
外还含金属的阳离子有_______ ,为使滤液Ⅰ的杂质离子沉淀完全,需用氨水调 ,则a的范围是
,则a的范围是_______ 。
(3)继续加氨水至 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为_______ 。
(4)向过滤Ⅲ所得滤液中加入 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为_______ 。
(5)为得到纯净的 ,
,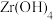 需要洗涤,检验
需要洗涤,检验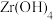 是否洗涤干净的方法是
是否洗涤干净的方法是_______ 。
 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为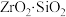 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。
已知:①
 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的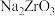 ,
,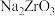 与酸反应生成
与酸反应生成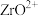 。
。②部分金属离子在实验条件下开始沉淀和完全沉淀的
 如表。
如表。| 金属离子 |  | 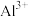 | 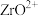 |
开始沉淀时 | 1.9 | 3.3 | 6.2 |
沉淀完全时 | 3.2 | 5.2 | 8.0 |
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ中除
 外还含金属的阳离子有
外还含金属的阳离子有 ,则a的范围是
,则a的范围是(3)继续加氨水至
 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为(4)向过滤Ⅲ所得滤液中加入
 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为(5)为得到纯净的
 ,
,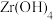 需要洗涤,检验
需要洗涤,检验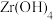 是否洗涤干净的方法是
是否洗涤干净的方法是
您最近一年使用:0次
2 . 次磷酸钠(NaH2PO2)可用于化学镀银、镍、铬等,工业上以泥磷(主要含有P4和少量CaO、Fe2O3、Al2O3、CaCl2等)为原料制备NaH2PO2·H2O的流程如下图所示:
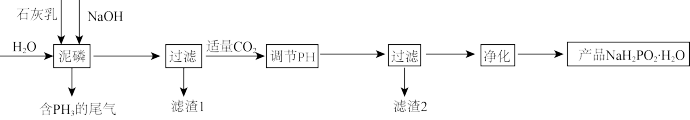
已知:(1)P4与碱反应生成相应的次磷酸盐和PH3;(2)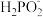 具有极强的还原性。
具有极强的还原性。
回答下列问题:
(1)已知次磷酸(H3PO2)为一元酸,则NaH2PO2是_______ (填“正盐”或“酸式盐”)。
(2)写出P4与NaOH溶液反应的化学方程式_______ 。
(3)尾气中的PH3可被NaClO氧化为NaH2PO2,氧化1mol PH3需要NaClO_______ g。
(4)滤渣1主要含有_______ ;通入CO2调节pH后会得到两种沉淀,分别是_______ ,写出生成其中一种沉淀的离子反应方程式_______ 。
(5)净化时加入Ag2SO4溶液等用以除去其中的Cl-,原理是_______ ,加入Ag2SO4过多会使产率降低,原因是_______ 。

已知:(1)P4与碱反应生成相应的次磷酸盐和PH3;(2)
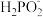 具有极强的还原性。
具有极强的还原性。回答下列问题:
(1)已知次磷酸(H3PO2)为一元酸,则NaH2PO2是
(2)写出P4与NaOH溶液反应的化学方程式
(3)尾气中的PH3可被NaClO氧化为NaH2PO2,氧化1mol PH3需要NaClO
(4)滤渣1主要含有
(5)净化时加入Ag2SO4溶液等用以除去其中的Cl-,原理是
您最近一年使用:0次
解题方法
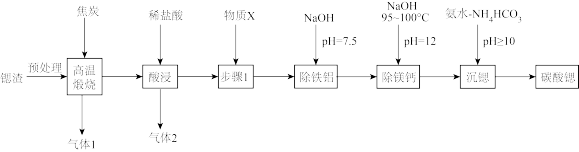
3 . 碳酸锶是重要的无机化工产品。利用锶渣(主要成分SrSO4,含少量CaCO3、Fe2O3、Al2O3、MgCO3杂质)制备超细碳酸锶的工艺如图:
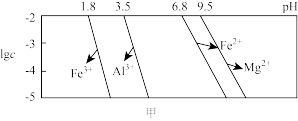
已知:25℃时溶液中金属离子物质的量浓度c与pH的关系如图甲所示:
回答下列问题:
(1)原料预处理的目的是加快煅烧反应速率,提高原料利用率。预处理方式可以是____ 。
(2)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为____ 。
(3)气体2为____ 。步骤1的目的为____ ,不设置步骤1带来的后果是____ 。
(4)“除铁铝”过程维持温度在75℃的好处是____ 。“除铁铝”后溶液温度降至室温(25℃),溶液中c(Fe3+)为____ mol/L。(100.9=7.9)
(5)①写出“沉锶”的离子反应方程式:____ 。
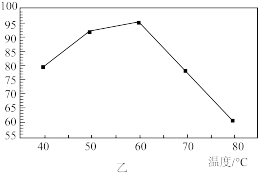
②反应温度对锶转化率的影响如图乙,温度高于60℃时,锶转化率降低的原因为____ 。

已知:25℃时溶液中金属离子物质的量浓度c与pH的关系如图甲所示:

回答下列问题:
(1)原料预处理的目的是加快煅烧反应速率,提高原料利用率。预处理方式可以是
(2)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为
(3)气体2为
(4)“除铁铝”过程维持温度在75℃的好处是
(5)①写出“沉锶”的离子反应方程式:
②反应温度对锶转化率的影响如图乙,温度高于60℃时,锶转化率降低的原因为

您最近一年使用:0次
4 . 兰尼镍(Raney-Ni)是一种带有多孔结构的细小晶粒组成的镍铝合金,常用作烯烃、炔烃等氢化反应催化剂,其高催化活性源自于镍本身的催化性质和其多孔结构对氢气的强吸附性。由镍矿渣(主要含Ni(OH)2、NiS,还含铁、铜、钙、镁化合物及其他不溶性杂质)制备兰尼镍的过程可表示如下:

已知:①Ksp(NiS)=1.07×10-21,Ksp(CuS)=1.27×10-26
②室温下,金属离子的沉淀pH范围如表:
(1)“酸溶”前将镍矿渣粉碎的目的是_______ 。
(2)“酸溶”过程中,NiS发生反应的离子方程式为_______ 。
(3)“除杂”过程分步进行,除铁时所调pH范围为_______ ,除铜时加入NiS发生的反应:NiS(s)+Cu2+(aq)=CuS(s)+Ni2+(aq),该反应的平衡常数K=_______ (保留三位有效数字)。
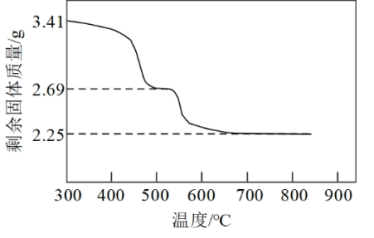
(4)“沉镍”所得沉淀有多种组成,可表示为xNiCO3•yNi(OH)2•zH2O。为测定其组成,进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~700℃条件下收集到的气体产物只有一种,700℃以上残留固体为NiO)。通过计算确定该样品的化学式为_______ 。
(5)“浸出”是制备兰尼镍的关键步骤,NaOH溶液在“浸出”过程中的作用是_______ 。
(6)使用新制兰尼镍进行催化加氢反应,有时不需通入氢气也能发生氢化反应,原因是_____ 。

已知:①Ksp(NiS)=1.07×10-21,Ksp(CuS)=1.27×10-26
②室温下,金属离子的沉淀pH范围如表:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 7.5 | 9.0 |
| Fe3+ | 2.2 | 3.2 |
| Ni2+ | 7.2 | 8.7 |
| Cu2+ | 5.6 | 6.7 |
| Mg2+ | 9.4 | 12.4 |
(2)“酸溶”过程中,NiS发生反应的离子方程式为
(3)“除杂”过程分步进行,除铁时所调pH范围为
(4)“沉镍”所得沉淀有多种组成,可表示为xNiCO3•yNi(OH)2•zH2O。为测定其组成,进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~700℃条件下收集到的气体产物只有一种,700℃以上残留固体为NiO)。通过计算确定该样品的化学式为

(5)“浸出”是制备兰尼镍的关键步骤,NaOH溶液在“浸出”过程中的作用是
(6)使用新制兰尼镍进行催化加氢反应,有时不需通入氢气也能发生氢化反应,原因是
您最近一年使用:0次
名校
解题方法
5 . 制备锂离子电池的正极材料的前体 的一种流程如下:
的一种流程如下:

资料:i.磷灰石的主要成分是
ii. 可溶于水,
可溶于水, 微溶于水
微溶于水
ii.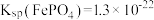
iv.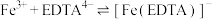
(1)制备
①用 溶液、
溶液、 溶液
溶液分步 浸取磷灰石生成HF、 和
和 ,主要反应是
,主要反应是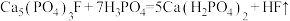 和
和_______ 。
②增大酸浸反应速率的措施有_______ (只写1条)。
③其他条件不变时,若仅用 溶液酸浸,浸取的速率低于用
溶液酸浸,浸取的速率低于用 、
、 分步浸取法,原因是
分步浸取法,原因是_______ 。
(2)制备
将 、
、 、
、 混合并调节溶液的pH制备
混合并调节溶液的pH制备 。
。
①酸性条件下,生成 的离子方程式是
的离子方程式是_______ 。
②含磷各微粒的物质的量分数与pH的关系如图。
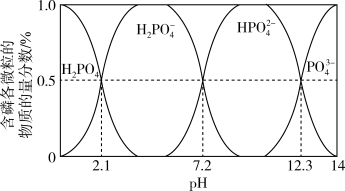
pH=1时,溶液中的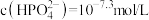 ,则
,则
_______  。再加入
。再加入 晶体、
晶体、 溶液使溶液中的
溶液使溶液中的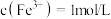 ,不考虑溶液体积的变化,通过计算说明此时能否产生
,不考虑溶液体积的变化,通过计算说明此时能否产生 沉淀
沉淀_______ 。
③ 的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。
的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。
ⅰ.研究表明,沉淀时可加入含 的溶液,
的溶液, 的作用是
的作用是_______ 。
ⅱ.其他条件不变时,工业上选择pH=2而不是更高的pH制备 ,可能的原因是
,可能的原因是_______ (答出2点)。
 的一种流程如下:
的一种流程如下:
资料:i.磷灰石的主要成分是

ii.
 可溶于水,
可溶于水, 微溶于水
微溶于水ii.
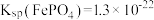
iv.
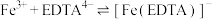
(1)制备

①用
 溶液、
溶液、 溶液
溶液 和
和 ,主要反应是
,主要反应是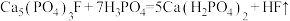 和
和②增大酸浸反应速率的措施有
③其他条件不变时,若仅用
 溶液酸浸,浸取的速率低于用
溶液酸浸,浸取的速率低于用 、
、 分步浸取法,原因是
分步浸取法,原因是(2)制备

将
 、
、 、
、 混合并调节溶液的pH制备
混合并调节溶液的pH制备 。
。①酸性条件下,生成
 的离子方程式是
的离子方程式是②含磷各微粒的物质的量分数与pH的关系如图。

pH=1时,溶液中的
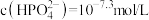 ,则
,则
 。再加入
。再加入 晶体、
晶体、 溶液使溶液中的
溶液使溶液中的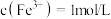 ,不考虑溶液体积的变化,通过计算说明此时能否产生
,不考虑溶液体积的变化,通过计算说明此时能否产生 沉淀
沉淀③
 的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。
的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。ⅰ.研究表明,沉淀时可加入含
 的溶液,
的溶液, 的作用是
的作用是ⅱ.其他条件不变时,工业上选择pH=2而不是更高的pH制备
 ,可能的原因是
,可能的原因是
您最近一年使用:0次
2022-04-10更新
|
920次组卷
|
7卷引用:四川省邻水实验学校2021-2022学年高二下学期第二次月考理综化学试题
四川省邻水实验学校2021-2022学年高二下学期第二次月考理综化学试题北京市西城区2022届高三一模化学试题(已下线)三轮冲刺卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)北京市第八中学2022-2023 学年高三上学期12 月月考化学试题北京市八一学校2022-2023学年高三上学期12月月考化学试题(已下线)北京市第四中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期末考试化学试卷
名校
解题方法
6 . 钼(Mo)是重要的过渡金属元素,具有广泛用途。由钼精矿(主要成分是MoS2)湿法回收钼酸铵[(NH4)2MoO4]部分工艺流程如下:

(1)“氧化焙烧”时通常采用粉碎矿石、逆流焙烧或增大空气量等措施,除了增大氧化焙烧速率,其作用还有_______ 。MoS2焙烧时得到+6价钼的氧化物,焙烧时的化学方程式为_______ 。
(2)向“滤液1”中加入硝酸,调节pH为5~7,加热到65~70℃过滤除硅。则滤渣2的成分为_______ 。
(3)为了提高原料的利用率,工艺流程中“滤渣1”应循环到_______ 操作。
(4)向“滤液2”先加入有机溶剂“萃取”,再加氨水“反萃取”,进行“萃取”和“反萃取”操作的目的是_______ 。
(5)“酸沉”中析出钼酸铵晶体时,加入HNO3调节pH为1.5~3,其原因是_______ 。
(6)Na2MoO4·2H2O是一种无公害型冷却水系统的金属缓蚀剂,常用钼酸铵和氢氧化钠反应来制取。写出制备Na2MoO4·2H2O的化学方程式_______ 。

(1)“氧化焙烧”时通常采用粉碎矿石、逆流焙烧或增大空气量等措施,除了增大氧化焙烧速率,其作用还有
(2)向“滤液1”中加入硝酸,调节pH为5~7,加热到65~70℃过滤除硅。则滤渣2的成分为
(3)为了提高原料的利用率,工艺流程中“滤渣1”应循环到
(4)向“滤液2”先加入有机溶剂“萃取”,再加氨水“反萃取”,进行“萃取”和“反萃取”操作的目的是
(5)“酸沉”中析出钼酸铵晶体时,加入HNO3调节pH为1.5~3,其原因是
(6)Na2MoO4·2H2O是一种无公害型冷却水系统的金属缓蚀剂,常用钼酸铵和氢氧化钠反应来制取。写出制备Na2MoO4·2H2O的化学方程式
您最近一年使用:0次



