名校
1 . 下列有关物质的性质与用途具有对应关系的是
| A.聚四氟乙烯耐酸碱腐蚀,可制作酸碱通用滴定管活塞 |
| B.明矾具有氧化性,可用于除去水中悬浮杂质 |
| C.MgO是离子化合物,可用于电解制取金属镁 |
D.FeS具有还原性,可用于除去废水中的 |
您最近半年使用:0次
名校
解题方法
2 . 将黄铁矿(主要成分 ,含杂质
,含杂质 等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝
等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝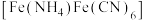 颜料,工艺流程如下:
颜料,工艺流程如下:
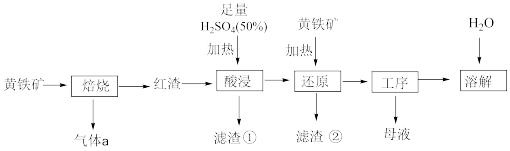

已知: 不与
不与 反应。
反应。
(1)写出黄铁矿焙烧的化学方程式___________ ;为提高焙烧的效率,可以采取的措施为___________ 。
A.进一步粉碎矿石 B.通入适当过量的空气 C.降低焙烧的温度
写出气体a的一种用途___________ 。
(2)在“还原”过程中,不会生成S单质,写出该过程中反应的离子方程式___________ 。
(3)在“沉铁”过程中会产生白色沉淀 ,该物质中
,该物质中 的化合价为
的化合价为___________ ,则“氧化”过程中加入 的作用是
的作用是___________ 。
(4) 用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备
用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备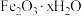 和
和 ,所加的物质为
,所加的物质为___________ 和___________ (填化学式,不引入新的杂质)。
(5)在“洗涤”过程中检验沉淀是否洗涤干净的方法是___________ 。
 ,含杂质
,含杂质 等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝
等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝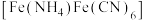 颜料,工艺流程如下:
颜料,工艺流程如下:

已知:
 不与
不与 反应。
反应。(1)写出黄铁矿焙烧的化学方程式
A.进一步粉碎矿石 B.通入适当过量的空气 C.降低焙烧的温度
写出气体a的一种用途
(2)在“还原”过程中,不会生成S单质,写出该过程中反应的离子方程式
(3)在“沉铁”过程中会产生白色沉淀
 ,该物质中
,该物质中 的化合价为
的化合价为 的作用是
的作用是(4)
 用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备
用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备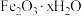 和
和 ,所加的物质为
,所加的物质为(5)在“洗涤”过程中检验沉淀是否洗涤干净的方法是
您最近半年使用:0次
3 . 下列物质性质、用途描述正确的是
A.利用 的氧化性,用作植物保鲜剂 的氧化性,用作植物保鲜剂 |
B.利用 的还原性,将废水中的 的还原性,将废水中的 转化为沉淀 转化为沉淀 |
C.利用 的漂白性,除去废水中的色素 的漂白性,除去废水中的色素 |
D.利用 的还原性,用作核反应堆的传热介质 的还原性,用作核反应堆的传热介质 |
您最近半年使用:0次
名校
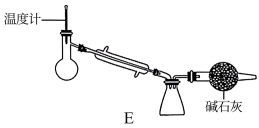
4 . 四氯化钛(TiCl4)是工业生产重要中间产品的原料,并有着广泛的用途。它为无色或淡黄色液体,熔点为—30℃,沸点为136.4℃,极易水解。在实验室用钛铁矿(FeTiO3)为原料制备TiCl4实验装置如图所示:
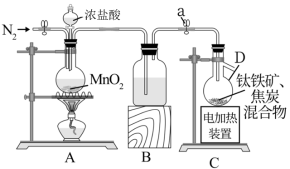
已知:(1)FeCl3熔点为306℃,沸点为316℃,极易水解;
(2)①Ag++SCN—=AgSCN↓;②Ksp(AgCl)>Ksp(AgSCN)。
请回答下列问题:
(1)装置A加热前先通一段时间N2,其目的是___ 。
(2)仪器D的名称是___ ;装置B中盛放的试剂名称是___ 。
(3)装置A中发生反应的离子方程式为___ 。
(4)装置C中发生反应的化学方程式为___ 。
(5)该制备装置不足之处:
①无尾气处理装置,CO与剩余Cl2会污染环境;
②___ 。
(6)停止滴加浓盐酸并关闭止水夹a,将装置c中所得物质转移到装置E中进行相关操作。装置E的作用是___ 。
(7)测定TiCl4产品的纯度。实验步骤如下:
①E装置相关操作结束后,待锥形瓶中的液体冷却至室温,准确称取14.0gTiCl4产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,过滤后将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL2.900mol•L-1AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X溶液为指示剂,用0.1000mol•L-1KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
根据以上步骤计算产品中TiCl4的质量分数为___ (已知产品中杂质不参与反应);若省去步骤③,所测定TiCl4产品的质量分数将会___ (选填“偏大”“偏小”或“不变”)。


已知:(1)FeCl3熔点为306℃,沸点为316℃,极易水解;
(2)①Ag++SCN—=AgSCN↓;②Ksp(AgCl)>Ksp(AgSCN)。
请回答下列问题:
(1)装置A加热前先通一段时间N2,其目的是
(2)仪器D的名称是
(3)装置A中发生反应的离子方程式为
(4)装置C中发生反应的化学方程式为
(5)该制备装置不足之处:
①无尾气处理装置,CO与剩余Cl2会污染环境;
②
(6)停止滴加浓盐酸并关闭止水夹a,将装置c中所得物质转移到装置E中进行相关操作。装置E的作用是
(7)测定TiCl4产品的纯度。实验步骤如下:
①E装置相关操作结束后,待锥形瓶中的液体冷却至室温,准确称取14.0gTiCl4产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,过滤后将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL2.900mol•L-1AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X溶液为指示剂,用0.1000mol•L-1KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
根据以上步骤计算产品中TiCl4的质量分数为
您最近半年使用:0次



