名校
1 . 下列物质的用途或事实与盐类的水解无关的是
A.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 |
B.明矾[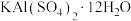 ]用于净水 ]用于净水 |
C.用热饱和 溶液清洗试管壁上附着的植物油 溶液清洗试管壁上附着的植物油 |
D.由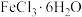 制取无水 制取无水 固体时,需在HCl气流中蒸发 固体时,需在HCl气流中蒸发 |
您最近半年使用:0次
2023-11-29更新
|
311次组卷
|
3卷引用:北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题
名校
2 . 下列物质的用途涉及氧化还原反应的是
| A.用NaHCO3作食品膨松剂 |
| B.用暖宝贴(成分:铁粉、水、食盐、活性炭等)供热 |
| C.用饱和Na2CO3溶液和盐酸处理水垢中的CaSO4 |
| D.用可溶性的铁盐、铝盐作净水剂 |
您最近半年使用:0次
2022-04-29更新
|
273次组卷
|
3卷引用:北京市丰台区2022届高三二模化学试题
3 . 银及其化合物在制造钱币、电子工业、医药等方面具有广泛用途。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag2O为原料冶炼银的化学方程式为__ 。
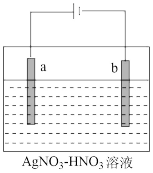
(2)电解精炼银的工作原理如图所示,___ (填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为___ 。
Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式__ 。
(4)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物。称取34g AgNO3固体,充分光照使其完全分解,测得反应后生成O2的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为__ 。
(5)纳米硫化(Ag2S)应用广泛。Ag2S溶于浓HNO3后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红棕色。写出反应的化学方程式__ 。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag2O为原料冶炼银的化学方程式为
(2)电解精炼银的工作原理如图所示,

Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(4)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物。称取34g AgNO3固体,充分光照使其完全分解,测得反应后生成O2的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为
(5)纳米硫化(Ag2S)应用广泛。Ag2S溶于浓HNO3后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红棕色。写出反应的化学方程式
您最近半年使用:0次
2021-05-03更新
|
598次组卷
|
4卷引用:北京市丰台区2021届高三第二次模拟考试化学试题
北京市丰台区2021届高三第二次模拟考试化学试题北京市第三中学2021-2022学年高三上学期期中考试化学试题(已下线)第二章能力提升检测卷-2022年高考化学一轮复习讲练测(已下线)第二章 化学物质及其变化(测)-2023年高考化学一轮复习讲练测(全国通用)
4 . Na2CO3和NaHCO3是中学化学中常见的物质,在生产生活中有重要的用途
(1)常温下,0.1mol/L碳酸钠溶液pH约为12。原因是_____ (用离子方程式表示)。
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因________ 。
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度______ PbSO4(填“大于”或“小于”)。
②用离子方程式解释Na2CO3的作用________ 。
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大。原因是________ 。
(4)25℃时,在10mL0.1mol·L-1Na2CO3溶液中逐滴加入0.1mol·L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示:
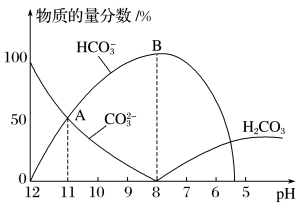
①请写出OAB段的离子方程式________ 。
②当pH=7时,溶液中主要含有哪些离子________ 。(除H+和OH-外)
(1)常温下,0.1mol/L碳酸钠溶液pH约为12。原因是
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度
②用离子方程式解释Na2CO3的作用
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大。原因是
(4)25℃时,在10mL0.1mol·L-1Na2CO3溶液中逐滴加入0.1mol·L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示:

①请写出OAB段的离子方程式
②当pH=7时,溶液中主要含有哪些离子
您最近半年使用:0次
13-14高三上·北京丰台·期末
名校
5 . 下列解释物质用途的反应方程式不正确的是
A.用Fe2(SO4)3净水:Fe3+ + 3H2O Fe(OH)3 + 3H+ Fe(OH)3 + 3H+ |
| B.用Na2S处理含Hg2+废水:Hg2+ + S2-=HgS↓ |
C.用Na2CO3溶液处理水垢中的CaSO4:Ca2+ +  =CaCO3↓ =CaCO3↓ |
D.燃煤时加入石灰石,减少SO2排放:2CaCO3 + 2SO2 + O2 2CaSO4 + 2CO2 2CaSO4 + 2CO2 |
您最近半年使用:0次
2016-12-09更新
|
918次组卷
|
3卷引用:2013届北京市丰台区高三上学期期末考试化学试卷



