1 . 下列说法不正确的是
| A.生铁中含碳,抗腐蚀能力比纯铁弱 |
| B.用锡焊接的铁质器件,焊接处易生锈 |
C.电解精炼铜时,阴极反应式为 |
| D.在铁制品上镀铜时,铁制品连接电源的正极 |
您最近一年使用:0次
2022-12-29更新
|
310次组卷
|
2卷引用:吉林省长春市第二实验中学2022-2023学年高二下学期4月月考化学试题
名校
解题方法
2 . 事物的变化都有两面性。下列关于金属的腐蚀和防护说法错误的是
| A.银首饰表面变黑属于电化学腐蚀 |
| B.食品袋里含炭粉、铁粉和食盐的除氧剂既能除氧又能除水 |
| C.为保护轮船的外壳,常在外壳上镶入锌块 |
| D.利用阳极氧化法处理铝制品的表面使之形成致密的氧化膜而防腐 |
您最近一年使用:0次
2022-12-07更新
|
244次组卷
|
5卷引用:吉林省四平市第一高级中学2022-2023学年高三上学期第三次月考化学试题
解题方法
3 . 回答下列问题:
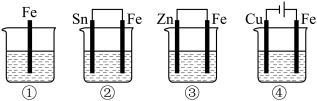
(1)图中各容器中盛有相同浓度的稀硫酸,铁被腐蚀的速率由快到慢的顺序是____ 。
(2)某兴趣小组的同学以甲醇燃料电池为电源研究有关电化学的问题。
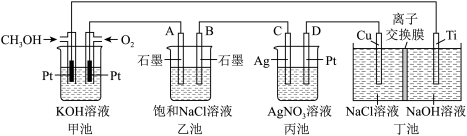
①甲池中,通入甲醇一极的电极反应式为_____ 。
②乙池中,A极(石墨)电极的电极反应式为____ 。
③丙池中,通电前C、D两电极的质量相同,通电一段时间后。
a.C电极的电极反应式为____ ,溶液中c(Ag+)将____ (填“增大”“减小”或“不变”)。
b.两极的质量相差17.28g,则甲池中消耗O2的体积为____ mL(标准状况下)。
 丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。
丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。
a.Ti电极的电极反应式为____ ,其附近溶液的碱性将____ (填“增大”“减小”或“不变”)。
b.Cu电极的电极反应式为____ 。
(1)图中各容器中盛有相同浓度的稀硫酸,铁被腐蚀的速率由快到慢的顺序是

(2)某兴趣小组的同学以甲醇燃料电池为电源研究有关电化学的问题。

①甲池中,通入甲醇一极的电极反应式为
②乙池中,A极(石墨)电极的电极反应式为
③丙池中,通电前C、D两电极的质量相同,通电一段时间后。
a.C电极的电极反应式为
b.两极的质量相差17.28g,则甲池中消耗O2的体积为
 丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。
丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。a.Ti电极的电极反应式为
b.Cu电极的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . 考古发掘出的古代青铜器(铜锡合金)文物常有 覆盖在其表面。下列说法正确的是
覆盖在其表面。下列说法正确的是
 覆盖在其表面。下列说法正确的是
覆盖在其表面。下列说法正确的是| A.铜易导电,属于电解质 |
| B.在自然环境中,青铜器中的锡加快了铜的腐蚀 |
| C.青铜器文物深浸在水中的腐蚀速率比暴露在空气中的快 |
D.生成 覆盖物的过程可能与电化学腐蚀有关 覆盖物的过程可能与电化学腐蚀有关 |
您最近一年使用:0次
解题方法
5 . 化学与生产生活密切相关。下列说法错误的是
| A.氯气可用于自来水杀菌消毒 |
| B.Al与Fe2O3的混合物作铝热剂可用于焊接铁轨 |
| C.泡沫灭火器可用于一般的起火,也适用于电器起火 |
| D.利用在船体水线以下贴装锌块的方式可减缓钢铁船体的腐蚀 |
您最近一年使用:0次
名校
6 . 《明会典》中记载:“嘉靖中则例,通宝钱六百万文,合用二火黄铜四万七千二百七十二斤……”这里黄铜是铜锌合金。下列说法错误的是
A.锌、铜均位于元素周期表的 区 区 |
| B.在铜、锌中,第二电离能与第一电离能相差较大的是锌 |
| C.在潮湿空气中,与黄铜中的铜相比,纯铜中的铜更容易被腐蚀 |
| D.用黄铜不用铁铸造“通宝钱”,主要因为黄铜的化学性质比铁稳定 |
您最近一年使用:0次
2022-10-28更新
|
179次组卷
|
5卷引用:吉林省通化市梅河口市第五中学2023-2024学年高三上学期9月月考化学试题
名校
解题方法
7 . 下列叙述正确的是
| A.在铁制品上镀铜时,镀件为阳极,铜盐溶液为电镀液 |
| B.钢铁水闸可用外加电流的阴极保护法防止其腐蚀 |
| C.钢铁吸氧腐蚀的负极反应:O2+2H2O+4e-=4OH- |
| D.船底镶嵌锌块,锌作阴极,以防船体被腐蚀 |
您最近一年使用:0次
名校
解题方法
8 . 如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片,观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面,以下有关解释合理的是


| A.生铁片中的碳是原电池的负极,发生还原反应 |
| B.雨水酸性较强,生铁片仅发生析氢腐蚀 |
| C.墨水回升时,碳极反应式为O2+2H2O+4e—=4OH— |
| D.具支试管中溶液pH逐渐减小 |
您最近一年使用:0次
2022-10-01更新
|
227次组卷
|
4卷引用:吉林省大安市第六中学2021-2022学年高二下学期期中考试化学试题
解题方法
9 . 原电池是将化学能转化为电能的装置。分析甲、乙两原电池装置,回答下列问题:
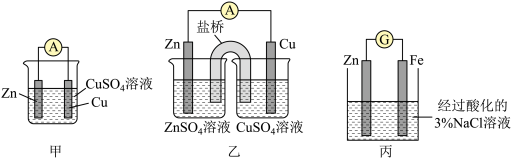
(1)甲、乙两装置中铜电极都有红色物质析出,则Zn电极是___________ 极,Cu电极表面发生反应的电极反应式为___________ ;盐桥中K+向___________ 移动(填“左”或“右”)。
(2)把甲池中的物质进行替换后变成丙装置,用以探究牺牲阳极的阴极保护法。一段时间后往Fe电极区滴入2滴铁氰化钾溶液,烧杯中的溶液颜色___________ (填“有”或“无)变化,若把Zn换成Cu后,Fe电极的反应式 ___________ 继,续反应一段时间后现象为___________ 。

(1)甲、乙两装置中铜电极都有红色物质析出,则Zn电极是
(2)把甲池中的物质进行替换后变成丙装置,用以探究牺牲阳极的阴极保护法。一段时间后往Fe电极区滴入2滴铁氰化钾溶液,烧杯中的溶液颜色
您最近一年使用:0次
10 . 有关钢铁腐蚀与防护的说法正确的是
| A.析氢腐蚀和吸氧腐蚀,负极均是Fe发生还原反应:Fe—2e—=Fe2+ |
| B.在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| C.镀层破损后,镀锡铁板的镀层仍能对铁制品起保护作用,比镀锌铁板更耐腐蚀 |
| D.将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
您最近一年使用:0次
2022-09-15更新
|
276次组卷
|
2卷引用:吉林省长春市部分高中2022-2023学年高二上学期10月月考化学试题



