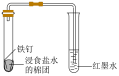
1 . 利用下列装置(夹持装置省略)进行实验,能达到实验目的的是
|
|
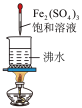
| A.证明氯水中有酸 | B.观察铁的的吸氧腐蚀 |
|
|
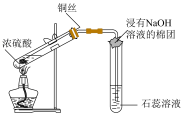
| C.制备Fe(OH)3胶体 | D.检验二氧化硫的漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列说法正确的是
| A.二氧化硅是一种半导体材料,应用于电子工业 |
| B.聚氯乙烯是一种重要的塑料,常用作食品保鲜膜 |
| C.马口铁(镀锡铁皮)镀层破坏后,镀层仍能起保护作用 |
| D.二氧化硫是一种抗氧化剂,可用作食品添加剂 |
您最近半年使用:0次
3 . 古代青铜器的出土,体现了古代中国对人类物质文明的巨大贡献。青铜器埋藏会产生多种锈蚀产物,其中 结构致密,可以阻止内部青铜继续被腐蚀,而
结构致密,可以阻止内部青铜继续被腐蚀,而 结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:不正确 的是
 结构致密,可以阻止内部青铜继续被腐蚀,而
结构致密,可以阻止内部青铜继续被腐蚀,而 结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
A.青铜锈蚀Ⅰ过程属于电化学腐蚀,负极的电极反应方程式为: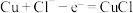 |
B.青铜锈蚀Ⅰ过程中 浓度越大,腐蚀趋势越大 浓度越大,腐蚀趋势越大 |
C.青铜锈蚀Ⅲ生成 的方程式为: 的方程式为: |
| D.青铜器修复可用碳酸钠溶液浸泡一段时间,使其保存更长久 |
您最近半年使用:0次
2024-04-18更新
|
253次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
解题方法
4 . 利用下列仪器、装置及药品能达到实验目的的是
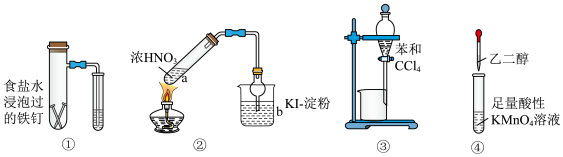
| A.图①装置可用于验证钢铁的吸氧腐蚀 | B.图②装置b中溶液变蓝能够说明浓 分解生成 分解生成 |
| C.图③装置可通过加水分离两种物质 | D.图④装置可制取乙二酸 |
您最近半年使用:0次
5 . 下列说法不正确 的是
| A.原电池中,正、负极材料可以是活性相同的材料,电极材料不一定参与反应 |
| B.“牺牲阳极法”是把被保护的设备外接直流电源负极,惰性电极做辅助阳极 |
| C.用惰性电极电解强酸强碱盐的水溶液时,阳极上产生的气体可能不是氧气 |
D.电解精炼铜时电解质溶液中加入硫酸,可提高溶液导电能力并抑制 水解 水解 |
您最近半年使用:0次
6 . 化学小组研究金属的电化学腐蚀,实验如下:
下列说法正确的是
| 实验 | Ⅰ | Ⅱ |
| 装置 | 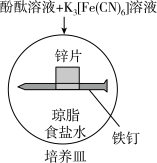 |  |
| 现象 | 锌片附近处颜色无变化,裸露在外的铁钉附近处出现红色。 | 铜片附近处出现红色,裸露在外的铁钉附近处出现蓝色 |
| A.实验I和Ⅱ中铁钉均为负极 |
B.实验I和Ⅱ中均发生吸氧腐蚀,且铁钉腐蚀速度实验 实验Ⅱ 实验Ⅱ |
C.一段时间后,实验I铁钉附近也出现了蓝色,可能是 氧化了单质 氧化了单质 |
| D.一段时间后,实验I和实验Ⅱ中均出现红褐色 |
您最近半年使用:0次
7 . 化学是一门以实验为基础的科学,下列有关实验装置或操作合理的是
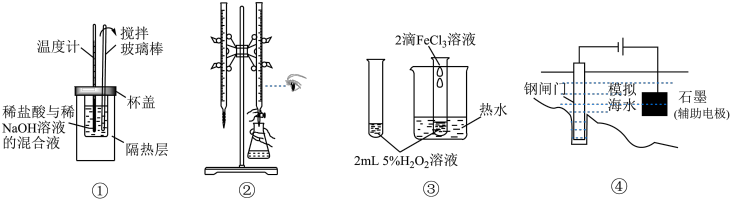

| A.图①是测定中和反应反应热 | B.图②是用标准盐酸滴定氢氧化钠溶液的过程 |
| C.图③是研究催化剂对化学反应速率的影响 | D.图④是模拟保护钢闸门 |
您最近半年使用:0次
8 . 破损的镀锌铁皮在氨水中发生电化学腐蚀,生成 和
和 ,下列说法不正确的是
,下列说法不正确的是
 和
和 ,下列说法不正确的是
,下列说法不正确的是| A.氨水浓度越大,腐蚀趋势越大 |
B.随着腐蚀的进行,溶液 变大 变大 |
C.铁电极上的电极反应式为: |
D.每生成标准状况下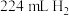 ,消耗 ,消耗 |
您最近半年使用:0次
2024-02-02更新
|
1433次组卷
|
2卷引用:2024年浙江高考真题化学(1月)
9 . 钢铁是用量最大的合金,防止钢铁腐蚀有利用于节约资源。下列防止钢铁腐蚀的方法不正确 的是
| A.水里的铁闸与直流电源的正极相连 | B.家用铁锅用完及时将水擦干 |
| C.铁质栏杆外面涂刷一层油漆 | D.轮船表面焊接锌块 |
您最近半年使用:0次
名校
解题方法
10 . 由下列实验操作及现象能得出相应结论的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 常温下,用pH计测得0.1 mol/L弱酸盐NaA、NaB、NaC溶液pH值分别为a、b、c | 若c>b>a | 水解程度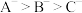 |
| B | 向BaCl2溶液中通入SO2和气体X | 产生白色沉淀 | 气体X一定为氧化剂 |
| C | 将稀硫酸酸化的H2O2加入 溶液中 溶液中 | 溶液出现黄色 | 说明H2O2的氧化性比Fe3+强 |
| D | 一块除去铁锈的铁片上滴一滴铁氰化钾溶液,静置2~3 min | 生成蓝色沉淀 | 铁片上可能发生了电化学腐蚀 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次