名校
解题方法
1 . 下列水龙头中,与铁制自来水管连接,水管腐蚀最快的是
| A.铜制水龙头 | B.铁制水龙头 | C.塑料水龙头 | D.陶瓷水龙头 |
您最近一年使用:0次
2020-10-03更新
|
158次组卷
|
4卷引用:福建省泉州科技中学2022-2023学年高二上学期期中考试化学试题
福建省泉州科技中学2022-2023学年高二上学期期中考试化学试题福建省三明市四地四校2021-2022学年高二上学期期中联考协作卷化学试题上海交通大学附属中学2019-2020学年高二上学期期中考试化学试题(已下线)4.3.1 金属的腐蚀(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
名校
解题方法
2 . 2018年7月至9月,国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。已知:正常海水呈弱碱性。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为_______ 。
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船进行了处理。

①下列说法不正确的是________ 。
A.锌块发生氧化反应:Zn-2e-=Zn2+
B.舰体有电子流入,可以有效减缓腐蚀
C.若通过外加电源保护舰体,应将舰体与电源正极相连
D.地下钢铁管道用导线连接锌块与该种舰体保护法原理相同
②采用“牺牲阳极的阴极保护法”后,舰体上正极的电极反应式为_________ 。
(3)船上有些器皿是铜制品,表面有铜锈。
①据了解铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。

下列说法正确的是________
A.疏松的Cu2(OH)3Cl属于有害锈
B.Cu2(OH)2CO3既能溶于盐酸也能溶于氢氧化钠溶液
C.青铜器表面涂一层食盐水可以做保护层
D.用HNO3溶液除锈可以保护青铜器的艺术价值,做到“修旧如旧”
②文献显示Cu2(OH)3Cl的形成过程中会产生CuCl(白色不溶于水的固体),将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,可以使CuCl转化为难溶的Cu2(OH)2CO3反应的离子方程式为______ 。
(4)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施保护文物。从电化学原理的角度分析“脱盐、干燥”的防腐原理:________ 。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船进行了处理。

①下列说法不正确的是
A.锌块发生氧化反应:Zn-2e-=Zn2+
B.舰体有电子流入,可以有效减缓腐蚀
C.若通过外加电源保护舰体,应将舰体与电源正极相连
D.地下钢铁管道用导线连接锌块与该种舰体保护法原理相同
②采用“牺牲阳极的阴极保护法”后,舰体上正极的电极反应式为
(3)船上有些器皿是铜制品,表面有铜锈。
①据了解铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。

下列说法正确的是
A.疏松的Cu2(OH)3Cl属于有害锈
B.Cu2(OH)2CO3既能溶于盐酸也能溶于氢氧化钠溶液
C.青铜器表面涂一层食盐水可以做保护层
D.用HNO3溶液除锈可以保护青铜器的艺术价值,做到“修旧如旧”
②文献显示Cu2(OH)3Cl的形成过程中会产生CuCl(白色不溶于水的固体),将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,可以使CuCl转化为难溶的Cu2(OH)2CO3反应的离子方程式为
(4)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施保护文物。从电化学原理的角度分析“脱盐、干燥”的防腐原理:
您最近一年使用:0次
2020-08-20更新
|
1057次组卷
|
11卷引用:福建省安溪一中、养正中学、惠安一中、泉州实验中学2022-2023学年高二上学期期中考联考化学试题
福建省安溪一中、养正中学、惠安一中、泉州实验中学2022-2023学年高二上学期期中考联考化学试题福建省泉州市 2022-2023学年高二上学期期中联考化学试题(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第28讲 金属的腐蚀与防护(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)安徽省宣城市2019-2020学年高二上学期期末考试化学试题(已下线)第01章 化学反应与能量转化(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)(已下线)练习10 金属的腐蚀与防护-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)河北省保定市2020-2021学年高二上学期期末考试化学试题(已下线)1.3.2 金属的电化学防护-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)四川省成都市第七中学2022-2023学年高二下学期3月月考化学试题第四章 章末训练
名校
解题方法
3 . 青铜器发生电化学腐蚀的原理示意图,下列说法正确的是
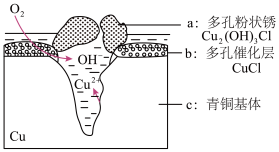

| A.腐蚀过程中,青铜基体是正极 |
| B.若有64g Cu腐蚀,理论上耗氧体积为22.4L(标准状况) |
| C.多孔催化层加速了青铜器的腐蚀,因为改变了反应的焓变 |
| D.为防止腐蚀,可通过导线将铜器与直流电源负极相连 |
您最近一年使用:0次
2020-08-14更新
|
691次组卷
|
11卷引用:福建省福州第十五中学2022-2023学年高二上学期10月月考化学试题
福建省福州第十五中学2022-2023学年高二上学期10月月考化学试题广州市天河中学2019—2020学年高二下学期期末测试化学试卷(已下线)第04章 电化学基础(A卷基础篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)第01章 化学反应与能量转化(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)山东省德州市夏津县第一中学2020-2021学年高二上学期第一次月考(10月)化学试题山东省济南市山东师范大学附属中学2020-2021学年高二上学期10月学业质量检测化学试题(已下线)专题4.4 金属的电化学腐蚀与防护-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)4.4 金属的电化学腐蚀与防护(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)山东省德州市夏津第一中学2021-2022学年高二上学期第一次月考化学试卷(已下线)4.3.2 金属的防护(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)4.3.1 金属的腐蚀(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
4 . 下列对实验方案的设计或评价合理的是
A. 经酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示具支试管中,一段时间后导管口有气泡冒出 经酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示具支试管中,一段时间后导管口有气泡冒出 |
B. 图中电流表会显示电流在较短时间内就会衰减 图中电流表会显示电流在较短时间内就会衰减 |
C. 图中应先用燃着的小木条点燃镁带,然后插入混合物中引发反应 图中应先用燃着的小木条点燃镁带,然后插入混合物中引发反应 |
D. 可用图显示的方法除去酸式滴定管尖嘴中的气泡 可用图显示的方法除去酸式滴定管尖嘴中的气泡 |
您最近一年使用:0次
2020-03-05更新
|
308次组卷
|
2卷引用:福建省福州第一中学2022-2023学年高二上学期12月月考化学试题
5 . 利用如下实验探究铁钉在不同溶液中的吸氧腐蚀。下列说法不正确的是
| 实验装置 | 实验编号 | 浸泡液 | pH | 氧气浓度随时间的变化 |
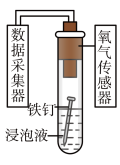 |  |  | 5 | 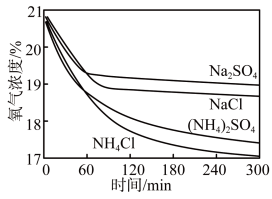 |
 | 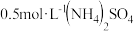 | 5 | ||
 |  | 7 | ||
 |  | 7 |
A.上述正极反应均为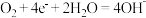 |
B.在不同溶液中, 是影响吸氧腐蚀速率的主要因素 是影响吸氧腐蚀速率的主要因素 |
C.向实验 中加入少量 中加入少量 固体,吸氧腐蚀速率加快 固体,吸氧腐蚀速率加快 |
D.在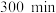 内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液 内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液 |
您最近一年使用:0次
2020-01-24更新
|
681次组卷
|
16卷引用:福建省福州市八县(市)一中2022-2023学年高二上学期11月期中联考化学试题
福建省福州市八县(市)一中2022-2023学年高二上学期11月期中联考化学试题(已下线)第14练 金属腐蚀和防护-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)福建省厦门第一中学2020-2021学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——化学反应速率的图像分析夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学反应速率及影响图像分析鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第4节 金属的腐蚀与防护人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第三节 金属的腐蚀与防护2河北省石家庄市二中学2021届高三上学期期中考试化学试题山西省实验中学2019届高三上学期第五次月考化学试题河北正定中学2020-2021学年高三上学期第四次半月考化学试题黑龙江省佳木斯市第一中学2021-2022学年高三上学期第五次调研考试化学试题浙江省温州市2021-2022学年高二上学期12月普通高中学考适应性测试化学试题天津市武清区杨村第一中学2021-2022学年高二上学期第三次月考化学试题重庆市万州第二高级中学2020-2021学年高二上学期期末考试化学试题2020高考化学二轮总复习高分必备 题型专题1 选择题专练北京市八一学校2023-2024学年高二上学期12月月考化学试题
名校
6 . 下列用来表示物质变化的化学用语中,正确的是( )
| A.碱性氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- |
| B.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| C.用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
| D.钢铁发生吸氧腐蚀时的正极反应式:Fe-2e-=Fe2+ |
您最近一年使用:0次
2020-01-02更新
|
889次组卷
|
4卷引用:福建省永安市第九中学2022-2023学年高二上学期9月月考化学试题
名校
7 . 某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_____________ 。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_______ ;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___________ 。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_____________ 。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究_____________________ 对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是_____________ 。
(1)同学们利用下表中装置进行实验并记录。
| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
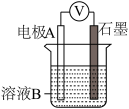 | Ⅰ | Fe | pH=2的H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究
您最近一年使用:0次
2019-11-21更新
|
1245次组卷
|
11卷引用:福建省莆田第六中学2022-2023学年高二上学期第二次月考(B卷)化学试题
福建省莆田第六中学2022-2023学年高二上学期第二次月考(B卷)化学试题福建省厦门第一中学2020-2021学年高二10月月考化学试题(已下线)第4章 电化学基础(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)【教材实验热点】09 化学能与电能河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题江苏省苏州市张家港高级中学2019-2020学年高二上学期期中考试化学试题安徽省太和第一中学2019-2020学年高一下学期期末考试化学试题河北省承德市隆化存瑞中学2019-2020学年高一下学期期末测试化学试题(已下线)专题4.4 金属的电化学腐蚀与防护-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)4.4 金属的电化学腐蚀与防护(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第4章 化学反应与电能(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
名校
8 . 下列有关装置图的叙述中正确的是
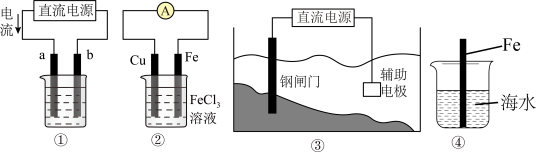

| A.用装置①给铜镀银,则b极为单质银,电解质溶液为AgNO3溶液 |
| B.装置②的总反应式:Cu + 2Fe3+ = Cu2+ + 2Fe2+ |
| C.装置③中钢闸门应与电源的负极相连被保护,该方法叫做外加电流的阴极保护法 |
| D.装置④中插入海水中的铁棒,越靠近底端腐蚀越严重 |
您最近一年使用:0次
2019-02-02更新
|
324次组卷
|
6卷引用:福建省德化第一中学2022-2023学年高二上学期第一次质检化学试题
名校
9 . 我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,防护原理如图所示。下列说法错误的是
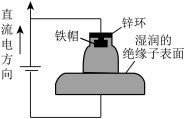

| A.通电时,锌环是阳极,发生氧化反应 |
| B.通电时,阴极上的电极反应为2H2O+2e-=H2↑+2OH- |
| C.断电时,锌环上的电极反应为Zn2++2e-=Zn |
| D.断电时,仍能防止铁帽被腐蚀 |
您最近一年使用:0次
2018-05-28更新
|
896次组卷
|
18卷引用:福建省福州市第一中学2022-2023学年高二上学期10月月考化学试题
福建省福州市第一中学2022-2023学年高二上学期10月月考化学试题(已下线)第14练 金属腐蚀和防护-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第36练 金属的腐蚀与防护-2023年高考化学一轮复习小题多维练(全国通用)第三节 金属的腐蚀与防护山东省菏泽市郓城第一中学2022-2023学年高二上学期自我检测(10月)化学试题福建省福州市闽侯县第一中学2023-2024学年高二上学期10月月考化学试题福建省厦门市松柏中学2023-2024学年高二上学期10月月考化学试题【全国市级联考】山东省潍坊市2018届高三第三次高考模拟考试理综化学试题(已下线)2018年高考题及模拟题汇编 专题08 电化学及其应用湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题16 金属的腐蚀与防护鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第4节 金属的腐蚀与防护高中必刷题高二选择性必修1第四章 化学反应与电能 第三节 金属的腐蚀与防护辽宁省大连市沙河口区辽宁师范大学附属中学2021届高三上学期10月模块考试化学试题(已下线)第17讲 电解池 金属的腐蚀与防护(练)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题六 金属的化学腐蚀与防护(练习)(已下线)考点20 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第四章 化学反应与电能 第三节 金属的腐蚀与防护
名校
10 . 埋在地下的钢管道可以用如图所示方法进行保护。下列说法正确的是


| A.该方法利用了电解池原理 |
| B.该方法称为“外加电流的阴极保护法” |
| C.在此装置中钢管道作正极 |
| D.镁块上发生的电极反应为O2+2H2O+4e-=== 4OH- |
您最近一年使用:0次
2018-03-06更新
|
298次组卷
|
7卷引用:福建省泉州市南安市侨光中学2022-2023学年高二上学期10月月考化学试题



