1 . I.回答下列问题
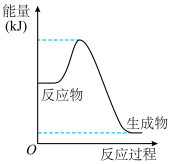
(1)下列变化中满足图示的是___________(填字母)。
(2)下图是在 101kPa、298K条件下,1mol NO₂气体和1mol CO反应生成 和 1mol NO 气体的能量变化的示意图。该反应的热化学方程式为
和 1mol NO 气体的能量变化的示意图。该反应的热化学方程式为___________ 。
(3)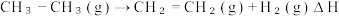 有关化学键的键能如上表所示。则该反应的反应热为ΔH=
有关化学键的键能如上表所示。则该反应的反应热为ΔH=___________ 。
Ⅱ. 近年来,我国化工技术获得重大突破,利用合成气(主要成分为 CO、CO₂和)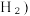 在催化剂的作用下合成甲醇(CH₃OH)是其中的一个研究项目。该研究发生的主要反应如下:
在催化剂的作用下合成甲醇(CH₃OH)是其中的一个研究项目。该研究发生的主要反应如下:
i. CO与H₂反应合成甲醇: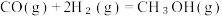
i i.CO₂与H₂反应合成甲醇:
(4)上述反应符合原子经济性的是反应___________ (i或ii)。
(5)在某一时刻采取下列措施,能使反应 i 的反应速率减小的措施是___________。
(6)一定温度下,在容积固定的密闭容器中发生反应ii,下列说法可以表明反应达到化学平衡状态的是___________。
(7)H₂还原 CO电化学法制备甲醇( 的工作原理如图所示:
的工作原理如图所示:___________ 极(填“正”或“负”),电池工作过程中  通过质子膜向
通过质子膜向___________ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________ 。
(1)下列变化中满足图示的是___________(填字母)。
| A.镁和稀盐酸的反应 |
B.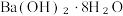 与NH₄Cl的反应 与NH₄Cl的反应 |
| C.NaOH 固体加入水中 |
| D.乙醇燃烧 |
(2)下图是在 101kPa、298K条件下,1mol NO₂气体和1mol CO反应生成
 和 1mol NO 气体的能量变化的示意图。该反应的热化学方程式为
和 1mol NO 气体的能量变化的示意图。该反应的热化学方程式为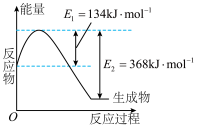
| 化学键 | C——H | C=C | C—C | H—H |
| 键能/(kJ·mol⁻¹) | 414 | 615 | 347.7 | 436.4 |
(3)
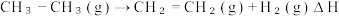 有关化学键的键能如上表所示。则该反应的反应热为ΔH=
有关化学键的键能如上表所示。则该反应的反应热为ΔH=Ⅱ. 近年来,我国化工技术获得重大突破,利用合成气(主要成分为 CO、CO₂和)
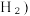 在催化剂的作用下合成甲醇(CH₃OH)是其中的一个研究项目。该研究发生的主要反应如下:
在催化剂的作用下合成甲醇(CH₃OH)是其中的一个研究项目。该研究发生的主要反应如下:i. CO与H₂反应合成甲醇:
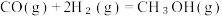
i i.CO₂与H₂反应合成甲醇:

(4)上述反应符合原子经济性的是反应
(5)在某一时刻采取下列措施,能使反应 i 的反应速率减小的措施是___________。
| A.恒温恒容下,再充入CO | B.升高温度 |
| C.恒温恒容下,向其中充入Ar | D.恒温恒压下,向其中充入 Ar |
(6)一定温度下,在容积固定的密闭容器中发生反应ii,下列说法可以表明反应达到化学平衡状态的是___________。
| A.单位时间内消耗 3molH₂, 同时生成1mol的 CH₃OH |
| B.CH₃OH 的体积分数不再发生变化 |
C.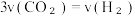 |
| D.容器内气体密度不再改变 |
(7)H₂还原 CO电化学法制备甲醇(
 的工作原理如图所示:
的工作原理如图所示: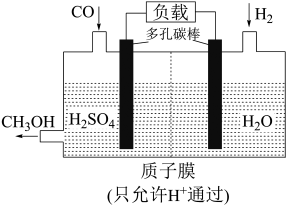
 通过质子膜向
通过质子膜向
您最近一年使用:0次
名校
解题方法
2 . 某科研人员提出:HCHO 与 O₂在羟基磷灰石(HAP)表面催化氧化生成(  和
和 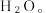 该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
 和
和 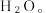 该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
| A.用 HAP 高效去除居室污染,符合绿色化学理念 |
| B.在反应示意图中,有 C—H键的断裂和C==O键的形成 |
| C.根据图示信息,CO₂分子中的氧原子全部来自O₂ |
| D.反应前后分子种类、原子种类均发生了变化 |
您最近一年使用:0次
名校
解题方法
3 . 有A、B、C、D、E五种短周期元素,A是地壳中含量最多的元素,B元素有3种同位素 B₁、B₂、B₃, B₃原子的质量数是B₁的3倍, C是非金属性最强的元素, D 和C可以形成DC型离子化合物,且离子的电子层结构相同,E元素原子的最外层电子数比内层电子总数少6个。下列说法正确的是
| A.离子半径: D⁺>C⁻ |
| B.EA₂是光导纤维的主要成分 |
| C.A和B不能形成原子个数比1∶1的化合物 |
| D.以上元素中形成的最高价氧化物对应的水化物酸性最强的是 C |
您最近一年使用:0次
名校
解题方法
4 . 下列反应对应的离子方程式正确的是
A.实验室用氨水与氯化铝溶液反应制取 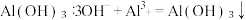 |
B.84 消毒液与洁厕灵混用产生有毒气体:  |
C.用浓氯化铁溶液制作印刷电路板:  |
D.硫氰化钾溶液与氯化铁溶液反应: 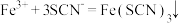 |
您最近一年使用:0次
名校
5 . 下列选项所示的物质间转化均能一步实现的是
A.NaCl(aq)→ Cl₂(g)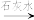 漂白粉(s) 漂白粉(s) |
B.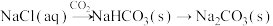 |
C.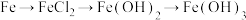 |
D. |
您最近一年使用:0次
名校
解题方法
6 . 下列各组变化中,前者是物理变化,后者是化学变化的是
| A.碘的升华、石油的分馏 |
| B.用NH₄Cl溶液(显酸性) 除铁锈、食盐水导电 |
| C.蛋白质溶液中加饱和(NH₄)₂SO₄溶液、蓝色的胆矾常温下变白 |
| D.煤的干馏、石油的裂化 |
您最近一年使用:0次
7 . 一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是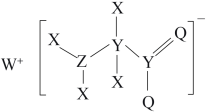
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近一年使用:0次
2024-04-08更新
|
96次组卷
|
14卷引用:福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题
福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题厦门外国语学校2021-2022学年高二下学期期中考试化学试题湖北省黄冈市麻城市第二中学2021-2022学年高二下学期3月月考化学试题 吉林省吉林第一中学2022-2023学年高二上学期11月月考化学试题福建省龙岩市一级校联盟2022-2023学年高二下学期4月期中考试化学试题福建省三明第一中学2022-2023学年高二下学期期中考试化学试题福建省厦门市湖滨中学2022-2023学年高二下学期期中考试化学试题云南省大理州实验中学2021-2022学年高二下学期化学期中考试题山东省德州市2020-2021学年高二下学期期末考试化学试题陕西省武功县普集高级中学2022-2023学年高二下学期第一次月考化学试题广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题2024届高考化学考点剖析精创专题卷——专题七 物质结构 元素周期律四川省达州市万源中学2023-2024学年高二下学期4月月考化学试题河南省郑州市十校2023-2024学年高二下学期期中联考化学试卷
解题方法
8 . Ⅰ.MnS纳米粒子被广泛应用于除去重金属离子中的铬离子。
(1)锰的价层电子排布式为______ 。
(2)磁性氧化铁纳米粒子除铬效率不如MnS纳米粒子,试比较两种纳米材料中的阴离子的半径大小O2-______ S2-(填“>”“<”或“=”)。H3O+中H—O—H的键角比H2O中的______ (填“大”或“小”)
(3)Mn可以形成多种配合物,[Mn(CO)(H2O)2(NH3)3]Cl2·H2O中第二周期元素第一电离能由大到小关系为______ ,Mn与CO的C原子形成配位键,该配合物的配位数为______ ,配体NH3的空间结构为______ (用文字描述)。
Ⅱ.
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为______ 。

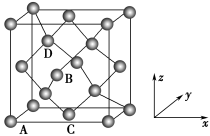
(5)图为金刚石晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为______ 。已知金刚石的晶胞参数为apm,则其密度为______ g·cm-3(列出计算式)。
(1)锰的价层电子排布式为
(2)磁性氧化铁纳米粒子除铬效率不如MnS纳米粒子,试比较两种纳米材料中的阴离子的半径大小O2-
(3)Mn可以形成多种配合物,[Mn(CO)(H2O)2(NH3)3]Cl2·H2O中第二周期元素第一电离能由大到小关系为
Ⅱ.
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为

(5)图为金刚石晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
您最近一年使用:0次
9 . 硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的轨道表示式为______ ,晶体硅和碳化硅熔点较高的是______ (填化学式);
(2)硅和卤素单质反应可以得到SiX4.SiX4的熔、沸点大小如下表所示:
①0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是______ (填化学式),沸点依次升高的原因是______ ,气态SiX4分子的空间构型是______ ;
②SiCl4与N甲基咪唑(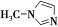 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
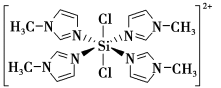
N甲基咪唑分子中碳原子的杂化轨道类型为______ ,H、C、N的电负性由大到小的顺序为______ ,1个M2+中含有______ 个σ键;
(1)基态硅原子最外层的轨道表示式为
(2)硅和卤素单质反应可以得到SiX4.SiX4的熔、沸点大小如下表所示:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
②SiCl4与N甲基咪唑(
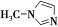 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
N甲基咪唑分子中碳原子的杂化轨道类型为
您最近一年使用:0次
10 . 断肠草为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构简式,相关推断正确的是
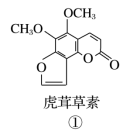

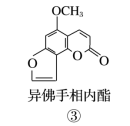
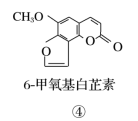




| A.②中所含官能团种类比③中多 |
| B.①和④互为同系物 |
| C.①与②、③与④分别互为同分异构体 |
| D.1mol③、④中均含有2mol双键 |
您最近一年使用:0次



