1 . 电化学在科技、生产、社会和生活的各个发面都发挥着重要的作用。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母)。这种防止金属材料腐蚀的方法叫做_______ 。

a.金块 b .锌板 c.铜板 d.钠块
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)

①写出A装置中发生反应的离子反应方程式:_______ 。
②写出燃料电池B中的负极的电极反应:_______ ;分析比较图示中a%与b%的大小:a% _______ b%(填“>”“<”或“=”);燃料电池B中的离子交换膜为_______ 离子交换膜。
(3)通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:
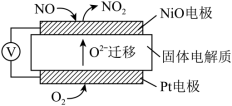
NiO电极上的电极反应式为_______ 。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.金块 b .锌板 c.铜板 d.钠块
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)

①写出A装置中发生反应的离子反应方程式:
②写出燃料电池B中的负极的电极反应:
(3)通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:

NiO电极上的电极反应式为
您最近一年使用:0次
2 . 实验小组研究金属电化学腐蚀,实验如下:
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ
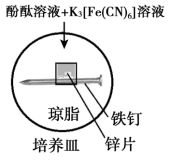
5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ

5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
| A.实验Ⅱ中Zn保护了Fe,使铁的腐蚀速率比实验Ⅰ慢 |
B.实验Ⅱ中正极的电极反应式: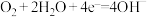 |
C.实验Ⅰ的现象说明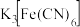 溶液与Fe反应生成了 溶液与Fe反应生成了 |
| D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
您最近一年使用:0次
2022-09-04更新
|
1372次组卷
|
13卷引用:福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题
福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题北京市第十二中学2021-2022学年高一下学期6月月考化学试题北京十二中2021-2022学年高一下学期六月月考(等级考)化学试题(已下线)【教材实验热点】17 金属的腐蚀与防护第四章 综合拔高练北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题山东省枣庄市第一中学2022-2023学年高二上学期期末达标化学试题福建省龙岩市连城县第一中学2023-2024学年高二上学期8月月考化学试题北京市朝阳区2021届高三上学期期末考试化学试题(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)北京市第四中学2021-2022学年高二上学期期中考试化学试题山东省滨州市2023-2024学年高三上学期11月期中考试化学试题
名校
3 . 《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_______ 。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
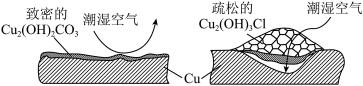
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因_____________ 。
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
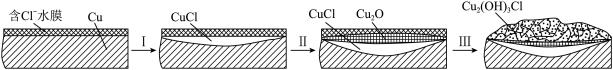
① 过程Ⅰ的正极反应物是___________ 。
② 过程Ⅰ负极的电极反应式是_____________ 。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:
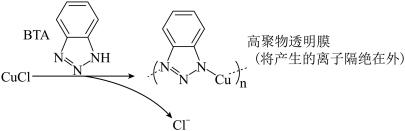
请回答下列问题:
①写出碳酸钠法的离子方程式___________________ 。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________ 。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:

Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:

① 过程Ⅰ的正极反应物是
② 过程Ⅰ负极的电极反应式是
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:

请回答下列问题:
①写出碳酸钠法的离子方程式
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
您最近一年使用:0次
2019-06-11更新
|
1878次组卷
|
7卷引用:福建省泉州市第六中学2022-2023学年高二上学期期中考化学试题



