名校
解题方法
1 . 某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中
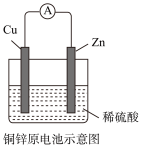
(1)外电路,电子从__________ 极流出。溶液中,阳离子向_______ 极移动。
(2)锌为____ 极,电极上发生的_______________ 反应(“氧化”或“还原”),电极反应式_______________ 锌片上观察到的现象为_____________________ ;铜为__________ 极,电极上发生的是_______________ 反应(“氧化”或“还原”), 电极反应式____________________________________ ,铜片上观察到现象的为__________
(3)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为______________ 。
(4)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_____ (填序号)。
A.无水乙醇 B.醋酸溶液 C.CuSO4溶液 D.苯
(5)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是____________ (填字母代号)。
A. NaOH+HCl=NaCl+H2O B. 2H2+O2=2H2O
C. Fe+2FeCl3=3FeCl2 D. 2H2O=2H2↑+O2↑

(1)外电路,电子从
(2)锌为
(3)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为
(4)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是
A.无水乙醇 B.醋酸溶液 C.CuSO4溶液 D.苯
(5)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是
A. NaOH+HCl=NaCl+H2O B. 2H2+O2=2H2O
C. Fe+2FeCl3=3FeCl2 D. 2H2O=2H2↑+O2↑
您最近一年使用:0次
名校
2 . 盐酸羟胺(化学式为NH3OHCl,其中N为-1价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
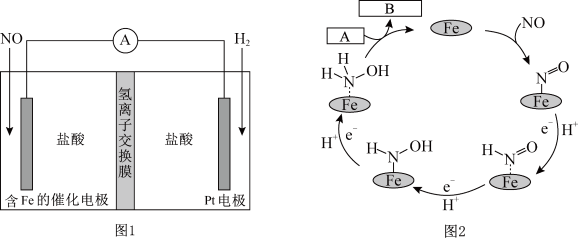

| A.含Fe的催化电极的电极反应为NO+3e-+4H+=NH3OH+ |
| B.图2中,A为H+,B为NH3OH+ |
| C.电池工作时,H+从右室穿过氢离子交换膜向左室迁移 |
| D.电池工作时,每消耗22.4LNO(标准状况),左室溶液质量增加34g |
您最近一年使用:0次
2022-10-30更新
|
447次组卷
|
2卷引用:新疆乌鲁木齐市高级中学2022-2023学年高三第一次模拟考试化学试题



