1 . 我国某大学最近研发出一种新型锂电池,该电池处于国内领先地位。以下是某种锂电池的电池反应:C6Li + Li1-xMO2 C6Li1-x + LiMO2(C6Li表示锂原子嵌入石墨形成的复合材料,LiMO2表示含锂的过度金属氧化物)。请回答问题:
C6Li1-x + LiMO2(C6Li表示锂原子嵌入石墨形成的复合材料,LiMO2表示含锂的过度金属氧化物)。请回答问题:
(1)锂电池放电时的负极反应为:C6Li -xe- = C6Li1-x + xLi+ ,则正极反应为:_______ 。
(2)电池放电时若转移1mol e-,消耗的负极材料_______ g。
 C6Li1-x + LiMO2(C6Li表示锂原子嵌入石墨形成的复合材料,LiMO2表示含锂的过度金属氧化物)。请回答问题:
C6Li1-x + LiMO2(C6Li表示锂原子嵌入石墨形成的复合材料,LiMO2表示含锂的过度金属氧化物)。请回答问题:(1)锂电池放电时的负极反应为:C6Li -xe- = C6Li1-x + xLi+ ,则正极反应为:
(2)电池放电时若转移1mol e-,消耗的负极材料
您最近一年使用:0次
名校
解题方法
2 . 如图中,甲是电解饱和食盐水,乙是电解精炼铜,丙是电镀,回答:

(1)b极上的电极反应式为___________ ,甲电池的总反应化学方程式是___________ 。
(2)在粗铜的电解精炼过程中,图中c电极的材料是___________ (填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为___________ ;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是___________ ,电解一段时间后,电解液中的金属离子有___________ 。
(3)如果要在铁制品上镀锌,则e电极的材料是___________ (填“铁制品”或“锌块”),电解质溶液可以用___________ 。若e电极的质量变化130 g,则a电极上产生的气体在标准状况下的体积为___________ 。

(1)b极上的电极反应式为
(2)在粗铜的电解精炼过程中,图中c电极的材料是
(3)如果要在铁制品上镀锌,则e电极的材料是
您最近一年使用:0次
名校
3 . 下图装置中:b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答
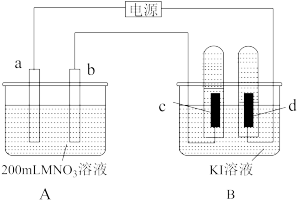
(1)a连接电源的___________ 极,a极上的电极反应式为___________ 。b极的电极反应式为___________ 。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是___________ 。此时C极上的电极反应式为___________ 。
(3)当d极上收集到44.8mL气体(标准状况)时,在b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为___________ 。

(1)a连接电源的
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是
(3)当d极上收集到44.8mL气体(标准状况)时,在b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为
您最近一年使用:0次
名校
解题方法
4 . 观察下列装置,回答下列问题。
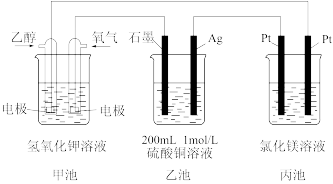
(1)甲装置中通入乙醇的电极反应式为___________ 。
(2)电解一段时间,乙池中石墨电极附近观察到的现象是___________ 。
(3)电解一段时间,当甲池消耗了112 mLO2(标况下),此时乙装置中溶液的pH为___________ (忽略电解前后溶液体积变化,忽略Cu2+的水解)。若要将该溶液完全恢复到电解前的浓度和pH,需要补充的物质是___________ ,其物质的量为___________ 。
(4)丙装置中总反应的离子方程式为___________ 。

(1)甲装置中通入乙醇的电极反应式为
(2)电解一段时间,乙池中石墨电极附近观察到的现象是
(3)电解一段时间,当甲池消耗了112 mLO2(标况下),此时乙装置中溶液的pH为
(4)丙装置中总反应的离子方程式为
您最近一年使用:0次
解题方法
5 . 微型纽扣电池在现代生活中应用广泛。有一种银锌电池,其电极分别是 和Zn,电解质溶液为KOH溶液,总反应式为
和Zn,电解质溶液为KOH溶液,总反应式为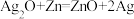 。回答下列问题:
。回答下列问题:
(1)Zn是_________ 极,发生_________ 反应,该电池的正极反应式为___________________________ 。
(2)电池内部电流方向是从_________ (填“ ”或“Zn”,下同)极流向
”或“Zn”,下同)极流向_________ 极,当外电路中有1mol  通过时,负极消耗的物质的质量是
通过时,负极消耗的物质的质量是_________ g。
(3)在使用过程中,电解质溶液中KOH的物质的量_________ (填“增大”“减小”或“不变”)。
 和Zn,电解质溶液为KOH溶液,总反应式为
和Zn,电解质溶液为KOH溶液,总反应式为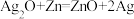 。回答下列问题:
。回答下列问题:(1)Zn是
(2)电池内部电流方向是从
 ”或“Zn”,下同)极流向
”或“Zn”,下同)极流向 通过时,负极消耗的物质的质量是
通过时,负极消耗的物质的质量是(3)在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
2020-12-30更新
|
153次组卷
|
3卷引用:河南省名校联盟2020-2021学年高二上学期12月联合考试化学试题
名校
解题方法
6 . 如图是一个电化学过程的示意图,请按要求回答下列问题:

(1)甲池是_______ 装置(填“原电池”或“电解池”),乙池中B为________ 极。
(2)写出电极反应式:通入O2电极:______ 。
(3)反应一段时间后,甲池中消耗(标况下)CH4体积为1.12 L,则乙池中转移电子___________ mol。
(4)电解饱和食盐水是重要的化工产业,它被称为 “氯碱工业”。完成下列问题:
①写出电解饱和食盐水的化学反应方程式___________ 。

②上图为电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,通电以后,Na+向右侧移动,可判断出电极2是___________ 极,在该电极周围的溶液中,NaOH浓度将会___________ (填“变大”或“减小”或“不变”);

(1)甲池是
(2)写出电极反应式:通入O2电极:
(3)反应一段时间后,甲池中消耗(标况下)CH4体积为1.12 L,则乙池中转移电子
(4)电解饱和食盐水是重要的化工产业,它被称为 “氯碱工业”。完成下列问题:
①写出电解饱和食盐水的化学反应方程式

②上图为电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,通电以后,Na+向右侧移动,可判断出电极2是
您最近一年使用:0次
7 . 已知甲池的总反应式:2CH3OH+3O2+4KOH=2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称。

甲池是____ 装置;乙池是___ 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是____ ,B(石墨)电极的名称是____ 。
(3)写出电极反应式:通入O2的电极的电极反应式是___ 。
(4)乙池中反应的化学方程式为___ 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2___ mL(标准状况下)。
(1)请回答图中甲、乙两池的名称。

甲池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)写出电极反应式:通入O2的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2
您最近一年使用:0次
8 . 如图装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:

(1)a为________ 极,c极的电极反应式为________ 。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:_______ ,电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应为________ 。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了________ mol气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为________ 。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200mL,取这种溶液加入到25.0mL 0.100mol·L-1 HCl溶液中,当加入31.25mL溶液时刚好沉淀完全。试计算:电解前A烧杯中MNO3溶液的物质的量浓度为________ 。

(1)a为
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200mL,取这种溶液加入到25.0mL 0.100mol·L-1 HCl溶液中,当加入31.25mL溶液时刚好沉淀完全。试计算:电解前A烧杯中MNO3溶液的物质的量浓度为
您最近一年使用:0次
2020-11-03更新
|
122次组卷
|
2卷引用:安徽省涡阳县育萃中学2020-2021学年高二上学期第一次月考化学试题
13-14高二·全国·单元测试
名校
解题方法
9 . (1)装置如图,打开K2,闭合K1。A极可观察到的现象是___ ;B极的电极反应为___ ,打开K1,闭合K2,A极可观察到的现象是_____ ;B极的电极反应为______ 。

(2)将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应为_____ ,电解反应的离子方程式为_____ , 实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积_____ L。


(2)将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应为

您最近一年使用:0次
2020-10-22更新
|
71次组卷
|
7卷引用:陕西省渭南市临渭区尚德中学2020-2021学年高二上学期第一次月考化学试题
10 . A、B、C三种强电解质,它们在水中电离出的离子的离子如下表所示:
在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16.0 g。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:
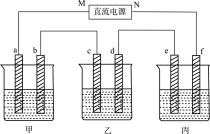
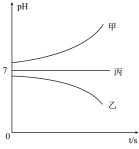
(1)b电极上的电极反应式为:_____ ;
(2)计算电极e上生成的气体在标况下的体积为_____ ;
(3)写出乙烧杯中的电解反应方程式:_____ ;
(4)要使丙烧杯中的C溶液恢复到原来的浓度,需要向丙烧杯中加入____ (填加入物质的名称和质量)。
(5)酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池放电产生的MnOOH。电池反应的离子方程式为:____ ;维持电流强度为0.5A,电池工作5min,理论上消耗锌_____ g(已知F=96500C·mol-1)。
阳离子 | Na+、K+、Cu2+、 |
阴离子 |
|


(1)b电极上的电极反应式为:
(2)计算电极e上生成的气体在标况下的体积为
(3)写出乙烧杯中的电解反应方程式:
(4)要使丙烧杯中的C溶液恢复到原来的浓度,需要向丙烧杯中加入
(5)酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池放电产生的MnOOH。电池反应的离子方程式为:
您最近一年使用:0次
2020-10-02更新
|
211次组卷
|
2卷引用:陕西省西安市第一中学2019-2020学年学高二上学期期末考试化学试题

 、OH-,
、OH-,

