1 . 某商用锂离子电池以石墨为负极材料,以LiCoO2为正极材料,电解质为LiPF6与乙烯碳酸酯。电池充电时,锂离子从正极材料中出来而进入负极,放电时则反过来。那么,下列说法中不正确的是
| A.充电时发生的正极反应为LiCoO2 →Li1-xCoO2 +xLi+ + xe- |
| B.负极反应为xLi++xe- +6C→LixC6 |
| C.正极材料Li1-xCoO2中的Co充电时被氧化,从Co3+变为Co4+,放电时被还原,从Co4+变为Co3+ |
| D.LiAlO2 和LiMn2O4等也可做正极材料 |
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
2 . 瑞典Linkoping(林雪平)大学研究出一款超级电池Power Paper,又称“纸电池”,该电池打破四项世界纪录,因拥有极其轻薄的厚度,并具有极佳的延展性和稳固性,反复经过多次折叠依然能保持良好状态。电池虽小,但其容量为26800毫安,约为iPhone电池容量的十倍,以保障手机具有持久的续航。而根据微软公布的消息,这是一种包含了柔性正电极和柔性负电极的电化学能量存储单元。正负电极都会在柔性的金属丝网上部署镓基液态金属。电化学能量存储单元还包括膜,该膜具有与柔性正电极接触的表面和与柔性负电极接触的相对表面,其结构简图如下图所示:

下列说法不正确的是:

下列说法不正确的是:
| A.由元素周期表可知,氢氧化镓能和苛性钠、苛性钾溶液反应;而纸电池具有柔韧性更好、容量更高、厚度更薄、延展性更好、稳固性更高等一系列的优点。 |
| B.若正极为铜片,负极分别是锌片和另一种银白色金属片,以NaCl溶液为电解液时,发现电流表指针的偏转方向相反,则另一种银白色金属片可能是银片。 |
C.此纸电池负极材料可以是铝片,正极材料可以是石墨片,若此原电池的电解液为NaOH溶液,其电极反应的负极反应式为:Al-e-+2OH-= AlO +H2O。 +H2O。 |
| D.原电池有携带方便、不需维护、可长期(几个月甚至几年)储存或使用等优点,但非氧化还原反应也可以设计成原电池,由此可得出原电池不等于化学电池。 |
您最近一年使用:0次
解题方法
3 . 已知: ;
; ;将
;将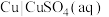 和
和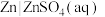 用盐桥连接构成原电池,下列情况下电动势的变化描述错误的是。
用盐桥连接构成原电池,下列情况下电动势的变化描述错误的是。
 ;
; ;将
;将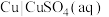 和
和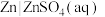 用盐桥连接构成原电池,下列情况下电动势的变化描述错误的是。
用盐桥连接构成原电池,下列情况下电动势的变化描述错误的是。A.在 和 和 浓度相同情况下, 浓度相同情况下,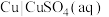 做正极, 做正极,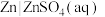 做负极 做负极 |
B.在 溶液中加入过量氨水,这时电池的电动势变小 溶液中加入过量氨水,这时电池的电动势变小 |
C.在 溶液中加入过量氨水,这时电池的电动势变大 溶液中加入过量氨水,这时电池的电动势变大 |
D.在 溶液和 溶液和 溶液中都加入过量氨水,这时电池的电动势变大 溶液中都加入过量氨水,这时电池的电动势变大 |
您最近一年使用:0次
4 . 巴格达电池发现于1936年6月,但其发明的时间距今已有大约两千年历史。巴格达电池外表看起来是一只简陋的小陶罐,但以陶罐内装的所有物质及其制作意图来判断,这只陶罐却像是一个电池的外壳。如下是其猜想的结构示意图,若用硫酸溶液作电解液,下列说法错误的是
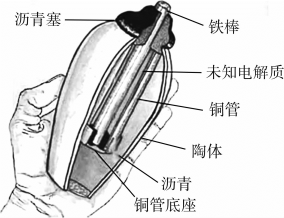

| A.铁作负极,铜作正极 |
| B.铜不发生反应 |
| C.理论上,电子回路中,每转移1 mol电子,铜管上就有22.4 L气体生成(标准状况) |
| D.放电后,氢离子浓度降低 |
您最近一年使用:0次
5 . 如图是一新型绿色电池的结构示意图,其中使用了最新研发的Rh SANs(单原子纳米酶)作为电极活性物质的催化剂,使葡萄糖和氧气之间的反应顺利地组成了原电池,葡萄糖反应后变为葡萄糖酸。下列说法错误的是


| A.Rh SANs可以降低葡萄糖还原的活化能 |
| B.该电池可以直接从日常生活中常见的饮料中收集燃料 |
C.理论上,每反应1 mol 共有2 mol葡萄糖被氧化 共有2 mol葡萄糖被氧化 |
| D.Rh SANs是需要附载在正极上 |
您最近一年使用:0次
6 . 电解质溶液A:25g CuSO4·5H2O + 4mL浓H2SO4 + 200mL H2O
电解质溶液B:16g CuCl+ 100mL浓HCIl+ 100mL H2O + 4g铜粉
以铜为电极,通电电解串连的两个电解槽(分别盛电解质溶液A和电解质溶液B)。正极质量改变如下表所示:
(1)正极质量改变不同的原因_______ 。
(2)电解质液中加铜粉的原因是_______ 。
(3)从理论上讲,电解过程铜粉质量不会改变,为什么?实际情况如何_______ 。
电解质溶液B:16g CuCl+ 100mL浓HCIl+ 100mL H2O + 4g铜粉
以铜为电极,通电电解串连的两个电解槽(分别盛电解质溶液A和电解质溶液B)。正极质量改变如下表所示:
| 电解前质量/g | 电解后质量/g | 改变量/g | ||
| 电解质液A | 正极 | 7.4 | 7.3 | -0.1 |
| 负极 | 7.5 | 7.6 | 0.1 | |
| 电解质液B | 正极 | 7.4 | 7.2 | -0.2 |
| 负极 | 7.3 | 7.5 | 0.2 |
(1)正极质量改变不同的原因
(2)电解质液中加铜粉的原因是
(3)从理论上讲,电解过程铜粉质量不会改变,为什么?实际情况如何
您最近一年使用:0次
解题方法
7 . 一种微型锂电池以锂与石墨作电极材料、以四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的溶液为电解质,具有容量大、电压稳定、工作温度范围宽(-56.7~71.1°C)等特点。下列有关说法中,不正确的是
| A.电池工作时,Li+向正极方向移动 |
| B.电池工作时,正极反应为2SOCl2+4e-=SO2+S+4Cl- |
| C.电池工作时,锂失去的电子与正极区析出硫的物质的量之比理论上为4:1 |
| D.电解质溶液要严禁混入水,因为锂会与水反应、SOCl2遇水会发生水解反应 |
您最近一年使用:0次
解题方法
8 . 一个容器被多孔隔板分隔成a、b两部分,a中盛放的是质量相等的两种金属氯化物混合物溶液、底部放一薄石墨片,b中盛放ZnCl2溶液、底部放一薄Zn片,这两个薄片可以与其上析出的沉淀一起称量。将溶液进行搅拌,用导线连接两薄片,两电极片质量变化与时间的关系如下表(按称量序号增大的次序,锌和水的反应可忽略不计):
下列说法中,不正确的是
| 称量编号 | 电极片质量的变化Δm/g | |
| 石墨 | Zn片 | |
| 实验前 | 0.00 | 0.00 |
| 1 | 0.00 | -0.20 |
| 2 | 0.00 | -0.40 |
| 3 | +0.49 | -0.56 |
| 4 | +0.74 | -0.64 |
| 5 | +1.47 | -0.88 |
| 6 | +1.30 | -1.04 |
| 7 | +1.15 | -1.18 |
| 8 | +0.95 | -1.37 |
| 9 | +0.95 | -1.37 |
| A.实验开始前,a中盛放的两种金属氯化物的质量均为18.2g |
| B.初期,石墨增量为0的原因是,两种金属氯化物中的一种被还原,且产物溶于水 |
| C.编号3~5的实验过程中发生了反应:Cu2++Cl-+e-=CuCl↓ |
| D.Cl-浓度在整个实验过程中的变化情况是:不变→减小→增加→不变 |
您最近一年使用:0次



