名校
解题方法
1 . 我国科学家开发的碳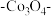 聚四氟乙烯催化剂可提高锌-空气碱性电池的放电性能,工作原理如图所示。
聚四氟乙烯催化剂可提高锌-空气碱性电池的放电性能,工作原理如图所示。
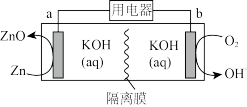
电池放电时,下列说法正确的是
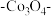 聚四氟乙烯催化剂可提高锌-空气碱性电池的放电性能,工作原理如图所示。
聚四氟乙烯催化剂可提高锌-空气碱性电池的放电性能,工作原理如图所示。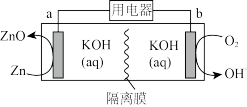
电池放电时,下列说法正确的是
| A.电子由a极经KOH溶液流入b极 |
B.放电时, 向b极移动 向b极移动 |
C.正极上的电极反应式为 |
D.a极净增1.6g时,b极有1.12L(标准状况) 参与反应 参与反应 |
您最近一年使用:0次
2022-05-25更新
|
424次组卷
|
3卷引用:河北省沧衡八校联盟2021-2022学年高一下学期期中考试化学试题
2 . 无膜氯液流电池是一种先进的低成本高储能电池,可广泛应用于再生能源储能和智能电网的备用电源等,工作原理如图所示,M为多孔碳电极,N为Na3Ti2( PO4)3和NaTi2(PO4)3电极。下列说法正确的是
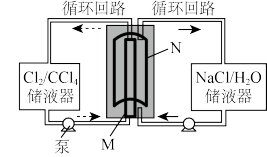

| A.放电时,M极电势高于N极 |
| B.放电时,N极的电极反应式为 NaTi2(PO4)3+2Na+ +2e- =Na3Ti2(PO4)3 |
| C.充电时,左侧储液器中Cl2的浓度减小 |
| D.充电时,电路中每转移1mole-,两电极质量变化的差值为23g |
您最近一年使用:0次
3 . 锌—空气电池(原理如图所示)适宜用作城市电动车的动力源,该电池放电时Zn转化为ZnO,该电池工作时下列说法正确的是


A.该电池正极的电极反应为 |
| B.该原电池中,电子由石墨电极经电解质溶液流入锌电极 |
C.该电池放电时 向锌电极移动 向锌电极移动 |
| D.该原电池工作一段时间后,电解质溶液的pH值变大 |
您最近一年使用:0次
名校
解题方法
4 . 微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置,某微生物燃料电池的工作原理如图所示(质子交换膜只允许 通过,a、b为电极),下列说法错误的是
通过,a、b为电极),下列说法错误的是
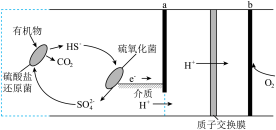
 通过,a、b为电极),下列说法错误的是
通过,a、b为电极),下列说法错误的是
| A.该电池在高温下进行效率更高 |
| B.b为电池正极,发生还原反应 |
| C.电子从电极a流出,经外电路流向电极b |
D.若该电池中有 参加反应,则电路中有0.4mol电子转移 参加反应,则电路中有0.4mol电子转移 |
您最近一年使用:0次
2023-05-02更新
|
373次组卷
|
2卷引用:山东省聊城第一中学2022-2023学年高一下学期期中考试化学试题
5 . 亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:
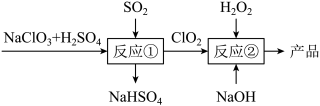
下列说法错误的是

下列说法错误的是
| A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2∶1 |
| B.若反应①通过原电池来实现,则ClO2是负极产物 |
| C.反应②中的H2O2可用NaClO4代替 |
| D.反应②条件下,ClO2的氧化性大于H2O2 |
您最近一年使用:0次
名校
解题方法
6 . 关于下列图示的说法中错误的是
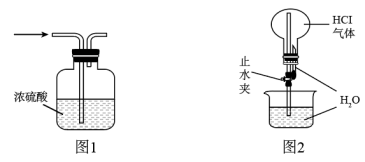
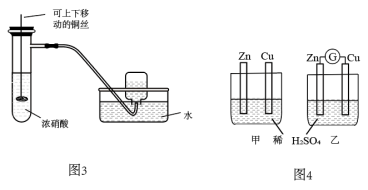


| A.用图1所示装置可以干燥SO2、NH3 | B.用图2所示装置演示喷泉实验 |
| C.用图3所示装置制备并收集少量NO2气体 | D.图4中两个烧杯内发生的化学反应相同 |
您最近一年使用:0次
2022-03-31更新
|
354次组卷
|
2卷引用:河北省邢台市卓越联盟2021-2022学年高一下学期第一次月考化学试题
解题方法
7 . 羟基自由基(•OH)是自然界中氧化性仅次于氟气的氧化剂。我国科学家设计了一种能将苯酚氧化为CO2和H2O的电化学装置。下列说法正确的是
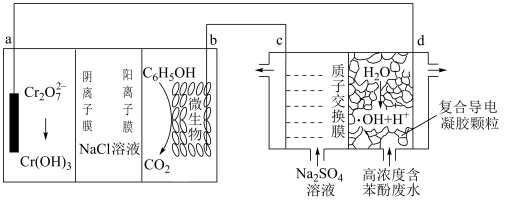

| A.d电极的电极反应式为:2H2O-4e-=4H++O2 |
| B.适当提高温度有利于提高微生物的活性,提高电池的性能 |
| C.电池运行过程中,NaCl溶液中溶质的量会逐渐减少,所以要不断补充NaCl |
D.当a极上有14molCr2O 参与反应时,右侧装置可以处理的苯酚的物质的量为3mol 参与反应时,右侧装置可以处理的苯酚的物质的量为3mol |
您最近一年使用:0次
8 . 某化学兴趣小组在三颈烧瓶中模拟雷雨条件下氮气和氧气反应,利用伽伐尼式氧气传感器测量反应过程中 含量,实验装置、氧气含量及氧气传感器结构如图所示。已知三颈烧瓶高压放电过程中有大量
含量,实验装置、氧气含量及氧气传感器结构如图所示。已知三颈烧瓶高压放电过程中有大量 等活性氧产生。下列说法错误的是
等活性氧产生。下列说法错误的是
 含量,实验装置、氧气含量及氧气传感器结构如图所示。已知三颈烧瓶高压放电过程中有大量
含量,实验装置、氧气含量及氧气传感器结构如图所示。已知三颈烧瓶高压放电过程中有大量 等活性氧产生。下列说法错误的是
等活性氧产生。下列说法错误的是
A.该传感器工作时 电极电势低于 电极电势低于 电极 电极 |
B.工作时 电极反应为 电极反应为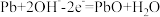 |
C.高压放电时,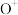 与 与 均参与电极反应,导致氧气传感器数值异常增大 均参与电极反应,导致氧气传感器数值异常增大 |
D.当空气中存在较多 时,氧气传感器测量数值偏小 时,氧气传感器测量数值偏小 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.镍氢电池、锂电池和碱性锌锰干电池都是二次电池 |
| B.燃料电池是一种高效但是会污染环境的新型电池 |
| C.化学电池的反应基础是氧化还原反应 |
| D.铅蓄电池放电的时候负极材料是Pb,正极材料是PbO2 |
您最近一年使用:0次
2023-03-15更新
|
291次组卷
|
2卷引用:山东省曹县第一中学2022-2023学年高一下学期2月月考化学试题
10 . 西北工业大学推出一种新型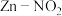 电池,通过自供电实现
电池,通过自供电实现 转化为
转化为 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
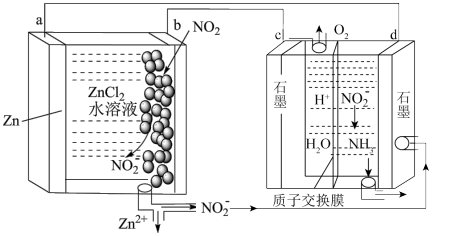
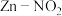 电池,通过自供电实现
电池,通过自供电实现 转化为
转化为 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
| A.b电极为原电池的正极 |
| B.装置工作时c极区溶液的pH减小 |
C.d电极反应式为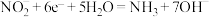 |
D.装置工作时,若消耗6.5gZn,理论上能得到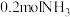 |
您最近一年使用:0次



