名校
1 . 某同学设计如下原电池,其工作原理如图所示。下列说法不正确 的是
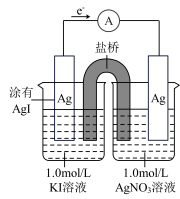

| A.该装置将化学能转化为电能 |
| B.负极的电极反应是:Ag +I--e-=AgI |
| C.电池的总反应是Ag+ +I-=AgI |
| D.盐桥(含KNO3的琼脂)中NO3-从左向右移动 |
您最近一年使用:0次
2019-07-30更新
|
1366次组卷
|
9卷引用:北京市朝阳区2018-2019学年高二第二学期期末统一考试化学试题
北京市朝阳区2018-2019学年高二第二学期期末统一考试化学试题(已下线)1.2.1 原电池的工作原理(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 化学能转化为电能——电池 课时2 化学电源高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 第一节综合训练(已下线)第2章 化学反应与能量(基础过关卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)选择性必修1专题1第二单元 综合训练福建省石狮市第一中学2022-2023学年高二上学期第一次月考化学试题(已下线)第六章 化学反应与能量 第35练 原电池 化学电源湖北省襄阳市第一中学2022-2023学年高一下学期4月月考化学试题
名校
2 . 下图为利用电化学方法处理有机废水的原理示意图。下列说法正确的是


| A.a、b极不能使用同种电极材料 |
| B.工作时,a极的电势低于b极的电势 |
| C.工作一段时间之后,a极区溶液的pH减小 |
D.b极的电极反应式为:CH3 COO-+4H2O-8e-=2HCO +9H+ +9H+ |
您最近一年使用:0次
2019-04-03更新
|
2513次组卷
|
6卷引用:【市级联考】山东省济南市2019届高三下学期模拟考试理科综合化学试题
名校
3 . 某种浓差电池的装置如下图所示,碱液室中加入电石渣浆液[主要成分为Ca(OH)2],酸液室通入CO2(以NaCl为支持电解质),产生电能的同时可生产纯碱等物质。下列叙述错误的是( )


| A.电子由M极经外电路流向N极 |
| B.N电极区的电极反应式为2H++2e-=H2↑ |
| C.在碱液室可以生成 NaHCO3、Na2CO3 |
| D.放电一段时间后,酸液室溶液pH增大 |
您最近一年使用:0次
2019-03-07更新
|
1160次组卷
|
4卷引用:【市级联考】福建省泉州市2019届高三毕业班下学期第一次质量检查理科综合化学试题
名校
4 . 将图1所示装置中的盐桥(琼脂-饱和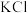 溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是

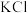 溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
A.图1中,铁棒质量减少5.6g,则甲池 溶液的质量增加5.6g 溶液的质量增加5.6g |
B.图1中的石墨电极与图2中乙池石墨 电极的电极反应式相同 电极的电极反应式相同 |
| C.两图所示装置的能量变化均是将化学能转化为电能 |
D.图2中电子流向为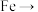 电流计→石墨a→石墨b→铜丝→石墨c→ 电流计→石墨a→石墨b→铜丝→石墨c→ |
您最近一年使用:0次
2019-01-13更新
|
755次组卷
|
6卷引用:【全国百强校】重庆市第八中学2018-2019学年高二上学期期中考试化学试题
5 . 液氨-液氧燃料电池曾用于驱动潜艇,其示意图如图所示,下列有关说法不正确的是
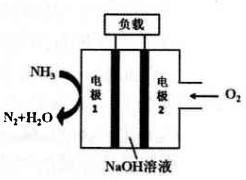

| A.电极2是正极,发生还原反应 |
| B.电池工作时,Na+向电极1移 动 |
| C.电流由电极2经外电路流向电极1 |
| D.电极1发生的电极反应为:2NH3+6OH--6e-= N2↑ +6H2O |
您最近一年使用:0次
2018-03-19更新
|
624次组卷
|
3卷引用:浙江省宁波市2018年3月新高考选考适应性考试化学试题
名校
6 . 已知LiAl/FeS电池是一种新型的车载可充电电池,该电池采用Li+交换膜。对该电池充电时, 阳极的电极反应式为:Li2S+Fe-2e-=2Li++FeS。下列有关该电池的说法中,正确的是
| A.化合物LiAl具有强还原性,作负极材料 |
| B.放电时,电子从LiAl极经过Li+交换膜流向FeS极 |
| C.放电时发生的总反应式为:2Li+FeS=Li2S+Fe |
| D.为了延长电池的使用寿命,可以隔一段时间添加含电解质的的水溶液 |
您最近一年使用:0次
2018-01-24更新
|
513次组卷
|
3卷引用:广东清远市2017—2018学年度第一学期期末教学质量检测高三理科综合化学试题
广东清远市2017—2018学年度第一学期期末教学质量检测高三理科综合化学试题山东省鄄城市第一中学2018-2019学年高二上学期第一次月考化学试题(已下线)【浙江新东方】高中化学20210304-004
7 . 燃料电池在工业生产中有重要用途,肼燃料电池产物对环境无污染,能量高,有广泛的应用前景,其工作原理如图所示。回答下列问题
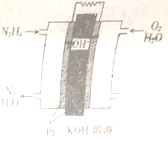
(1)该燃料电池中,负极通入的气体是_________ ,正极通入的气体是_________ .
(2)电池工作时,OH-向_____ 极移动,负极的电极反应式为_________ .
(3)肼在工业上常以氨和次氯酸钠为原料制得,其反应的化学方程式为2NH3+NaClO═N2H4+NaCl+H2O,该反应中每生成1molN2H4时,转移电子的物质的量为______ 。

(1)该燃料电池中,负极通入的气体是
(2)电池工作时,OH-向
(3)肼在工业上常以氨和次氯酸钠为原料制得,其反应的化学方程式为2NH3+NaClO═N2H4+NaCl+H2O,该反应中每生成1molN2H4时,转移电子的物质的量为
您最近一年使用:0次
解题方法
8 . 高锰酸钾广泛用作氧化剂。现有一个氧化还原反应的体系中共有KMnO4、MnSO4、H2O、Fe2(SO4)3、
FeSO4、H2SO4、K2SO4七种物质。
Ⅰ.写出一个包含上述七种物质的氧化还原反应方程式(需要配平):____________ 。
Ⅱ.某研究性学习小组根据上述反应设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol/L,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。
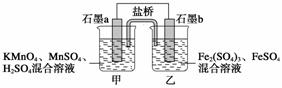
回答下列问题:
(1)此原电池的正极是石墨__________ (填“a”或“b”),发生________ 反应。
(2)电池工作时,盐桥中的SO42-移向________ (填“甲”或“乙”)烧杯。
(3)乙烧杯中的电极反应式分别为__________________ 。
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________ mol。
FeSO4、H2SO4、K2SO4七种物质。
Ⅰ.写出一个包含上述七种物质的氧化还原反应方程式(需要配平):
Ⅱ.某研究性学习小组根据上述反应设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol/L,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。

回答下列问题:
(1)此原电池的正极是石墨
(2)电池工作时,盐桥中的SO42-移向
(3)乙烧杯中的电极反应式分别为
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为
您最近一年使用:0次
名校
9 . 一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:CH3CH2OH + O2 === CH3COOH + H2O。下列有关说法正确的是( )
| A.负极上的反应为:CH3CH2OH+ H2O-4e- === CH3COOH + 4H+ |
| B.正极上发生的反应为:O2 + 4e- + 2H2O === 4OH- |
| C.检测时,电解质溶液中的H+向负极移动 |
| D.若有0.4mol电子转移,则消耗2.24L氧气 |
您最近一年使用:0次
名校
解题方法
10 . 如图是某同学设计的原电池装置,下列叙述中正确的是( )
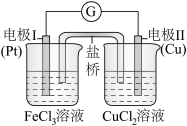

| A.氧化剂和还原剂必须直接接触才能发生反应 |
| B.电极Ⅱ上发生还原反应,作原电池的正极 |
| C.该原电池的总反应式为:2Fe3++Cu===Cu2++2Fe2+ |
| D.盐桥中装有含氯化钾的琼脂,K+移向负极区 |
您最近一年使用:0次
2017-08-19更新
|
1231次组卷
|
4卷引用:2018版化学(苏教版)高考总复习专题六课时跟踪训练--原电池 化学电源



