20. T℃下,向一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/×10-4mol·L-1 | 10.0 | 4.50 | c1 | 1.50 | 1.00 | 1.00 |
| c(CO)/×10-3mol·L-1 | 3.60 | 3.05 | c2 | 2.75 | 2.70 | 2.70 |
(1)则
c2合理的数值为
___(填字母)。
A.4.20 B.4.00 C.2.95 D.2.80
(2)将不同物质的量的H
2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H
2O(g)+CO(g)

CO
2(g)+H
2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所
需时间/min |
| H2O | CO | CO | H2 |
| Ⅰ | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| Ⅱ | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| Ⅲ | 900 | a | b | c | d | t |
若a=2,b=1,则c=
__,达到平衡时实验组Ⅱ中H
2O(g)和实验组Ⅲ中CO的转化率的关系为α
Ⅱ(H
2O)
___(填“<”“>”或“=”)α
Ⅲ(CO)。
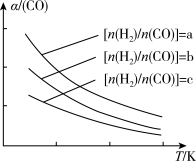
(3)二甲醚是清洁能源,用CO在催化剂存在下制备二甲醚的反应原理为2CO(g)+4H
2(g)

CH
3OCH
3(g)+H
2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比

的变化曲线如图所示。
①a、b、c按从大到小的顺序排序为
___。
②根据图象可以判断该反应为放热反应,理由是
___。
(4)氨气是工业制硝酸的主要原料。T℃时,NH
3和O
2可能发生如下反应:
①4NH
3(g)+5O
2(g)

4NO(g)+6H
2O(g) Δ
H=-907kJ·mol
-1②4NH
3(g)+3O
2(g)

2N
2(g)+6H
2O(g) Δ
H= -1269kJ·mol
-1其中②是副反应,若要减少副反应,提高NO的产率,最合理的措施是
__;T℃时N
2和O
2反应生成NO的热化学方程式为
__。