解题方法
1 . 燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是
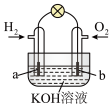
| A.a极是负极,该电极上发生氧化反应 |
| B.b极反应是O2+2H2O-4e-=4OH- |
| C.总反应方程式为2H2+O2=2H2O |
| D.若将H2改成CH4,则负极电极反应为:CH4-8e-+2H2O=CO2+8H+ |
您最近一年使用:0次
2022-10-05更新
|
649次组卷
|
4卷引用:四川省广元市八二一中学2021-2022学年高一下学期期中考试化学试题
四川省广元市八二一中学2021-2022学年高一下学期期中考试化学试题(已下线)专题06 化学反应与电能(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)江西省彭泽县第二高级中学2022-2023学年高一下学期5月期中考试化学试题(已下线)清单03 化学反应与能量(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
2 . 有A、B、C、D四种金属浸入稀H2SO4溶液中,用导线两两连接分别组成原电池。A、D相连,A为负极;A、B相连,电流由A经外电路流向B;C、D相连,C极上有大量气体产生。则这四种金属的活动性由强到弱的顺序为
| A.C>D>B>A | B.A>B>C>D | C.B>A>D>C | D.A>B>D>C |
您最近一年使用:0次
2022-10-01更新
|
585次组卷
|
7卷引用:四川省成都市郫都区2022-2023学年高一下学期4月期中化学试题
四川省成都市郫都区2022-2023学年高一下学期4月期中化学试题贵州省黔东南州从江县第一民族中学2021-2022学年高一下学期期中考试化学试题上海市奉贤区曙光中学2022-2023学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【期中考】【杭四吴山】【高中化学】【赵涛收集】甘肃省天水市第一中学2022-2023学年高一下学期5月期中考试化学试题上海市奉贤区致远高级中学2022-2023学年高一下学期期末教学评估化学试题(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
3 . 微型纽扣电池在现代生活中被广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O=Zn(OH)2+2Ag,其中一个电极反应式为Ag2O+H2O+2e-=2Ag+2OH-。
(1)负极材料为_______ ,正极材料为_______ 。
(2)电池工作时,电子由_______ (填“正极”或“负极”,下同)流向_______ ,溶液中的阳离子流向电池的_______ ,阴离子流向电池的_______ 。
(3)甲醇(CH3OH)燃料电池为绿色化学电源,在NaOH溶液为电解质溶液时的负极反应式为_______ ,正极反应式为_______ 。该电池工作时,外电路每流过1×103mole-,消耗标准状况下氧气_______ L。
(1)负极材料为
(2)电池工作时,电子由
(3)甲醇(CH3OH)燃料电池为绿色化学电源,在NaOH溶液为电解质溶液时的负极反应式为
您最近一年使用:0次
4 . 日常生活常用的干电池构造示意图如图。下列说法错误的是
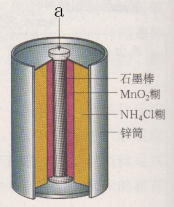

| A.电极a为正极,发生氧化反应 |
| B.电池使用过程中锌筒逐渐变薄 |
| C.负极的电极反应式为Zn-2e-=Zn2+ |
| D.电池工作时,MnO2得到电子被还原 |
您最近一年使用:0次
名校
解题方法
5 . 燃料电池是一种高效、环境友好的发电装置,某氢氧燃料电池的构造示意图如下,该电池工作时,下列说法正确的是
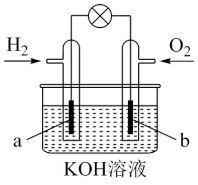

| A.O2在b电极上发生氧化反应 |
| B.电解质溶液中OH-向正极移动 |
| C.该装置实现了电能到化学能的转化 |
| D.电子从a电极沿外电路流向b电极 |
您最近一年使用:0次
2022-08-24更新
|
583次组卷
|
2卷引用:四川省凉山州宁南中学2021-2022学年高一下学期第二次月考化学试题
名校
解题方法
6 . 请根据所学知识,回答下列问题:
某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
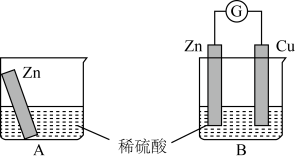
(1)B中Zn板是___________ 极,正极发生的电极反应是___________
(2)该小组同学反思原电池的原理,其中观点正确的是___________;
(3)在B中,当导线中有1 mol电子通过时,理论上的两极变化是___________。
(4)若将反应2Fe3++Cu=Cu2++2Fe2+设计成原电池,写出正极电极反应式___________ ;
(5)写出碱性氢氧燃料电池正极电极反应式___________
(6)写出酸性乙醇(C2H5OH)燃料电池负极电极反应式___________
(7)写出铜片和铝片插入浓硝酸溶液中的正极反应为:___________
某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
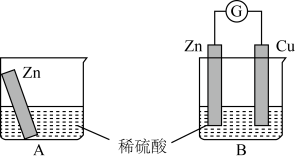
(1)B中Zn板是
(2)该小组同学反思原电池的原理,其中观点正确的是___________;
| A.原电池反应的过程中一定有电子转移 |
| B.电极一定不能参加反应 |
| C.原电池装置中的电子流向:负极→外线路→正极→电解质→负极 |
| D.氧化反应和还原反应可以拆开在两极发生 |
| A.锌片溶解32.5 g | B.锌片增重32.5 g |
| C.铜片上析出2 g H2 | D.铜片上析出1 mol H2 |
(5)写出碱性氢氧燃料电池正极电极反应式
(6)写出酸性乙醇(C2H5OH)燃料电池负极电极反应式
(7)写出铜片和铝片插入浓硝酸溶液中的正极反应为:
您最近一年使用:0次
2020高三·全国·专题练习
名校
解题方法
7 . 普通锌锰干电池的简图如图所示,它是用锌皮制成的锌筒作为电极,中央插一根石墨棒,石墨棒顶端加一铜帽。在石墨棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液。该电池工作时的总反应为Zn+2NH +2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
+2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
 +2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
+2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是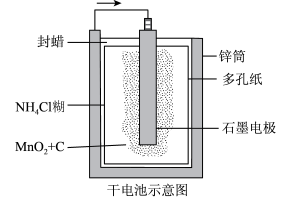
| A.当该电池电压逐渐下降后,利用电解原理能重新充电复原 |
B.电池负极反应为2MnO2+2NH +2e-=Mn2O3+2NH3+H2O +2e-=Mn2O3+2NH3+H2O |
| C.原电池工作时,电子从负极通过外电路流向正极 |
| D.外电路中每通过0.1 mol 电子,锌的质量理论上减少6.5 g |
您最近一年使用:0次
2023-05-13更新
|
289次组卷
|
10卷引用:四川省眉山市仁寿县2022-2023学年高一下学期5月期中联考化学试题
四川省眉山市仁寿县2022-2023学年高一下学期5月期中联考化学试题6.1.2 化学反应与电能 随堂练习(已下线)专题6.2 原电池 化学电源(讲)——2020年高考化学一轮复习讲练测(已下线)第四章 化学反应与电能(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)第一节 原电池 第2课时 化学电源河南省洛阳市宜阳县第一高级中学2022-2023学年高二上学期第五次能力达标测试化学试题辽宁省辽阳市第二高级中学2022-2023学年高二上学期12月月考化学试题新疆塔城地区塔城市2022-2023学年高二上学期11月期中考试化学试题陕西省渭南市白水中学2022-2023学年高二上学期12月月考化学试题河南省焦作市第十一中学2023-2024学年高二上学期12月份月考 化学试卷
解题方法
8 . 能源、资源问题是当前人类社会面临的一项重大课题。直接利用物质燃烧提供热能在当今社会仍然占很大比重,但存在利用率低的问题。燃料电池将能量转化效率比直接燃烧效率高,H2、CH4、CH3OH都是重要的能源物质。
(1)其中氢氧燃料电池是常见的燃料电池,如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
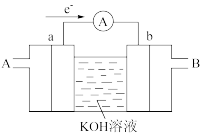
①使用时,空气从_____ 口通入(填“A”或“B”);负极是_____ (填“a”或“b”)。电流由_____ 流向_____ (填“a”或“b”)。其总反应方程式为_____ ,在碱性条件下,负极反应式为_____ 。
②假设使用的“燃料”是甲烷(酸性条件下),a极的电极反应为:_____ 。
(2)某同学设计如图的原电池,负极实验现象为_____ ,则正极的电极反应式为:_____ ,当导线中有3.01×1023个电子流过,溶液质量变化为_____ g。

(3)能把硫酸铜溶液改成氢氧化钠溶液吗_____ (填“能”或“不能”),为什么_____ 。
(1)其中氢氧燃料电池是常见的燃料电池,如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲烷(酸性条件下),a极的电极反应为:
(2)某同学设计如图的原电池,负极实验现象为

(3)能把硫酸铜溶液改成氢氧化钠溶液吗
您最近一年使用:0次
名校
9 . 高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是___________ 。
(2)放电时,正极发生___________ (填“氧化”或“还原”)反应。
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为___________ 。
(4)放电时,___________ (填“正”或“负”)极附近溶液的碱性增强。
 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:(1)高铁电池的负极材料是
(2)放电时,正极发生
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为
(4)放电时,
您最近一年使用:0次
2024-02-24更新
|
232次组卷
|
4卷引用:四川省江油中学2019-2020学年高一下学期开学考试化学试题
名校
解题方法
10 . 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是


A.Zn为正极,电极反应式为: |
B.电池工作时 向Cu电极移动 向Cu电极移动 |
| C.电子由Zn电极经稀硫酸溶液流向Cu电极 |
D.Zn电极质量每减少65g,则在该电极产生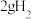 |
您最近一年使用:0次
2022-07-15更新
|
127次组卷
|
2卷引用:四川省凉山州2021-2022学年高一下学期期末考试化学试题



