名校
解题方法
1 . 随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具有重要意义。有学者想以如图所示装置用原电池原理将SO2转化为重要的化工原料。
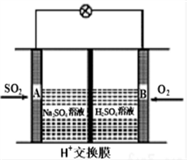
下列说法不正确的是

下列说法不正确的是
| A.溶液中H+的移动方向由A极到B极 |
| B.电池总反应方程式为:2SO2 + O2 + 2H2O = 2H2SO4 |
C.正极电极反应式为:SO2+ 2H2O-2e=SO +4H+ +4H+ |
| D.当有0.25mol SO2被吸收时,通过H+交换膜的H+的物质的量为0.5mol |
您最近一年使用:0次
2017-05-04更新
|
343次组卷
|
2卷引用:甘肃省嘉峪关市第一中学2021届高三下学期七模考试理综化学试题
名校
2 . 下列关于原电池的叙述中正确的是
| A.在镁、铝、稀NaOH溶液组成的原电池中,镁是负极,铝是正极 |
| B.在铁、铝、稀硫酸组成的原电池中,电子由铁片通过导线流向铝片 |
| C.在锌、铜、稀硫酸组成的原电池中,当电池工作时,硫酸根离子向正极移动 |
| D.在锌、铜、CuSO4溶液组成的原电池中,负极质量减轻,正极质量增加 |
您最近一年使用:0次
2016-12-09更新
|
490次组卷
|
5卷引用:2015-2016学年甘肃省会宁四中高一下学期期中考试化学试卷
3 . 原电池是将化学能转变为电能的装置,关于如图所示原电池的说法正确的是
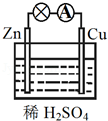

| A.Cu为负极,Zn为正极 |
| B.电子由铜片通过导线流向锌片 |
| C.正极反应式为Zn﹣2e﹣=Zn2+ |
| D.原电池的反应本质是氧化还原反应 |
您最近一年使用:0次
2016-12-09更新
|
259次组卷
|
3卷引用:甘肃省镇原县第二中学2021-2022学年高二上学期期中考试化学试题
名校
4 . 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是


| A.该电池的负极反应为BH4-+8OH--8e-=BO2-+6H2O |
| B.电池放电时Na+从b极区移向a极区 |
| C.每消耗3 mol H2O2,转移的电子为3 mol |
| D.电极a采用MnO2作电极材料 |
您最近一年使用:0次
2016-12-09更新
|
436次组卷
|
6卷引用:2016届甘肃省高三下学期3月高考诊断考试理综化学试卷
名校
5 . 一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( )
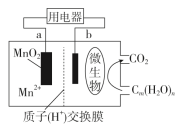

| A.电池工作时,电子由a流向b |
| B.微生物所在电极区放电时发生还原反应 |
| C.放电过程中,H+从正极区移向负极区 |
| D.正极反应式为:MnO2+4H++2e-=Mn2++2H2O |
您最近一年使用:0次
2016-12-09更新
|
1464次组卷
|
18卷引用:甘肃省张掖市高台县第一中学2018—2019学年高一下学期期中考试化学试题
甘肃省张掖市高台县第一中学2018—2019学年高一下学期期中考试化学试题2015届福建省漳州市高三3月质量检查化学试卷12015届福建省漳州市高三3月质量检查化学试卷2山东省淄博市淄川中学2018-2019学年高二6月月考化学试题云南省华宁一中2019-2020学年高二上学期开学考试化学试题云南省文山壮族苗族自治州广南县第二中学2018-2019学年高一下学期期中考试化学试题河北省承德市第一中学2019-2020学年高一下学期3月疫情期间直播课堂检测化学试题山西省晋中市和诚中学2019-2020学年高一3月月考化学试题黑龙江省哈尔滨市宾县第二中学2019-2020学年高二下学期期中考试化学试题四川省泸县第四中学2019-2020学年高一下学期第四学月考试化学试题四川省双流棠湖中学2020-2021学年高二上学期开学考试化学试题福建省福州市罗源第一中学2020-2021学年高二上学期10月月考化学试题(鲁科版2019)必修第二册 第2章 化学键 化学反应规律 第2节 化学反应与能量转化 第3课时 发展中的化学电源吉林省汪清县第六中学2020-2021学年高二上学期期末考试化学试题辽宁省沈阳市重点高中联合体2021-2022学年高三12月考试化学试题广东省梅州市兴宁市第一中学2021-2022学年高二下学期期中段考化学试题(已下线)题型19 微生物电池的应用(已下线)专题三 新型电池(练习)
14-15高二上·浙江温州·期末
6 . 根据下图,下列判断中正确的是
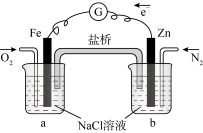

| A.烧杯a中的溶液pH升高 |
| B.烧杯a中发生的反应为2H2O+2e-=H2↑+2OH- |
| C.烧杯b中发生还原反应 |
| D.烧杯b中发生的反应为2Cl--2e-=Cl2↑ |
您最近一年使用:0次
2016-12-09更新
|
293次组卷
|
5卷引用:2014-2015甘肃省兰州一中高二上学期期末化学试卷
2014-2015甘肃省兰州一中高二上学期期末化学试卷(已下线)2013-2014学年浙江省温州市十校联合体高二上学期期末考试化学试卷2014-2015浙江省严州中学高二1月月考化学试卷(已下线)同步君 选修4 第4章 第4节 金属的电化学腐蚀与防护高中化学人教版 选修四 第四章 电化学基础 第四节 金属的电化学腐蚀与防护 金属的电化学腐蚀与防护
11-12高二上·甘肃兰州·期中
解题方法
7 . 烧过菜的铁锅未及时洗净,第二天便出现红棕色锈斑(该锈斑为Fe(OH)3失水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
(1)负极_____________________ ;
(2)正极_______________ ;
(3)离子方程式____________________ ;
(4)化学方程式______________________ .
(1)负极
(2)正极
(3)离子方程式
(4)化学方程式
您最近一年使用:0次
10-11高一下·甘肃天水·阶段练习
解题方法
8 . 有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1) A2B2的电子式为____________ 。
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。
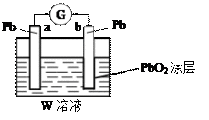
在b电极上发生的反应可表示为:PbO2+4H++SO +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________ 。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为____________________________________ 。
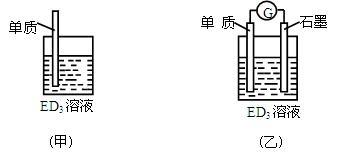
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池,则在该原电池工作时,石墨一极发生的反应可以表示为_____________________ 。比较甲、乙两图,说明石墨除形成闭合回路外所起的作用是_______________ 。
(1) A2B2的电子式为
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。

在b电极上发生的反应可表示为:PbO2+4H++SO
 +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为

(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池,则在该原电池工作时,石墨一极发生的反应可以表示为
您最近一年使用:0次
10-11高二上·甘肃天水·阶段练习
解题方法
9 . 人们应用原电池原理制作了多种电池,以满足不同的需要。在现代生活、生产和科学技术的发展中,电池发挥着越来越重要的作用。以下每小题中的电池即为广泛使用于日常生活、生产和科学技术等方面的实用电池,请根据题中提供的信息,填写空格。
(1)电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反应为:Ag2O+Zn+H2O=2Ag+Zn(OH)2。
①工作时电流从_____ 极流向_____ 极(两空均选填“Ag2O”或“Zn”)。
②电极反应式为:正极_____________ ,负极______________________ 。
(2)蓄电池在放电时起原电池作用,在充电时起电解池的作用。爱迪生蓄电池分别在充电和放电时发生的反应为:
①放电时,正极为________ 。正极的电极反应式为________________ 。
②该蓄电池中的电解质溶液应为________ (选填“酸性”或“碱性”)溶液。
(1)电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反应为:Ag2O+Zn+H2O=2Ag+Zn(OH)2。
①工作时电流从
②电极反应式为:正极
(2)蓄电池在放电时起原电池作用,在充电时起电解池的作用。爱迪生蓄电池分别在充电和放电时发生的反应为:

①放电时,正极为
②该蓄电池中的电解质溶液应为
您最近一年使用:0次
名校
解题方法
10 . 流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4===CuSO4+PbSO4+2H2O。下列说法不正确的是( )
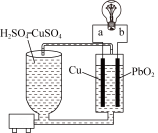

| A.a为负极,b为正极 |
| B.该电池工作时PbO2电极附近溶液的pH增大 |
| C.a极的电极反应为Cu-2e-===Cu2+ |
| D.调节电解质溶液的方法是补充CuSO4 |
您最近一年使用:0次
2016-11-15更新
|
1421次组卷
|
18卷引用:甘肃省兰州市第五十八中学2018-2019学年高二(理科)第一学期期末考试化学试题
甘肃省兰州市第五十八中学2018-2019学年高二(理科)第一学期期末考试化学试题2016-2017学年黑龙江大庆一中高二上10月月考化学卷2018-2019学年人教版高中化学选修四电化学基础章末综合测评题(四)云南省曲靖市富源县第六中学2019-2020学年高二上学期期末考试化学试题河南省鹤壁市高级中学2018-2019学年高一下学期精英对抗赛化学试题(已下线)1.2.2 化学电源 练习《新教材同步备课》(鲁科版选择性必修1)河北省邯郸市大名县第一中学2020-2021学年高二上学期9月月考化学试题黑龙江省大庆铁人中学2020-2021学年高二上学期第一次月考化学试题福建省连城县第一中学2020-2021学年高二上学期第一次月考化学试题福建省三明市泰宁第一中学2020-2021学年高二上学期学分认定暨第一次阶段考试化学试题河北省武安市第三中学2021届高三上学期期中考试化学试题海南省万宁市北京师范大学万宁附属中学2020-2021学年高二上学期第一次月考化学试题河南省驻马店市2020-2021学年高二上学期期终考试化学试题重庆实验中学2020-2021学年高二上学期第二阶段考试化学试题宁夏平罗中学2021-2022学年高三上学期第一次月考化学试题(已下线)第12练 原电池原理及其应用-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)福建省福州第三中学2021-2022学年高三上学期第六次质量检测化学试题陕西省西安交通大学附属中学2023-2024年高二上学期第一次月考化学试题



