名校
解题方法
1 . 甲醇(化学式: )是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
)是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知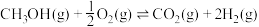 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是___________ (填字母)。 转变成
转变成 的过程是一个吸收能量的过程
的过程是一个吸收能量的过程
b.化学变化不仅有新物质生成,同时也一定有能量变化
c. 的生成速率与
的生成速率与 的消耗速率之比为
的消耗速率之比为
d.1mol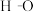 键断裂的同时2mol
键断裂的同时2mol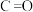 键断裂,则反应达最大限度
键断裂,则反应达最大限度
(2)某温度下,将5mol 和2mol
和2mol 充入2L的密闭容器中,经过4min反应达到平衡,测得
充入2L的密闭容器中,经过4min反应达到平衡,测得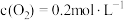 ,4min内平均反应速率
,4min内平均反应速率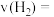
___________ ,则 的转化率为
的转化率为___________ 。
(3) 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为
燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为___________ ,下列说法正确的是___________ (填序号)。
b.电池放电时,电解质溶液的碱性逐渐减弱
c.电池放电时每消耗6.4g 转移1.2mol电子
转移1.2mol电子
d.电池放电时 向a电极移动
向a电极移动
(4)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别加入甲醇和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导
固体,它在高温下能传导 。则c电极的名称为
。则c电极的名称为___________ (填“正极”或“负极”),d电极上的电极反应式为___________ 。
 )是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
)是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。(1)已知
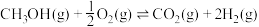 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是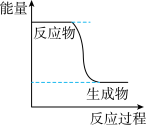
 转变成
转变成 的过程是一个吸收能量的过程
的过程是一个吸收能量的过程b.化学变化不仅有新物质生成,同时也一定有能量变化
c.
 的生成速率与
的生成速率与 的消耗速率之比为
的消耗速率之比为
d.1mol
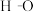 键断裂的同时2mol
键断裂的同时2mol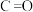 键断裂,则反应达最大限度
键断裂,则反应达最大限度(2)某温度下,将5mol
 和2mol
和2mol 充入2L的密闭容器中,经过4min反应达到平衡,测得
充入2L的密闭容器中,经过4min反应达到平衡,测得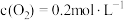 ,4min内平均反应速率
,4min内平均反应速率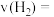
 的转化率为
的转化率为(3)
 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为
燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为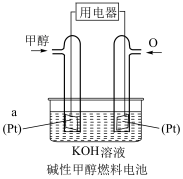
b.电池放电时,电解质溶液的碱性逐渐减弱
c.电池放电时每消耗6.4g
 转移1.2mol电子
转移1.2mol电子d.电池放电时
 向a电极移动
向a电极移动(4)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别加入甲醇和空气,其中固体电解质是掺杂了
 的
的 固体,它在高温下能传导
固体,它在高温下能传导 。则c电极的名称为
。则c电极的名称为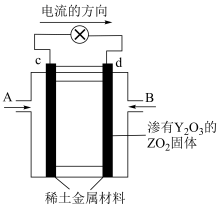
您最近一年使用:0次
解题方法
2 . 回答下列问题。
(1)补齐物质及其用途的连线。

________________ 。
(2)化学电池的发明,是贮能和供能技术的巨大进步。
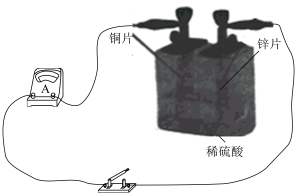
①上图所示装置中, 片作
片作___________ (填“正极”或“负极”), 片上发生反应的电极反应式为
片上发生反应的电极反应式为___________ 。
②上图所示装置可将___________ (写离子反应方程式)反应释放的能量直接转变为电能;能证明产生电能的实验现象是___________ 。
(3)镁、石墨、海水溶解氧可构成原电池,为水下小功率设备长时间供电,其结构示意图如下图所示。该原电池的总反应为: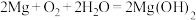 。
。
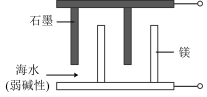
下列说法正确的是___________ (填字母)。
a.石墨是电池的负极
b. 发生氧化反应
发生氧化反应
c.当有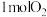 参与反应时转移电子
参与反应时转移电子
(1)补齐物质及其用途的连线。

(2)化学电池的发明,是贮能和供能技术的巨大进步。

①上图所示装置中,
 片作
片作 片上发生反应的电极反应式为
片上发生反应的电极反应式为②上图所示装置可将
(3)镁、石墨、海水溶解氧可构成原电池,为水下小功率设备长时间供电,其结构示意图如下图所示。该原电池的总反应为:
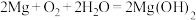 。
。
下列说法正确的是
a.石墨是电池的负极
b.
 发生氧化反应
发生氧化反应c.当有
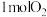 参与反应时转移电子
参与反应时转移电子
您最近一年使用:0次
名校
解题方法
3 . 电池的种类很多,在生活中有广泛的用途。
Ⅰ.其中纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O===2Ag+Zn(OH)2。
(1)其正极的电极反应式:_________________________________ ,工作时电池电解质溶液的碱性_______ (填“增强”、“减弱”或“不变”)。
Ⅱ.固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
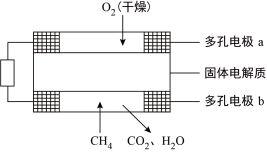
(2) a电极为电源的_______ 极,固体电解质中的阳离子向_______ 极移动;
(3) b电极的电极反应式为:_______________________________________ ;
(4)电池的总反应方程式为:______________________________________ ;
当电路中有2mol电子转移时,理论上负极消耗的标况下气体体积是______________ L。
Ⅰ.其中纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O===2Ag+Zn(OH)2。
(1)其正极的电极反应式:
Ⅱ.固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。

(2) a电极为电源的
(3) b电极的电极反应式为:
(4)电池的总反应方程式为:
当电路中有2mol电子转移时,理论上负极消耗的标况下气体体积是
您最近一年使用:0次
4 . 金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是
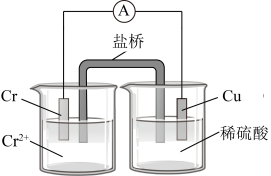

| A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液 |
| B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池 |
| C.此过程中H+得电子,发生氧化反应 |
| D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中 |
您最近一年使用:0次
2016-12-06更新
|
1733次组卷
|
5卷引用:【百强校】2016-2017学年浙江省温州中学高二上期中化学卷(带解析)
(已下线)【百强校】2016-2017学年浙江省温州中学高二上期中化学卷(带解析)甘肃省临夏甘南两地联考2022-2023学年高二上学期12月期中考试化学试题浙江省丽水四校2019-2020学年高三10月联考化学试题黑龙江省七台河市第一中学2019-2020学年高一下学期期末考试化学试题甘肃省嘉峪关市等3地2022-2023学年高二上学期12月期末化学试题
名校
解题方法
5 . 某研究小组提出了一种新的设想:利用原电池原理,设计一种H2、Cl2燃料电池,原电池总反应为:H2+Cl2=2HCl,在对外提供电能的同时还可得到工业上具有重要用途的较浓的盐酸。他们设计的原电池装置如下,其中两个电极均为多孔铂电极。下列有关叙述不正确的是
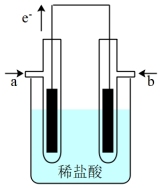

| A.a为负极,通入的气体为氢气 |
| B.正极的电极反应式为:Cl2+2e-=2Cl- |
| C.电流由b极流出,经外电路到a极 |
| D.原电池内部,H+移向负极,Cl-移向正极 |
您最近一年使用:0次
2016-12-09更新
|
296次组卷
|
2卷引用:2015届湖北省襄阳四中等高三下学期期中四校联考化学试卷



