1 . 某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如表:
试根据表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)______ (填“相同”或“不相同”)。
(2)对实验3完成下列填空:
①铝为_____ 极,电极反应式:______ 。
②石墨为_____ 极,电极反应式:______ 。
③电池总反应方程式:______ 。
(3)实验4中铝作______ ,理由是______ 。写出铝电极的电极反应式:______ 。
(4)解释实验5中电流计指针偏向铝的原因:______ 。
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极(正极或负极)
(2)对实验3完成下列填空:
①铝为
②石墨为
③电池总反应方程式:
(3)实验4中铝作
(4)解释实验5中电流计指针偏向铝的原因:
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:
您最近一年使用:0次
2 . 高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是___________ 。
(2)放电时,正极发生___________ (填“氧化”或“还原”)反应。
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为___________ 。
(4)放电时,___________ (填“正”或“负”)极附近溶液的碱性增强。
 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:(1)高铁电池的负极材料是
(2)放电时,正极发生
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为
(4)放电时,
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.“绿水青山就是金山银山”,利用电池原理治理污染是今后科研的重要课题。
(1)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化——化学耦合分解硫化氢的研究中获得新进展,相关装置如图所示。

①a为_____ 极。
②请用离子方程式分析H2S气体去除的原理:___________ 。
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和 :
: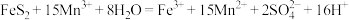 。已知:两电极为完全相同的惰性电极。
。已知:两电极为完全相同的惰性电极。
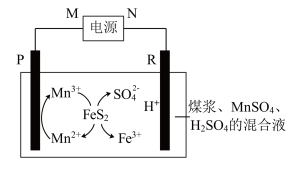
(2)电解池刚开始工作时,R上的电极反应式为_____ 。
(3)若电路中转移 电子,则此时消耗的
电子,则此时消耗的 的质量为
的质量为_____ g(不考虑其他反应,下同),产生的气体的体积为______ L(已换算成标准状况)。
(4)电解过程中,混合溶液中的pH将_____ (填“变大”“变小”或“不变”),原因是___________ 。
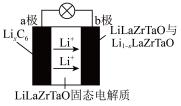
(5)Garnet型固态电解质被认为是锂离子电池最佳性能固态电解质。LiLaZrTaO材料是目前能达到最高电导率的Garnet型电解质。某Garnet型可充电锂离子电池放电时工作原理如图所示,若用该电池作为电解脱硫的外加电源,则b极应接_____ (填“M”或“N”)极。
(1)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化——化学耦合分解硫化氢的研究中获得新进展,相关装置如图所示。

①a为
②请用离子方程式分析H2S气体去除的原理:
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和
 :
: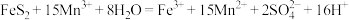 。已知:两电极为完全相同的惰性电极。
。已知:两电极为完全相同的惰性电极。
(2)电解池刚开始工作时,R上的电极反应式为
(3)若电路中转移
 电子,则此时消耗的
电子,则此时消耗的 的质量为
的质量为(4)电解过程中,混合溶液中的pH将
(5)Garnet型固态电解质被认为是锂离子电池最佳性能固态电解质。LiLaZrTaO材料是目前能达到最高电导率的Garnet型电解质。某Garnet型可充电锂离子电池放电时工作原理如图所示,若用该电池作为电解脱硫的外加电源,则b极应接

您最近一年使用:0次
4 . 化学电源在生产生活中有着广泛的应用,回答下列问题:
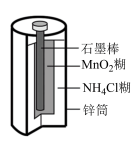
(1)常见的锌锰干电池其构造如图所示。常见的锌锰干电池属于___________ (填“一次电池”或“二次电池”),从氧化还原反应的角度分析,锌筒上发生的反应属于_________ 反应。
(2)为了探究化学反应中的能量变化,某同学设计了如图中的两个实验装置(装置中除连接的铜棒不同外,其他均相同),下列有关实验现象的说法正确的是_________ (填标号)。
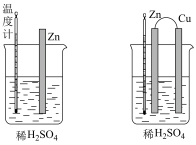
A.两装置温度计的示数相等,且均高于室温
B.两装置的气泡均产生于锌棒表面
C.连接铜棒的装置产生气体的速度快
(3)有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸溶液中,乙同学将电极放入等浓度的 溶液中,如图所示。
溶液中,如图所示。
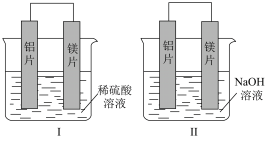
①装置Ⅰ中放电时氢离子向_________ (填“镁片”或“铝片”)移动。写出装置Ⅰ中正极的电极反应式:_________ 。
②装置Ⅱ中铝片为_________ 极,写出该电极的电极反应式_________ 。
③如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的结论。依据该实验得出的下列结论中,正确的有_________ (填标号)。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
(1)常见的锌锰干电池其构造如图所示。常见的锌锰干电池属于

(2)为了探究化学反应中的能量变化,某同学设计了如图中的两个实验装置(装置中除连接的铜棒不同外,其他均相同),下列有关实验现象的说法正确的是

A.两装置温度计的示数相等,且均高于室温
B.两装置的气泡均产生于锌棒表面
C.连接铜棒的装置产生气体的速度快
(3)有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸溶液中,乙同学将电极放入等浓度的
 溶液中,如图所示。
溶液中,如图所示。
①装置Ⅰ中放电时氢离子向
②装置Ⅱ中铝片为
③如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的结论。依据该实验得出的下列结论中,正确的有
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
您最近一年使用:0次
名校
解题方法
5 . 化学变化过程中均存在物质变化与能量变化。
(1)某化学兴趣小组进行如图所示实验装置,以验证此结论。
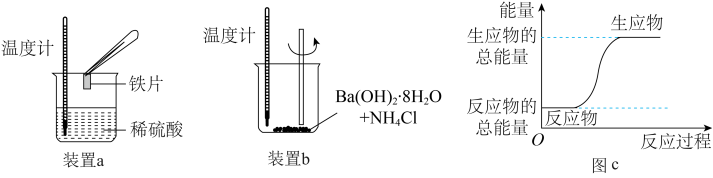
请回答下列问题:
①进行实验时,装置a中溶液变色,装置b中能闻到___________ ;装置a中温度计中水银液面变化是___________ (填“升高”或“降低”,下同);装置b中温度计中水银液面变化是___________ 。
②下列化学反应中的能量变化关系与图c相符合的是___________ 。
A.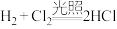
B.天然气的燃烧
C.
D.
(2)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,若反应生成2 mol NO气体(选“吸收”或“放出”)___________ kJ热量,该反应的反应物的总能量___________ (填“大于”、“等于”或“小于”)生成物的总能量。

(3)有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入2 mol/L H2SO4溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如下图所示。
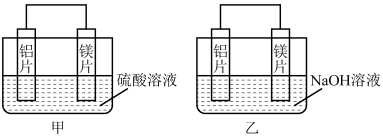
①甲池中,镁片上发生___________ (填“氧化”或“还原”)反应。
②乙池中铝片为___________ 极,写出铝电极的电极反应式:___________ 。
(1)某化学兴趣小组进行如图所示实验装置,以验证此结论。

请回答下列问题:
①进行实验时,装置a中溶液变色,装置b中能闻到
②下列化学反应中的能量变化关系与图c相符合的是
A.
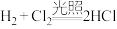
B.天然气的燃烧
C.

D.

(2)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,若反应生成2 mol NO气体(选“吸收”或“放出”)

(3)有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入2 mol/L H2SO4溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如下图所示。

①甲池中,镁片上发生
②乙池中铝片为
您最近一年使用:0次
名校
6 . Ⅰ.给你提供纯锌、纯铜片和500mL0.2mol·L-1的H2SO4溶液、导线、1000mL量筒。试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。
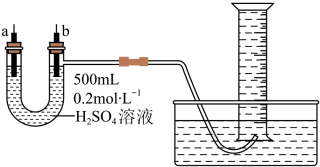
(1)如图所示,装置气密性良好,且1000mL量筒中已充满了水,则开始实验时,首先要_______ 。
(2)a电极材料为_______ ;b电极材料为_______ ,b电极反应式为_______ 。
(3)当量筒中收集672mL气体时(已折算到标准状况下),通过导线的电子的物质的量为_______ 。
Ⅱ.某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
(4)则A极是电池的_______ 极;电子从该极_______ (填“流入”或“流出”)。

(1)如图所示,装置气密性良好,且1000mL量筒中已充满了水,则开始实验时,首先要
(2)a电极材料为
(3)当量筒中收集672mL气体时(已折算到标准状况下),通过导线的电子的物质的量为
Ⅱ.某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
(4)则A极是电池的
您最近一年使用:0次
2023-07-29更新
|
44次组卷
|
2卷引用:云南省龙陵县第一中学2022-2023学年高一下学期期末考试化学试题
解题方法
7 . 根据原电池原理,结合如图所示装置图,按要求解答问题:

(1)若X为 ,Y为稀硫酸溶液,则X为
,Y为稀硫酸溶液,则X为_______ (填电极名称),X极电极反应式为_______ ;铜电极的名称是_______ ,溶液中的 移向
移向_______ (填“ ”或“X”)电极。
”或“X”)电极。
(2)若X为 ,Y为硫酸铜溶液,则铜电极的名称是
,Y为硫酸铜溶液,则铜电极的名称是_______ ,铜电极反应式为_______ 。

(1)若X为
 ,Y为稀硫酸溶液,则X为
,Y为稀硫酸溶液,则X为 移向
移向 ”或“X”)电极。
”或“X”)电极。(2)若X为
 ,Y为硫酸铜溶液,则铜电极的名称是
,Y为硫酸铜溶液,则铜电极的名称是
您最近一年使用:0次
名校
解题方法
8 . 燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。
(1)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
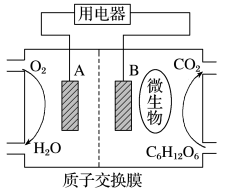
①A为生物燃料电池的_______ (填“正”或“负”)极。
②正极反应式为_______ 。
③放电过程中, 由
由_______ 极区向_______ 极区迁移(填“正”或“负”)。
④在电池反应中,每消耗 氧气,理论上生成标准状况下二氧化碳的体积是
氧气,理论上生成标准状况下二氧化碳的体积是_______ 。
(2)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇一氧化钠,其中 可以在固体介质
可以在固体介质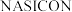 中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。
中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。

①工作时, 由电极
由电极_______ 向电极_______ 移动(填“a”或b”);
②电子由电极_______ 通过传感器流向电极_______ (填“a”或b”)。
(1)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的
②正极反应式为
③放电过程中,
 由
由④在电池反应中,每消耗
 氧气,理论上生成标准状况下二氧化碳的体积是
氧气,理论上生成标准状况下二氧化碳的体积是(2)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇一氧化钠,其中
 可以在固体介质
可以在固体介质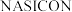 中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。
中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。
①工作时,
 由电极
由电极②电子由电极
您最近一年使用:0次
2022-05-04更新
|
231次组卷
|
3卷引用:云南省楚雄第一中学2022-2023学年高一下学期期末考试化学试题



