名校
解题方法
1 . 有关电化学知识的描述正确的是

A.反应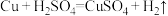 可设计成原电池 可设计成原电池 |
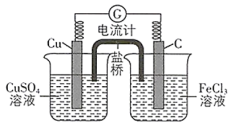
B.利用 ,可设计如图所示原电池装置,盐桥内 ,可设计如图所示原电池装置,盐桥内 向 向 溶液移动 溶液移动 |
C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中组成原电池,铁作负极,铜作正极,其负极反应式为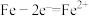 |
D.由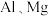 与氢氧化钠溶液组成的原电池,其负极反应式为 与氢氧化钠溶液组成的原电池,其负极反应式为 |
您最近一年使用:0次
2020-09-12更新
|
1019次组卷
|
11卷引用:【校级联考】山西省陵川第一中学、高平一中、阳城一中2018-2019学年高二上学期第三次月考化学试题
【校级联考】山西省陵川第一中学、高平一中、阳城一中2018-2019学年高二上学期第三次月考化学试题【校级联考】福建省福州八县一中2018-2019学年高二上学期期中考试化学试题【校级联考】天津市七校(静海一中、宝坻一中、杨村一中等)2018-2019学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 化学能转化为电能——电池 课时1 原电池的工作原理福建省泰宁第一中学2018-2019学年高二上学期第二阶段考试化学(理)试题高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 课时1 原电池的工作原理人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第一节 原电池 教材帮选择性必修1专题1第二单元 课时1 原电池的工作原理河北省衡水市第十四中学2021-2022学年高二上学期二调考试化学试题辽宁省辽河油田第二高级中学2022-2023学年高二上学期期末考试化学试题1.2.1原电池的工作原理 课后
解题方法
2 . 如图是锌和铜形成的原电池,某实验兴趣小组做完实验后,在读书卡片上写下了一些实验后的记录:①Zn为阳极,Cu为阴极;②H+向负极移动;③电子流动方向Zn→Cu;④Cu极有H2产生;⑤若有1mol电子流过导线,则产生H2为0.5mol;⑥正极电子反应式:Zn-2e-=Zn2+;其中描述合理的是


| A.①②③ | B.③④⑤ | C.④⑤⑥ | D.②③④ |
您最近一年使用:0次
解题方法
3 . 关于铜锌原电池(稀硫酸作电解质溶液)的叙述正确的是( )
| A.铜是负极,铜片上有气泡产生 | B.电流从锌片经导线流向铜片 |
| C.H+在铜片表面被还原 | D.铜片质量逐渐减小 |
您最近一年使用:0次
2020-07-14更新
|
248次组卷
|
2卷引用:山西省太原市第二十一中学校2019-2020学年高二会考模拟化学试题
4 . 熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为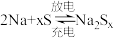 (x=5~3,难溶于熔融硫),下列说法
(x=5~3,难溶于熔融硫),下列说法错误 的是
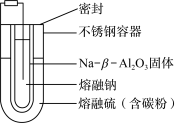
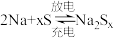 (x=5~3,难溶于熔融硫),下列说法
(x=5~3,难溶于熔融硫),下列说法
A.Na2S4的电子式为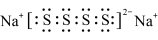 |
B.放电时正极反应为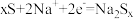 |
| C.Na和Na2Sx分别为电池的负极和正极 |
D.该电池是以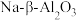 为隔膜的二次电池 为隔膜的二次电池 |
您最近一年使用:0次
2020-07-11更新
|
8295次组卷
|
39卷引用:山西大学附属中学2020-2021学年高二上学期8月模块诊断化学试题
山西大学附属中学2020-2021学年高二上学期8月模块诊断化学试题四川省成都市新津中学高2020-2021学年高二下学期4月月考试题选择性必修1(SJ)专题1专题培优专练选择性必修1 专题1 素养检测河北省张家口市第一中学2020-2021学年高二上学期10月月考(衔接班)化学 试题河北正定中学2020-2021学年高二上学期开学考试化学试题河南省信阳高级中学2021-2022学年高二上学期9月月考化学试题山东省文登第一中学2022-2023学年高二上学期1月期末考试化学试题辽宁省朝阳市建平县建平县实验中学2023-2024学年高二上学期开学考试化学试题2020年天津卷化学高考试题(已下线)专题08 电化学及其应用-2020年高考真题和模拟题化学分项汇编(已下线)小题必刷02 常见化学用语——2021年高考化学一轮复习小题必刷(通用版)(已下线)易错09 电化学基础-备战2021年高考化学一轮复习易错题(已下线)专题讲座(六)新型电源及电极反应式的书写(精讲)——2021年高考化学一轮复习讲练测(已下线)小题必刷25 原电池及化学电源——2021年高考化学一轮复习小题必刷(通用版本)(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)热点9 化学能与电能-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)小题18 可充电电池装置 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)难点2 电极反应式的书写-2021年高考化学专练【热点·重点·难点】辽宁省沈阳市五校2020-2021学年高一6月联考化学试题(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第16讲 原电池 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(四)新型电源及电极反应式的书写 (讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)2020年天津卷化学高考真题变式题1-12(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习山东省烟台市第二中学2021-2022学年高一下学期4月月考化学试题(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第16讲 原电池 新型电源 (练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)【知识图鉴】单元讲练测必修第二册第六单元03巩固练(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第六章 化学反应与能量 第35讲 原电池 化学电源(已下线)题型104 二次电池(已下线)专题12 电化学的综合应用
9-10高一下·河北衡水·期中
名校
解题方法
5 . 人造地球卫星上使用的一种高能电池(银锌蓄电池),其电池的电极反应式为:Zn+2OH--2e- =ZnO+H2O,Ag2O+H2O+2e- =2Ag+2OH-。据此判断氧化银是
| A.正极,被还原 | B.负极,被氧化 |
| C.正极,被氧化 | D.负极,被还原 |
您最近一年使用:0次
2020-06-18更新
|
788次组卷
|
82卷引用:2015-2016学年山西省大同一中高二上期末考试化学试卷
2015-2016学年山西省大同一中高二上期末考试化学试卷(已下线)2010-2011学年广西北海市合浦县教研室高二上学期期末考试化学试卷(已下线)2011-2012学年山东省济南外国语学校高二上学期期中考试化学(文)试卷(已下线)2011-2012学年山东临清三中高二上学期学分认定测试化学试卷(已下线)2011-2012学年贵州省湄潭中学高二上学期期末考试化学试卷(已下线)2012-2013学年吉林省实验中学高二上学期期末考试化学试卷(已下线)2013-2014湖南省衡南县高二下学期期末考试化学试卷2015-2016学年黑龙江大庆铁人中学高二上9月考化学试卷湖南省2016-2017学年高二普通高中学业水平考试模拟二化学试题福建省长泰县第一中学2017-2018学年高二上学期期中考试(理)化学试题河北省黄骅中学2018-2019学年高二上学期第二次月考化学试题【校级联考】江苏省常州“教学研究合作联盟”2018-2019学年高二下学期期中考试化学试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(学考)试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(选考)试题(已下线)江苏省如皋市2019-2020学年高二下学期第二次月考化学试题四川省雅安市2019-2020学年高二下学期期末考试化学试题重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题吉林省吉林市江城中学2020-2021学年高二上学期期中考试化学(理)试题云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题四川省雅安市名山区第三中学2023-2024学年高二12月月考化学试题(已下线)2009—2010学年河北冀州中学高一下学期期中考试化学卷(已下线)09-10年深圳高中高一下学期期末测试化学卷(已下线)2010年黑龙江省牡丹江一中高一下学期期末测试化学(已下线)2010年内蒙古通辽一中高一下学期期末考试化学试题(已下线)2010—2011学年辽宁省大连协作体高一4月月考化学试卷(已下线)2010—2011学年安徽蚌埠二中第二学期高一期中考试化学试卷(已下线)2010-2011学年甘肃省张掖中学高一下学期期中考试化学试卷(已下线)2010-2011学年河南省许昌市高一下学期四校期中联考化学试卷(已下线)2011-2012学年浙江省衢州一中高一下学期期中检测化学试卷(已下线)2011-2012学年贵州省湄潭中学高一下学期期中考试化学试卷 (已下线)2011-2012年江苏南通小海中学高一下学期期中考试化学试卷(已下线)2011-2012年湖南湘潭等四县一中高一下学期期中联考化学试卷(已下线)2011-2012学年广东省罗定市高一下学期期中质检理综化学试卷(已下线)2011-2012学年陕西省岐山县高一下学期期中考试化学试卷(已下线)2011-2012学年陕西省西安一中高一下学期期末考试化学试卷2014-2015浙江省杭州地区七校高一下学期期中联考化学试卷2014-2015陕西省西安市一中高一下学期期中化学试卷2014-2015学年安徽省涡阳四中高一下第二次质检化学试卷2015-2016学年陕西省黄陵中学高一下学期期中考试化学试卷2015-2016学年福建省清流一中高一实验班下第三段测化学试卷2015-2016学年河北省沧州市黄骅中学高一下期中化学试卷吉林省东北师范大学附属中学净月实验学校2016-2017学年高一下学期期中考试化学试题吉林省吉林油田实验中学2016-2017学年高一下学期期中考试化学试题湖北省沙市中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2017-2018学年高一下学期第二次6月月考化学试题宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题浙江省慈溪市三山高级中学2018-2019学年高一下学期第一次月考化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一下学期期中考试化学试题【校级联考】吉林省长春市九台区师范高中、实验高中2018-2019学年高一下学期期中考试化学试题广东省江门市第二中学2018-2019学年高一5月月考化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高一下学期期中考试化学试题(宾县用卷)新疆兵团八师一四三团一中2018-2019学年高一下学期期中考试化学试题黑龙江省龙东南联合体2018-2019学年高一下学期期末考试化学试题2020届高三化学化学二轮复习——新型电池基础练习【精编24题】河南省新乡市卫辉高中2019-2020学年高一下学期第一次调研考试化学试题甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期中考试化学试题湖南省常德市桃花源一中2019-2020学年高一下学期期中考试化学试题黑龙江省鸡西市鸡东县第二中学2019-2020学年高一下学期线上考试化学试题四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题辽宁省营口市第二高级中学2018-2019学年高一下学期第一次月考化学试题湖北省宜昌市长阳县第一高级中学2019-2020高一下学期期中考试化学试题浙江省金华市曙光学校2019-2020学年高一下学期第一次月考化学试题四川省遂宁市船山区第二中学校2019-2020学年高一下学期期中考试化学试题江苏省泰州中学2019-2020学年高一下学期期中考试化学试题安徽省桐城市第八中学2019-2020学年高一下学期期中考试化学试题贵州省兴仁市凤凰中学2019-2020学年高一下学期第一次月考化学试题广东省东莞市东华中学2019-2020学年高一下学期期末模拟化学试题安徽省安庆市第一中学2019-2020学年高一下学期月考化学试题甘肃省武威市第八中学2019-2020学年高一下学期期末考试化学试题湖南省衡阳市衡东县欧阳遇实验中学2019-2020学年高一上学期期末考试化学试题河南省漯河市临颍县南街高级中学2020-2021学年高一10月质量检测化学试题北京市第四十三中学2020-2021学年高一下学期第一次月考化学试题北京市丰台第八中学2020-2021学年高一下学期期中考试化学试题广西钦州市第四中学2020-2021学年高一下学期4月月考化学试题2甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(文)试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题陕西省宝鸡市金台区2021-2022学年高一下学期期中考试化学试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高一下学期期中考试(会考)化学试题北京师范大学附属中学2022-2023学年高一下学期期中考试化学试题海南省海口市长流中学2022-2023学年高一下学期期中考试化学试题A卷北京市第三中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
6 . 科学家研究利用如图装置对天然气进行脱硫,将硫由化合态转化成游离态,减少对环境的污染。已知甲、乙池中发生的反应如图所示。下列说法正确的是( )
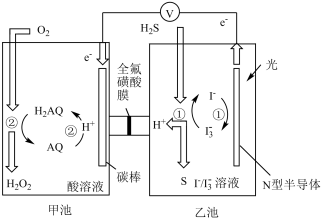

| A.全氟磺酸膜为阳离子交换膜,H+从甲池移向乙池,乙池溶液的pH变小 |
| B.电路中每转移2mol电子,甲池溶液质量增加32g |
| C.N型半导体为负极,发生的电极反应式为H2S+I3-=3I-+S↓+2H+ |
| D.甲池中碳棒上发生的电极反应为AQ+2H++2e-=H2AQ |
您最近一年使用:0次
2020-06-09更新
|
565次组卷
|
4卷引用:山西省长治市第二中学校2020-2021学年高二下学期期中考试化学试题
山西省长治市第二中学校2020-2021学年高二下学期期中考试化学试题甘肃省兰州市2020届高三诊断考试理科综合化学试题(已下线)【南昌新东方】9.2020年11月江西南昌三中高三上学期期中化学河北省正定中学2022-2023学年高一下学期第二次月考化学试题
10-11高三下·广东·期中
名校
7 . 将铝片和铜片用导线相连,一组插入浓HNO3溶液中,一组插入稀NaOH溶液中,分别形成了原电池,则在这两个原电池中,正极分别为( )
| A.铜片、铝片 | B.铝片、铜片 | C.铝片、铝片 | D.铜片、铜片 |
您最近一年使用:0次
2020-06-03更新
|
138次组卷
|
17卷引用:山西省应县第一中学校2019-2020学年高二上学期第四次月考化学试题
山西省应县第一中学校2019-2020学年高二上学期第四次月考化学试题(已下线)2010-2011学年黑龙江省哈六中高二下学期期中考试化学试卷(已下线)2011-2012学年吉林省长春外国语学校高二上学期期末考试化学试卷陕西省西安市高新一中2016-2017学年高二上学期第一次月考化学试题广西蒙山县第一中学2017-2018学年高二上学期期末考试化学试题宁夏回族自治区中卫市中宁县中宁中学2019-2020学年高二下学期阶段测试化学试题河北省石家庄市藁城区第一中学2019-2020学年高二上学期第三次月考化学试题新疆博尔塔拉蒙古自治州蒙古中学2020-2021学年高二下学期期中考试化学试题 黑龙江省大庆市东风中学2022-2023学年高二10月月考化学试题甘肃省民勤县第四中学2021-2022学年高二上学期期中考试化学试题(已下线)2010-2011学年广东省龙山中学高一下学期期中考试化学试卷(已下线)2011-2012学年黑龙江海林市高级中学高一下学期期中考试化学试卷 (已下线)湖北省仙桃市毛嘴高中2012-2013学年高一上学期学业水平监测化学试卷2015-2016学年安徽省安庆市一中高一下学期期中化学试卷新疆奎屯市第一高级中学2018-2019学年高一下学期第一次月考化学试题河南省信阳市商城县上石桥高中2019-2020学年高一下学期期中考试化学试题(鲁科版2019)必修第二册 第2章 化学键 化学反应规律 学科素养提升
名校
解题方法
8 . 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法正确的是( )
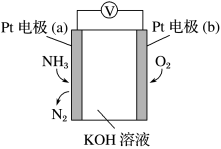

| A.O2在电极b上发生氧化反应 |
| B.溶液中OH-向电极b移动 |
| C.反应消耗的NH3与O2的物质的量之比为4:3 |
| D.正极的电极反应式为2NH3-6e-+6OH-=N2+6H2O |
您最近一年使用:0次
2020-05-28更新
|
669次组卷
|
11卷引用:山西省实验中学2021-2022学年高二下学期开学分班素质测试化学试题
山西省实验中学2021-2022学年高二下学期开学分班素质测试化学试题山西省实验中学2021-2022学年高二上学期开学考试化学试题(已下线)第05练 化学能与热能-2020年【衔接教材·暑假作业】新高二化学(人教版)江苏省扬州中学2020-2021学年高二上学期开学检测化学试题安徽省滁州市定远县民族中学2021-2022学年高二上学期9月质量检测化学试题江苏省泰州中学2019-2020学年高一下学期期中考试化学试题吉林江城中学2020-2021学年高一下学期期末考试化学试题广东省广州市玉岩中学2020-2021学年高一下学期期中考试化学试题江西省赣州市信丰县第一中学2021-2022学年高一下学期期中考试化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)广东省茂名市第一中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
9 . 2008年10月8日,瑞典皇家科学院宣布美籍华裔科学家钱永健获得2008年度诺贝尔化学奖。少年时代,他就对化学产生了浓厚的兴趣。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获具有“少年诺贝尔奖”之称的著名奖项。下列说法正确的是( )
| A.金属腐蚀就是金属失去电子被还原的过程 |
| B.将水库中的水闸(钢板)与外加直接电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
| C.由原电池原理知所有的合金都比纯金属更易被腐蚀 |
| D.铜板上的铁铆钉处在潮湿的空气中发生:Fe-3e-═Fe3+,从而形成铁锈,但此过程铜不被腐蚀 |
您最近一年使用:0次
名校
解题方法
10 . 如图所示的原电池装置,X、Y为两个电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列叙述正确的是
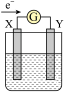

| A.外电路中的电流方向为:X→外电路→Y |
| B.若两个电极分别为Zn和碳棒,则X为碳棒,Y为Zn |
| C.若两个电极都是金属,则它们的活动性为X>Y |
| D.X极上发生的是还原反应,Y极上发生的是氧化反应 |
您最近一年使用:0次
2019-12-25更新
|
312次组卷
|
11卷引用:山西省山西大学附属中学2017-2018学年高二上学期9月月考化学试题
山西省山西大学附属中学2017-2018学年高二上学期9月月考化学试题2015-2016学年湖南省衡阳县高二上学期期末统考化学试卷山西省汾阳中学2016-2017学年高一下学期期中考试(理)化学试题内蒙古集宁一中(西校区)2020-2021学年高二上学期第二次月考化学试题河北省衡水市第十四中学2020-2021学年高二下学期摸底考试化学试题福建省南安市柳城中学2021-2022学年高二上学期期中考试化学试题2015-2016学年辽宁鞍山一中高一下期中化学试卷湖北省孝感市七校教学联盟2016-2017学年高一下学期期末考试化学试题【全国市级联考】江苏省宿迁市2017-2018学年高一下学期期中考试化学试题浙江省丽水四校联考2019-2020学年高一11月月考化学试题(已下线)第15练 化学反应与能量变化-2023年高考化学一轮复习小题多维练(全国通用)



