10-11高三下·广东·期中
名校
解题方法
1 . A、B、C都是金属,把A浸入C的硫酸盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为
| A.A>B>C | B.A>C>B | C.B>A>C | D.B>C>A |
您最近一年使用:0次
2020-06-18更新
|
163次组卷
|
24卷引用:2015-2016学年湖南省邵阳市邵东三中高一下期中化学试卷
2015-2016学年湖南省邵阳市邵东三中高一下期中化学试卷湖南省湘南中学2018-2019学年高一下学期期中考试化学试题(已下线)2010-2011学年广东省龙山中学高一下学期期中考试化学试卷(已下线)2010-2011学年吉林省延吉市汪清六中高一下学期期中考试化学试卷(已下线)2010-2011学年吉林省汪清中学高一下学期期中考试化学试卷(已下线)2010-2011学年黑龙江省哈六中高二下学期期中考试化学试卷(已下线)2010—2011学年山东省汶上一中高二下学期期末考试化学试卷(已下线)2011-2012学年江西省井冈山实验学校高一下学期第二次月考化学试卷(已下线)2011-2012学年黑龙江海林市高级中学高一下学期期中考试化学试卷 (已下线)2011-2012学年南京学大教育专修学校高二暑期结业测试文科化学试卷2014-2015吉林省吉林市一中高二上学期期末化学试卷2014-2015学年福建省永春美岭中学高一下学期期中考试化学试卷2015-2016学年安徽黄山屯溪一中高一下期中化学试卷宁夏六盘山高级中学2016-2017学年高一下学期期中考试化学试题黑龙江省伊春市第二中学2016-2017学年高一下学期期中考试(理)化学试题黑龙江省伊春市第二中学2016-2017学年高一下学期期中考试(文)化学试题新疆兵团八师一四三团一中2018-2019学年高一下学期期中考试化学试题陕西省渭南市临渭区尚德中学2019-2020学年高一下学期网络教学调研评估检测化学试题吉林省长春市第二十九中学2019-2020学年高一下学期期中考试化学试题(文)吉林省长春市第二十九中学2019-2020学年高一下学期期中考试化学试题(理)陕西省子洲中学2018-2019学年高一下学期第二次月考化学试题浙江师范大学附属东阳花园外国语学校2020-2021学年高一下学期第一次质量检测化学试题吉林省通化县综合高级中学2020-2021学年高一下学期期中考试化学试题江苏省南京市中华中学2020-2021学年高一下学期期中考试化学试题
9-10高一下·河北衡水·期中
名校
解题方法
2 . 人造地球卫星上使用的一种高能电池(银锌蓄电池),其电池的电极反应式为:Zn+2OH--2e- =ZnO+H2O,Ag2O+H2O+2e- =2Ag+2OH-。据此判断氧化银是
| A.正极,被还原 | B.负极,被氧化 |
| C.正极,被氧化 | D.负极,被还原 |
您最近一年使用:0次
2020-06-18更新
|
788次组卷
|
82卷引用:2011-2012年湖南湘潭等四县一中高一下学期期中联考化学试卷
(已下线)2011-2012年湖南湘潭等四县一中高一下学期期中联考化学试卷(已下线)2013-2014湖南省衡南县高二下学期期末考试化学试卷湖南省2016-2017学年高二普通高中学业水平考试模拟二化学试题湖南省常德市桃花源一中2019-2020学年高一下学期期中考试化学试题湖南省衡阳市衡东县欧阳遇实验中学2019-2020学年高一上学期期末考试化学试题(已下线)2009—2010学年河北冀州中学高一下学期期中考试化学卷(已下线)09-10年深圳高中高一下学期期末测试化学卷(已下线)2010年黑龙江省牡丹江一中高一下学期期末测试化学(已下线)2010年内蒙古通辽一中高一下学期期末考试化学试题(已下线)2010-2011学年广西北海市合浦县教研室高二上学期期末考试化学试卷(已下线)2010—2011学年辽宁省大连协作体高一4月月考化学试卷(已下线)2010—2011学年安徽蚌埠二中第二学期高一期中考试化学试卷(已下线)2010-2011学年甘肃省张掖中学高一下学期期中考试化学试卷(已下线)2010-2011学年河南省许昌市高一下学期四校期中联考化学试卷(已下线)2011-2012学年山东省济南外国语学校高二上学期期中考试化学(文)试卷(已下线)2011-2012学年山东临清三中高二上学期学分认定测试化学试卷(已下线)2011-2012学年贵州省湄潭中学高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省衢州一中高一下学期期中检测化学试卷(已下线)2011-2012学年贵州省湄潭中学高一下学期期中考试化学试卷 (已下线)2011-2012年江苏南通小海中学高一下学期期中考试化学试卷(已下线)2011-2012学年广东省罗定市高一下学期期中质检理综化学试卷(已下线)2011-2012学年陕西省岐山县高一下学期期中考试化学试卷(已下线)2011-2012学年陕西省西安一中高一下学期期末考试化学试卷(已下线)2012-2013学年吉林省实验中学高二上学期期末考试化学试卷2014-2015浙江省杭州地区七校高一下学期期中联考化学试卷2014-2015陕西省西安市一中高一下学期期中化学试卷2014-2015学年安徽省涡阳四中高一下第二次质检化学试卷2015-2016学年黑龙江大庆铁人中学高二上9月考化学试卷2015-2016学年山西省大同一中高二上期末考试化学试卷2015-2016学年陕西省黄陵中学高一下学期期中考试化学试卷2015-2016学年福建省清流一中高一实验班下第三段测化学试卷2015-2016学年河北省沧州市黄骅中学高一下期中化学试卷吉林省东北师范大学附属中学净月实验学校2016-2017学年高一下学期期中考试化学试题吉林省吉林油田实验中学2016-2017学年高一下学期期中考试化学试题福建省长泰县第一中学2017-2018学年高二上学期期中考试(理)化学试题湖北省沙市中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2017-2018学年高一下学期第二次6月月考化学试题宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题河北省黄骅中学2018-2019学年高二上学期第二次月考化学试题浙江省慈溪市三山高级中学2018-2019学年高一下学期第一次月考化学试题【校级联考】江苏省常州“教学研究合作联盟”2018-2019学年高二下学期期中考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一下学期期中考试化学试题【校级联考】吉林省长春市九台区师范高中、实验高中2018-2019学年高一下学期期中考试化学试题广东省江门市第二中学2018-2019学年高一5月月考化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高一下学期期中考试化学试题(宾县用卷)新疆兵团八师一四三团一中2018-2019学年高一下学期期中考试化学试题黑龙江省龙东南联合体2018-2019学年高一下学期期末考试化学试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(学考)试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(选考)试题2020届高三化学化学二轮复习——新型电池基础练习【精编24题】河南省新乡市卫辉高中2019-2020学年高一下学期第一次调研考试化学试题甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期中考试化学试题黑龙江省鸡西市鸡东县第二中学2019-2020学年高一下学期线上考试化学试题四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题辽宁省营口市第二高级中学2018-2019学年高一下学期第一次月考化学试题湖北省宜昌市长阳县第一高级中学2019-2020高一下学期期中考试化学试题浙江省金华市曙光学校2019-2020学年高一下学期第一次月考化学试题四川省遂宁市船山区第二中学校2019-2020学年高一下学期期中考试化学试题江苏省泰州中学2019-2020学年高一下学期期中考试化学试题安徽省桐城市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)江苏省如皋市2019-2020学年高二下学期第二次月考化学试题贵州省兴仁市凤凰中学2019-2020学年高一下学期第一次月考化学试题广东省东莞市东华中学2019-2020学年高一下学期期末模拟化学试题安徽省安庆市第一中学2019-2020学年高一下学期月考化学试题甘肃省武威市第八中学2019-2020学年高一下学期期末考试化学试题四川省雅安市2019-2020学年高二下学期期末考试化学试题河南省漯河市临颍县南街高级中学2020-2021学年高一10月质量检测化学试题重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题吉林省吉林市江城中学2020-2021学年高二上学期期中考试化学(理)试题北京市第四十三中学2020-2021学年高一下学期第一次月考化学试题北京市丰台第八中学2020-2021学年高一下学期期中考试化学试题广西钦州市第四中学2020-2021学年高一下学期4月月考化学试题2甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(文)试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题陕西省宝鸡市金台区2021-2022学年高一下学期期中考试化学试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高一下学期期中考试(会考)化学试题云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题北京师范大学附属中学2022-2023学年高一下学期期中考试化学试题海南省海口市长流中学2022-2023学年高一下学期期中考试化学试题A卷四川省雅安市名山区第三中学2023-2024学年高二12月月考化学试题北京市第三中学2023-2024学年高一下学期期中考试化学试题
解题方法
3 . 某学习小组用如图所示装置探究金属锌和稀硫酸的反应,实验过程中电流表的指针发生偏转。请回答下列问题:

(1)锌片做电池的__________ 极(填“正或负”),发生的电极反应式:__________ 。
(2)铜片的现象是__________ ,发生的电极反应式:__________ 。
(3)若将稀H2SO4换成CuSO4,则正极反应式为:__________ 。
(4)若将电极换成铁片和铜片,则负极是__________ (填“铁片或铜片”)

(1)锌片做电池的
(2)铜片的现象是
(3)若将稀H2SO4换成CuSO4,则正极反应式为:
(4)若将电极换成铁片和铜片,则负极是
您最近一年使用:0次
2020-06-12更新
|
90次组卷
|
3卷引用:湖南省湘西土家族苗族自治州古丈县第一中学2019-2020学年高一下学期质量检测化学试题
4 . 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Zn+H2SO4=ZnSO4+H2↑;B.NaOH+HCl=NaCl+H2O。能设计成原电池的反应是__________ (填“A”或“B”)。
(2)将锌片和铜片按如图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
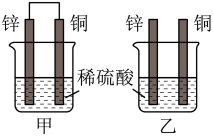
①下列说法正确的是__________ 。
A.甲、乙均为化学能转变为电能的装置
B.甲中铜片质量减少、乙中锌片质量减少
C.两烧杯中溶液的c(H+)均减小
②在相同时间内,两烧杯中产生气泡的速度:甲__________ 乙(填“>”、“<”或“=”)。
③请写出图中构成原电池的正极电极反应式:__________ 。
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为__________ 。
(1)现有如下两个反应:A.Zn+H2SO4=ZnSO4+H2↑;B.NaOH+HCl=NaCl+H2O。能设计成原电池的反应是
(2)将锌片和铜片按如图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置
B.甲中铜片质量减少、乙中锌片质量减少
C.两烧杯中溶液的c(H+)均减小
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的正极电极反应式:
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
您最近一年使用:0次
解题方法
5 . 如图所示是铜锌原电池示意图。当该原电池工作时,下列描述不正确的是
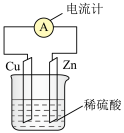

| A.溶液逐渐变蓝 |
| B.锌片上的电极反应式是:Zn—2e—===Zn2+ |
| C.铜片上有气泡产生 |
| D.电流计指针发生偏转 |
您最近一年使用:0次
名校
解题方法
6 . 某玩具所用的钮扣电池的两极材料分别为锌和氧化银,电解质溶液为NaOH溶液,电池的总反应式为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是
| A.原电池工作时,负极附近溶液的pH增大 | B.锌为负极,Ag2O为正极 |
| C.锌为正极,Ag2O为负极 | D.原电池工作时,外电路电流由负极流向正极 |
您最近一年使用:0次
2020-05-27更新
|
80次组卷
|
6卷引用:湖南省怀化市辰溪县辰溪县第一中学2019-2020学年高二12月月考化学试题
湖南省怀化市辰溪县辰溪县第一中学2019-2020学年高二12月月考化学试题浙江省嘉兴市第一中学2018届高三上学期期末考试化学试题浙江省嘉兴市第一中学2017-2018学年高二上学期期末考试化学试题(已下线)【艺体生文化课百题突围系列-基础练测】专题2.9 电化学基础(已下线)【新东方】高中化学5001新疆维吾尔自治区伊犁哈萨克自治州奎屯市第一高级中学2019-2020学年高二期末考试试题
名校
解题方法
7 . 某原电池装置如图所示,盐桥中装有含琼胶的KCl饱和溶液。下列有关叙述中正确的是( )
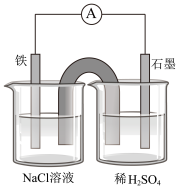

| A.Fe作正极,发生氧化反应 | B.工作一段时间后,两烧杯中溶液pH均不变 |
| C.负极反应:2H++2e-=H2↑ | D.工作一段时间后,NaCl溶液中c(Cl-)增大 |
您最近一年使用:0次
2020-05-27更新
|
77次组卷
|
3卷引用:湖南省怀化市辰溪县辰溪县第一中学2019-2020学年高二12月月考化学试题
名校
解题方法
8 . 可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法正确的是
| A.比较钠、镁、铝三种金属空气电池,Na-空气电池的理论比能量最高 |
| B.以NaOH溶液为电解液时,负极反应为Al+3OH--3e-=Al(OH)3↓ |
| C.以NaOH溶液为电解液时,电池在工作过程中电解液的碱性保持不变 |
| D.以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-=4OH- |
您最近一年使用:0次
名校
解题方法
9 . (1)有① 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ;四组微粒或物质。互为同位素的是
;四组微粒或物质。互为同位素的是________ (填编号,下同),互为同素异形体的是_________ 。
(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要__________ (填“放出”或“吸收”)___________ kJ能量。
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4。则负极是______ (填“A”或“B”),负极反应式为 ______________ 。

(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为_______ ,(填化学式),负极反应式为______________
 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ;四组微粒或物质。互为同位素的是
;四组微粒或物质。互为同位素的是(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4。则负极是

(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为
您最近一年使用:0次
名校
解题方法
10 . 分析下图所示的三个原电池装置,其中结论正确的是
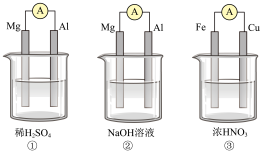

| A.①②中Mg作负极 |
| B.③中电流方向由Cu流向Fe |
| C.②中Mg作正极,电极反应式为2H2O+2e-=2OH-+H2↑ |
| D.③中Cu作正极,电极反应式为2H++2e-=H2↑ |
您最近一年使用:0次
2020-05-09更新
|
227次组卷
|
4卷引用:湖南省娄底市2019-2020学年高一下学期期末考试化学试题



