1 . 我国科学家以LiI为催化剂,通过改变盐浓度或溶剂调节锂-硫电池的放电性能,放电模型装置如图所示。下列说法正确的是
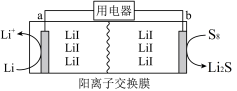

| A.放电时,导线中无电流 |
| B.放电时,Li+通过导线向a极迁移 |
| C.b极反应式为S8+16e-+16Li+=8Li2S |
| D.a极质量的减少量和b极质量的增加量无关联性 |
您最近一年使用:0次
名校
解题方法
2 . 由锌片、铜片和200mL稀H2SO4组成的原电池如下图所示:
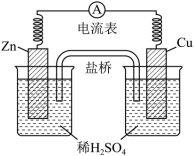
(1)原电池的负极反应式为___________ ,正极反应式为___________ ,盐桥中的K+向___________ (填“铜”或“锌”)电极移动。
(2)一段时间后,当在铜片上放出5.6L(标准状况)气体时,H2SO4恰好消耗一半,则产生这些气体的同时,共消耗___________ g锌,有___________ mol电子通过了导线,原硫酸的物质的量浓度是___________ 。
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为___________ 。

(1)原电池的负极反应式为
(2)一段时间后,当在铜片上放出5.6L(标准状况)气体时,H2SO4恰好消耗一半,则产生这些气体的同时,共消耗
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次



