解题方法
1 .  等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
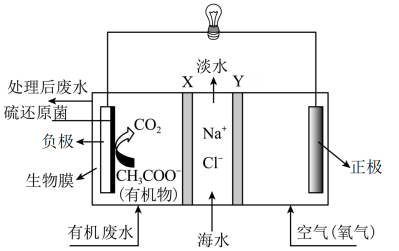
等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
 等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
| A.该装置可以在高温下工作 |
B. 依次为阴离子、阳离子交换膜 依次为阴离子、阳离子交换膜 |
C.负极反应式为 |
| D.该装置工作时,电能转化为化学能 |
您最近一年使用:0次
解题方法
2 . 一种钠离子电池的工作原理如图所示。充电过程中,磷酸钒钠[Na3V2(PO4)3]在外电压的作用下脱嵌部分Na+形成Na3-xV2(PO4)3,脱出的Na+进入电解液中,再传输到硬碳材料形成化合物NaxC。下列说法正确的是
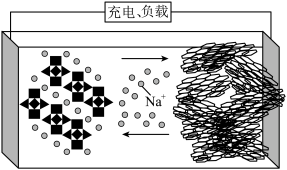

| A.充电时Na3V2(PO4)3为阴极 |
| B.充电时,电解液的质量增大 |
| C.放电时Na+由负极迁移到正极材料中 |
| D.放电时的正极反应为Na3V2(PO4)3-xe-=Na3-xV2(PO4)3+xNa+ |
您最近一年使用:0次
2024-03-16更新
|
38次组卷
|
2卷引用:陕西省安康市高新中学2023-2024学年高三12月月考理科综合试题
名校
3 . 铝硫二次电池是一种具有高能量密度、廉价原材料、有前途的替代储能装置,一种铝硫电池如图所示,放电时的电池总反应为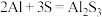 。下列说法错误的是
。下列说法错误的是

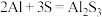 。下列说法错误的是
。下列说法错误的是
A.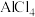 和 和 中均存在配位键 中均存在配位键 |
| B.该电池电解质区域所用溶剂不可以为水 |
C.电池放电时的正极反应式为 |
| D.用该电池保护地下铁管道不被腐蚀,铁管道应连接电池的硫碳电极 |
您最近一年使用:0次
名校
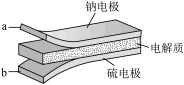
4 . 室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。
工作时,在硫电极发生反应: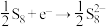 ,
,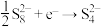 ,
,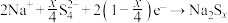
下列叙述错误的是
工作时,在硫电极发生反应:
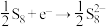 ,
,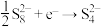 ,
,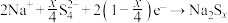
下列叙述错误的是

A.放电时 从钠电极向硫电极迁移 从钠电极向硫电极迁移 |
B.放电时外电路电子流动的方向是 |
C.充电时阴极反应为: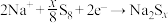 |
| D.炭化纤维素纸的作用是增强硫电极导电性能 |
您最近一年使用:0次
名校
5 . 詹姆斯·韦伯太空望远镜捕捉到第一批火星图像。火星本身不发光, 其红色的外观源于表层土壤中丰富的铁元素及反射的太阳光。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于___________ (填“吸收”或“发射”)光谱。
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是___________ ,基态铁原子价电子轨道表示式为___________ ,其核外有___________ 种不同运动状态的电子。
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池___________ 。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池
您最近一年使用:0次
名校
6 . 一种三室微生物燃料电池的工作原理如图所示,该电池能同时去除有机物、脱氮形成无害气体和水。下列说法不正确 的是
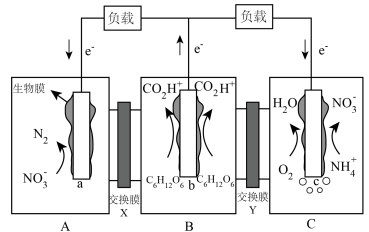
| A.X、Y交换膜均为质子交换膜 |
| B.电极室C中溶液经灭菌后通入电极室A |
C.b电极反应式: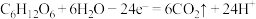 |
| D.电极室C中仅发生还原反应 |
您最近一年使用:0次
解题方法
7 . 中国科学院将分子 引入电解质中调整充电和放电反应途径,实现了高功率可充电
引入电解质中调整充电和放电反应途径,实现了高功率可充电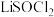 电池,工作原理如下图所示。下列有关说法错误的是
电池,工作原理如下图所示。下列有关说法错误的是
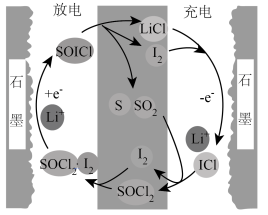
 引入电解质中调整充电和放电反应途径,实现了高功率可充电
引入电解质中调整充电和放电反应途径,实现了高功率可充电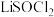 电池,工作原理如下图所示。下列有关说法错误的是
电池,工作原理如下图所示。下列有关说法错误的是
A.分子 的引入催化了电池放电和充电过程 的引入催化了电池放电和充电过程 |
| B.电池工作环境必须在无水无氧的条件下进行 |
C.充电时阴极反应式: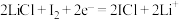 |
D.电池的放电总反应: |
您最近一年使用:0次
解题方法
8 . 某小组研究Cu2+和Fe3+的氧化性,进行如下实验。
实验Ⅰ: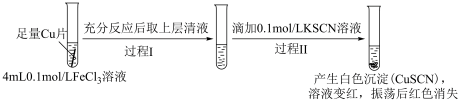
已知:1.(SCN)2 是黄色液体,氧化性:I2 < (SCN)2 < Br2。
2.K3[Fe(CN)6]溶液可用于Fe2+的检验,生成蓝色沉淀。
3.Fe3+与SCN-可以形成多种微粒,例如[Fe(SCN)]2+、Fe(SCN)3等溶液显红色。
(1)实验Ⅰ过程Ⅰ中Cu与FeCl3反应的化学方程式是___________ 。
(2)实验Ⅰ过程Ⅱ中溶液变红,说明产生了Fe3+,分析可能原因。
假设①:Fe2+被Cu2+氧化。
过程Ⅱ发生反应的电极反应式:
a.氧化反应:Fe2+-e-+3SCN-=Fe(SCN)3
b.还原反应:___________ 。
假设②:Cu2+和SCN-发生反应生成(SCN)2,进而将清液中的Fe2+氧化为Fe3+。
设计实验Ⅱ证实假设。
实验Ⅱ: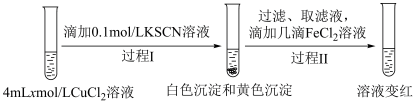
i.
___________ 。
ⅱ.实验Ⅱ中过程Ⅱ的离子方程式为___________ 。
(3)设计实验进一步研究Fe3+能否氧化SCN-。
实验Ⅲ:
①实验Ⅲ中加入K3[Fe(CN)6]溶液后,若___________ (写出实验现象),
说明在该实验条件下,Fe3+未能氧化SCN-。
②进一步查阅资料发现:Fe3+与SCN-可以发生氧化还原反应。该小组通过实验证明了该反应的发生。请你在答题卡方框中用文字或图示 设计实验方案,并描述相关的实验现象:___________ 。
实验Ⅰ:

已知:1.(SCN)2 是黄色液体,氧化性:I2 < (SCN)2 < Br2。
2.K3[Fe(CN)6]溶液可用于Fe2+的检验,生成蓝色沉淀。
3.Fe3+与SCN-可以形成多种微粒,例如[Fe(SCN)]2+、Fe(SCN)3等溶液显红色。
(1)实验Ⅰ过程Ⅰ中Cu与FeCl3反应的化学方程式是
(2)实验Ⅰ过程Ⅱ中溶液变红,说明产生了Fe3+,分析可能原因。
假设①:Fe2+被Cu2+氧化。
过程Ⅱ发生反应的电极反应式:
a.氧化反应:Fe2+-e-+3SCN-=Fe(SCN)3
b.还原反应:
假设②:Cu2+和SCN-发生反应生成(SCN)2,进而将清液中的Fe2+氧化为Fe3+。
设计实验Ⅱ证实假设。
实验Ⅱ:

i.

ⅱ.实验Ⅱ中过程Ⅱ的离子方程式为
(3)设计实验进一步研究Fe3+能否氧化SCN-。
实验Ⅲ:

①实验Ⅲ中加入K3[Fe(CN)6]溶液后,若
说明在该实验条件下,Fe3+未能氧化SCN-。
②进一步查阅资料发现:Fe3+与SCN-可以发生氧化还原反应。该小组通过实验证明了该反应的发生。请你在
您最近一年使用:0次
解题方法
9 . 原电池原理广泛应用于科技、生产和生活中。
(1)一种处理垃圾渗透液并用其发电的装置工作示意图如下。

①在空气中,微生物将垃圾渗透液硝化,该反应的离子方程式为___________ 。
②Y电极的电极反应式为___________ 。
③盐桥中 移向
移向___________ (填“X或Y”)极;当转移0.15mol电子时,生成标准状况下 的体积为
的体积为___________ L。
(2)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
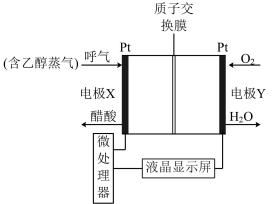
①电极X是该电池的___________ (填“正”或“负”)极,电池总反应式为___________ 。
②电池工作时,质子通过交换膜___________ (填“从左向右”或“从右向左”)迁移。
(1)一种处理垃圾渗透液并用其发电的装置工作示意图如下。

①在空气中,微生物将垃圾渗透液硝化,该反应的离子方程式为
②Y电极的电极反应式为
③盐桥中
 移向
移向 的体积为
的体积为(2)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

①电极X是该电池的
②电池工作时,质子通过交换膜
您最近一年使用:0次
名校
10 . 银铝电池具有能量密度高的优点,其工作原理如图所示,电池放电时的反应为2Al+3Ag2O+2NaOH+3H2O=2Na[Al(OH)4]+6Ag。
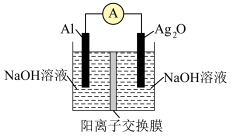
下列说法错误的是

下列说法错误的是
| A.Al为电源负极 | B.正极反应为Ag2O+2e-+H2O=2Ag+2OH- |
| C.放电时负极区pH增大 | D.放电时Na+通过交换膜向右侧移动 |
您最近一年使用:0次
2023-11-10更新
|
685次组卷
|
4卷引用:河北省定州市2023-2024学年高二上学期11月期中考试化学试题



