解题方法
1 . 电池的发明是化学对人类的一项重大贡献。
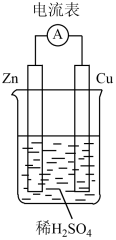
(1)下图所示装置中,Zn片作___________ (填“正极”或“负极”)。Cu片上发生反应的电极反应式为___________ ;能证明化学能转化为电能的实验现象是___________ 。
(2)氢氧燃料电池是一种高效、低污染的新型电池,在新能源汽车、航空航天、轨道交通等领域均有应用。某氢氧燃料电池的示意图如下。

下列说法正确的是___________ (填序号)。
①b电极是电池的负极
②该装置实现了将 反应释放的能量直接转化为电能
反应释放的能量直接转化为电能
③电池工作时,电池内部的 定向移动
定向移动
(1)下图所示装置中,Zn片作

(2)氢氧燃料电池是一种高效、低污染的新型电池,在新能源汽车、航空航天、轨道交通等领域均有应用。某氢氧燃料电池的示意图如下。

下列说法正确的是
①b电极是电池的负极
②该装置实现了将
 反应释放的能量直接转化为电能
反应释放的能量直接转化为电能③电池工作时,电池内部的
 定向移动
定向移动
您最近一年使用:0次
2 . 根据原电池原理,人们研制出了性能各异的化学电池。

(1)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
①通入H2的一极是电池的______ (填“正极”或“负极”)。
②电子从通入______ 的一极经导线流向通入______ 的一极(填“H2”或“O2”)。
③通入O2一极的电极反应式为______ 。
(2)一种新型Mg-海水电池的工作原理如图所示,下列说法正确的是______ (填字母)。

a.该电池工作时,金属镁作正极
b.H2O2在石墨电极上得到电子,发生还原反应

(1)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
①通入H2的一极是电池的
②电子从通入
③通入O2一极的电极反应式为
(2)一种新型Mg-海水电池的工作原理如图所示,下列说法正确的是

a.该电池工作时,金属镁作正极
b.H2O2在石墨电极上得到电子,发生还原反应
您最近一年使用:0次
3 . 氢气是一种新型的绿色能源,又是一种重要的化工原料。
①氢气燃烧热值高。实验测得,在常温常压下,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式正确的是________ 。
A.H2(g)+ O2(g)═H2O(g)△H=+285.8kJ/mol
O2(g)═H2O(g)△H=+285.8kJ/mol
B. H2(g)+ O2(g)═H2O(l)△H=﹣285.8kJ/mol
O2(g)═H2O(l)△H=﹣285.8kJ/mol
C. H2(g)+ O2(g)═H2O(l)△H=+285.8kJ/mol
O2(g)═H2O(l)△H=+285.8kJ/mol
D. H2+ O2═H2O△H=﹣285.8 kJ/mol
O2═H2O△H=﹣285.8 kJ/mol
②氢氧燃料电池能量转化率高,具有广阔的发展前景。氢氧燃料电池中,发生还原反应的物质是______ (填“氢气”或“氧气”)。
③氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g) △H=﹣92.4 kJ/mol
反应达到平衡后,升高温度则反应速率_______ (填“增大”或“减小”);平衡将向____________ (填“正反应方向”或“逆反应方向”)移动。
①氢气燃烧热值高。实验测得,在常温常压下,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式正确的是
A.H2(g)+
 O2(g)═H2O(g)△H=+285.8kJ/mol
O2(g)═H2O(g)△H=+285.8kJ/molB. H2(g)+
 O2(g)═H2O(l)△H=﹣285.8kJ/mol
O2(g)═H2O(l)△H=﹣285.8kJ/molC. H2(g)+
 O2(g)═H2O(l)△H=+285.8kJ/mol
O2(g)═H2O(l)△H=+285.8kJ/molD. H2+
 O2═H2O△H=﹣285.8 kJ/mol
O2═H2O△H=﹣285.8 kJ/mol②氢氧燃料电池能量转化率高,具有广阔的发展前景。氢氧燃料电池中,发生还原反应的物质是
③氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g) △H=﹣92.4 kJ/mol
反应达到平衡后,升高温度则反应速率
您最近一年使用:0次
2016-09-13更新
|
231次组卷
|
2卷引用:2015-2016学年湖南省长沙市望城县高二(下)学业水平模拟化学试卷



