名校
解题方法
1 . 下列说法正确的是
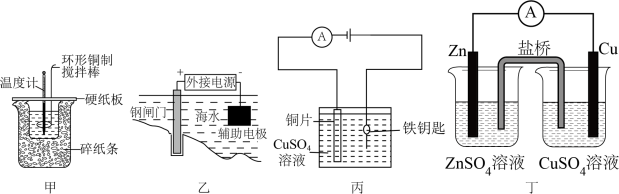

A.用图甲装置测得中和热 偏大 偏大 |
| B.图乙可以保护钢闸门不被腐蚀 |
| C.图丙用于铁上镀铜且硫酸铜溶液浓度不变 |
D.图丁装置盐桥中阴离子向 溶液中迁移 溶液中迁移 |
您最近一年使用:0次
2023-12-14更新
|
417次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题福建省福州格致中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假收官卷02-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)重庆市万州二中2023-2024学年高二下学期开学考试 化学
解题方法
2 . 化学电池是新能源和可再生能源的重要组成部分。根据所学知识,回答下列问题:
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入 溶液中,实验装置如图所示。
溶液中,实验装置如图所示。
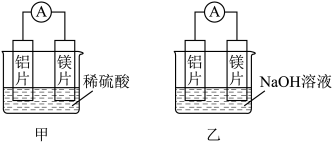
①写出甲中电池总反应的离子方程式:_________ 。
②乙中铝为_________ 极,写出铝电极的电极反应式:_________ 。
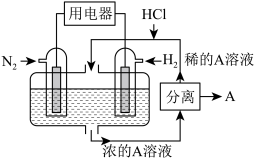
(2)有人设想以 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是_________ ,A是_________ (填化学式)。
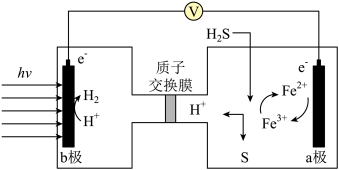
(3)我国科学家在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。b极为光能转化为电能的装置,该电极的电极材料可用_________ (填化学式),该装置的总反应为__________________ ,a极发生的反应为_________ (填“氧化”或“还原”)反应。
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入
 溶液中,实验装置如图所示。
溶液中,实验装置如图所示。
①写出甲中电池总反应的离子方程式:
②乙中铝为
(2)有人设想以
 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
(3)我国科学家在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。b极为光能转化为电能的装置,该电极的电极材料可用

您最近一年使用:0次
2023-04-27更新
|
193次组卷
|
2卷引用:江西省九江市五校2022-2023学年高一下学期5月联考化学试题
名校
解题方法
3 . 电化学原理在工业生产、物质制备、污染物理处理等方面应用广泛,请按要求回答下列问题。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
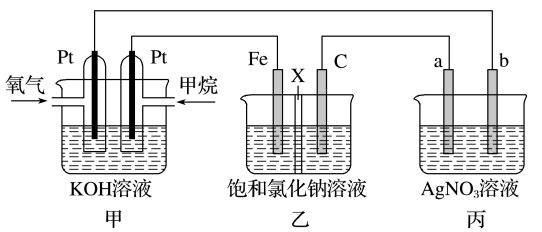
请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是___________ 。
(2)乙中X是___________ 交换膜,向乙中加入几滴酚酞溶液,工作一段时间后___________ 电极(填“铁”或“碳”)附近溶液变红,该电极的电极反应式为___________ 。
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为___________ 。
(4)欲用丙装置给铜镀银,b应是___________ (填化学式)。
(5)将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为___________ L
Ⅱ.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统原理示意图。
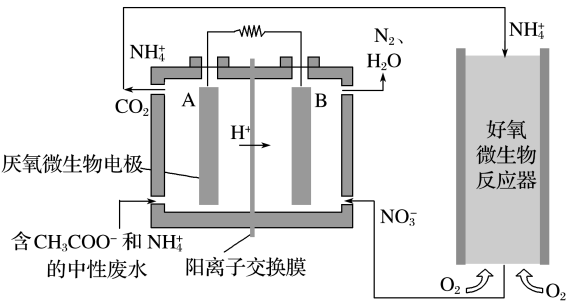
(6)A极的电极反应式为___________ ,A、B两极生成CO2和N2的物质的量之比为___________ 。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。

请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为
(4)欲用丙装置给铜镀银,b应是
(5)将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为
Ⅱ.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统原理示意图。

(6)A极的电极反应式为
您最近一年使用:0次
2022-08-27更新
|
393次组卷
|
2卷引用:江西省万安中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
4 . 用氟硼酸(HBF4属于强酸)代替硫酸作铅蓄电池的电解质溶液,可使铅蓄电池在低温下工作时的性能更优良,反应方程式为

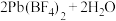 ,
, 为可溶于水的强电解质,下列说法正确的是
为可溶于水的强电解质,下列说法正确的是


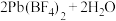 ,
, 为可溶于水的强电解质,下列说法正确的是
为可溶于水的强电解质,下列说法正确的是A.充电时,当阳极质量减少23.9g时转移 电子 电子 |
B.放电时, 电极附近溶液的 电极附近溶液的 增大 增大 |
C.电子放电时,负极反应为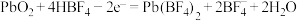 |
D.充电时, 电极的电极反应式为 电极的电极反应式为 |
您最近一年使用:0次
2022-08-21更新
|
115次组卷
|
2卷引用:江西省景德镇一中2021-2022学年高一下学期期中质量检测(19)班化学试题
名校
5 . 蓄电池在放电时起原电池的作用,在充电时起电解池的作用,下面是某蓄电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2下列推断正确的是
Fe(OH)2+Ni(OH)2下列推断正确的是
 Fe(OH)2+Ni(OH)2下列推断正确的是
Fe(OH)2+Ni(OH)2下列推断正确的是| A.放电时的正极在充电时须接电源的负极 |
| B.放电时NiO2是正极,转移2mol电子时正极有1molNiO2被还原 |
| C.放电时,电解质溶液中的阳离子向负极方向移动 |
| D.充电时,阴极上的电极反应为Fe(OH)2-2e-=Fe+2OH- |
您最近一年使用:0次
2021-06-23更新
|
203次组卷
|
2卷引用:江西省清江中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
6 . 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。一段时间后,断开电键K,下列说法正确的是

| A.电流由A极流出,最后由B极流入 |
| B.反应一段时间后,向乙池中加入一定量Cu固体能使溶液恢复原浓度 |
C.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O= +8H+ +8H+ |
| D.甲池中消耗280mL(标准状况下)O2,此时丙池中理论上析出3.2g固体 |
您最近一年使用:0次
2020-10-20更新
|
903次组卷
|
4卷引用:江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题
江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题江西省南昌十九中2021-2022学年高二上学期期末考试化学试卷内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题(已下线)第12单元 电化学基础(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷
名校
解题方法
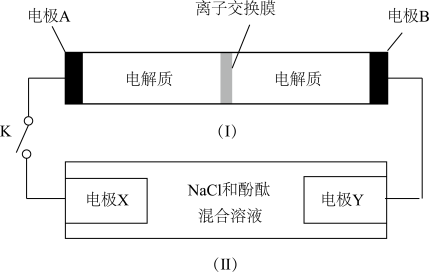
7 . 如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电时的电池反应为2K2S2+KI3 K2S4+3KI。装置(Ⅱ)为电解池的示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法不正确的是( )
K2S4+3KI。装置(Ⅱ)为电解池的示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法不正确的是( )
 K2S4+3KI。装置(Ⅱ)为电解池的示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法不正确的是( )
K2S4+3KI。装置(Ⅱ)为电解池的示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法不正确的是( )
| A.K+从左到右通过离子交换膜 |
B.电极A上发生的反应为 +2e-= 3I- +2e-= 3I- |
| C.电极Y上发生的反应为2Cl--2e-= Cl2↑ |
| D.当有0.1 mol K+通过离子交换膜时,X电极上产生1.12 L气体 |
您最近一年使用:0次
2020-09-18更新
|
289次组卷
|
7卷引用:江西省丰城中学2018-2019学年高一上学期课改期末考试化学试题
名校
8 . 有关下列四个常用电化学装置的叙述中,正确的是( )
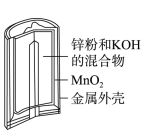 | 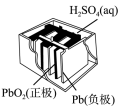 |  | 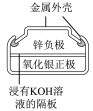 |
| 图Ⅰ 碱性锌锰电池 | 图Ⅱ 铅硫酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
| A.图Ⅰ所示电池中,MnO2的作用是催化剂 |
| B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 |
| D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag |
您最近一年使用:0次
2020-05-23更新
|
261次组卷
|
13卷引用:江西省赣州市石城中学2022-2023学年高一下学期第一次月考化学试题
江西省赣州市石城中学2022-2023学年高一下学期第一次月考化学试题【校级联考】江西省南昌市八一中学、洪都中学等七校2018-2019学年高二上学期期末考试化学试题辽源市第五中学2019-2020学年高一下学期第二次月考化学试题江西省南昌市八一中学、洪都中学、南师附中、十七中四校2021-2022学年高二上学期期末联考化学考试试题(已下线)2013届北京市海淀区高三下学期期末练习理综化学试卷北京师范大学附属中学2017-2018学年高二上学期期末考试化学试题新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题吉林省九台市第四中学2017-2018学年高二上学期期末考试化学试题【校级联考】湖南省浏阳一中、醴陵一中2018-2019学年高二上学期12月联考化学试题宁夏育才中学2019-2020学年高二上学期期末考试化学试题黑龙江省牡丹江市穆棱市第一中学2019-2020学年高二上学期期末考试化学试题新疆克拉玛依市2018届高三第三次模拟检测理综化学试题福建省三明第一中学2021-2022学年高二上学期开学考试化学试题
2011·江苏·一模
9 . 如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是( )
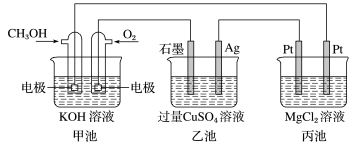
| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+ |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度 |
| D.甲池中消耗280mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体 |
您最近一年使用:0次
2020-05-16更新
|
1362次组卷
|
39卷引用:【南昌新东方】2019-2020 南昌五中高一下第一次月考
(已下线)【南昌新东方】2019-2020 南昌五中高一下第一次月考(已下线)2014届江西省玉山一中高三化学强化周考(十三)试卷2014-2015学年湖北省武汉市第二中学高一下期末化学试卷江西省抚州市临川第二中学2015-2016学年高二上12月月考化学试卷2016-2017学年江西省南昌市第二中学高二上学期期末考试化学试卷河北省承德市第一中学2018-2019学年高一下学期第三次月考化学试题河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题江西省宜春市万载中学2021-2022学年高二上学期第二次月考化学试题(已下线)2011届江苏省苏锡常镇四市高三调研测试(一)化学试卷(已下线)2011届湖北省天门市高三模拟考试(三)(理综)化学部分(已下线)2012届浙江省重点中学协作体高三3月调研理综部分(已下线)2012届江苏省扬州中学高三3月双周练习(二)化学试卷(已下线)2014高考名师推荐化学电解规律及电化学计算2015届河南省新密市青屏高中高三第三次月考化学试卷2015-2016学年吉林省吉林一中高二上期中考试化学试卷2015-2016学年山东省新泰一中高二上学期期中测试化学试卷2016届甘肃省嘉峪关一中高三上第三次模拟考试化学试卷2016届四川省新津中学高三下学期3月月考化学试卷12016届四川省新津中学高三下学期3月月考化学试卷22015-2016学年河北省定州中学高二6月月考化学试卷2017届河北省沧州市第一中学高三上周测化学试卷2017届湖南省长沙市长郡中学高三上学期第三次月考模拟化学试卷2016-2017学年辽宁省实验中学分校高二上期中化学卷2016-2017学年甘肃省天水市第一中学高二下学期开学考试化学试卷2016-2017学年甘肃省天水市第一中学高二下学期开学考试(寒假作业检测)化学试卷山西省康杰中学2018届高三上学期第一次月考化学试卷河北省邢台市第一中学2017-2018学年高二上学期第二次月考化学试题湖南省衡阳市第八中学2018届高三(实验班)第三次质检化学试题四川省广安市第二中学校2017-2018学年高二下学期第二次月考化学试题山西省运城市临猗中学2019届高三上学期第一次月考化学试题河南省南阳市2018-2019学年高二上学期期中质量评估化学试题2020届高三化学化学二轮复习——高考常考题型:离子放电顺序及电解规律【夯基提能】【精编30题】河北省石家庄外国语学校2019-2020学年高二上学期期末考试化学试题人教版(2019)高二化学选择性必修1第四章 化学反应与电能 第二节 电解池 课时2 电解原理的应用黑龙江省哈尔滨市第一中学2021届高三上学期期中考试化学试题(已下线)第四章 化学反应与电能(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题浙江省温州市2021-2022学年高二上学期12月普通高中学考适应性测试化学试题(已下线)专题八 电化学的相关计算
名校
10 . 如图中A为电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,容器C为盛有500mL各0.1mol/L的CuSO4和K2SO4混合液的电解槽,e、f均为铂电极。接通电路后,发现B上的c点显红色,C中阳极产生1.12L(标况)气体,电解过程不考虑能量损失。
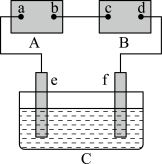
(1)电源A上的b为______ 极,滤纸B上d为______ 极。
(2)写出B上所发生的反应的化学反应方程式_________ 。
(3)写出C容器中阳极产生的气体是_______ (填名称),另一极增重____ 克。

(1)电源A上的b为
(2)写出B上所发生的反应的化学反应方程式
(3)写出C容器中阳极产生的气体是
您最近一年使用:0次
2019-05-01更新
|
271次组卷
|
2卷引用:江西省景德镇一中2020-2021学年高一下学期期中考试化学(2班)试题



