化学电池是新能源和可再生能源的重要组成部分。根据所学知识,回答下列问题:
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入 溶液中,实验装置如图所示。
溶液中,实验装置如图所示。
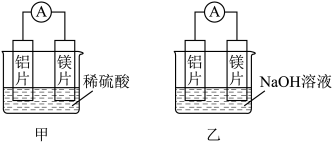
①写出甲中电池总反应的离子方程式:_________ 。
②乙中铝为_________ 极,写出铝电极的电极反应式:_________ 。
(2)有人设想以 和
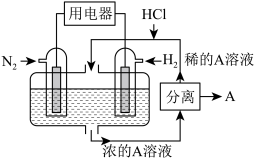
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是_________ ,A是_________ (填化学式)。
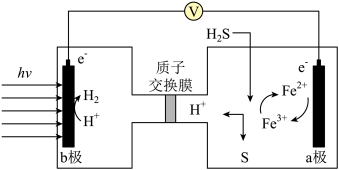
(3)我国科学家在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。b极为光能转化为电能的装置,该电极的电极材料可用_________ (填化学式),该装置的总反应为__________________ ,a极发生的反应为_________ (填“氧化”或“还原”)反应。
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入
 溶液中,实验装置如图所示。
溶液中,实验装置如图所示。
①写出甲中电池总反应的离子方程式:
②乙中铝为
(2)有人设想以
 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
(3)我国科学家在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。b极为光能转化为电能的装置,该电极的电极材料可用

更新时间:2023-04-27 22:45:29
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】亚铁氰化钾K4Fe(CN)6俗名黄血盐,可溶于水,不溶于乙醇。以某电镀厂排放的含NaCN废液为主要原料制备黄血盐的流程如下:
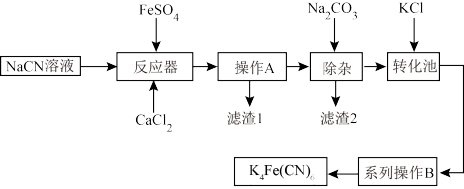
请回答下列问题:
(1)常温下,HCN的电离常数Ka=5.0×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是_____ 。
②浓度均为0.5mol·L−1的NaCN和HCN的混合溶液显___ (填“酸”“碱”或“中”)性,通过计算说明:____ 。
(2)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:_____ 。
(3)系列操作B为_______ 。
(4)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗可溶性盐Tl2SO4中毒,得到K2SO4及另外一种复杂难溶物,试写出上述治疗Tl2SO4中毒的离子方程式:_____ 。
(5)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。①K+移向催化剂______ (填“a”或“b”)。②催化剂a表面发生的反应为_______ 。


请回答下列问题:
(1)常温下,HCN的电离常数Ka=5.0×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是
②浓度均为0.5mol·L−1的NaCN和HCN的混合溶液显
(2)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:
(3)系列操作B为
(4)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗可溶性盐Tl2SO4中毒,得到K2SO4及另外一种复杂难溶物,试写出上述治疗Tl2SO4中毒的离子方程式:
(5)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。①K+移向催化剂

您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某化学兴趣小组探究FeCl3溶液和Na2SO3溶液的反应情况。
已知:K3[Fe(CN)6]可以和Fe2+生成蓝色沉淀,常用于Fe2+的检验。请回答相关问题。
[实验1]分别将100mL1.0mol·L-1的FeCl3溶液和Na2SO3溶液装入两个烧杯中,按图进行实验,观察到电流计指针发生偏转。
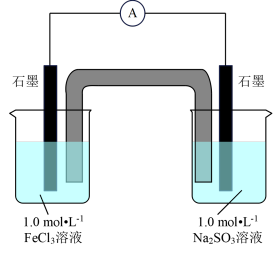
(1)请写出左侧烧杯中的电极反应式__ 。盐桥中的阳离子向__ (填“左侧”或“右侧”)烧杯中迁移。
[实验2]在试管1中加入2mL1.0mol·L-1Na2SO3溶液,然后再滴加两滴1.0mol·L-1FeCl3溶液,溶液中立刻变成红褐色。对试管1进行加热至沸腾,产生红褐色沉淀。取出几滴混合液,加K3[Fe(CN)6]溶液,无蓝色沉淀出现。整个过程中未观察到明显的气泡产生。
[实验3]在试管2中加入5mL1.0mol·L-1FeCl3溶液,然后再滴加1mL1.0mol·L-1Na2SO3溶液,溶液立刻变成红褐色。取出几滴混合液,加K3[Fe(CN)6]溶液,产生蓝色沉淀。
(2)实验3中生成蓝色沉淀的离子方程式为__ 。请设计实验证明SO 被氧化
被氧化__ 。
[反思与研讨]
资料显示:H2SO3的Ka1=1.7×10-2Ka2=6.0×10-8;Fe(OH)3的Ksp=4×10-38;反应2Fe3++ SO +H2O
+H2O 2Fe2++SO
2Fe2++SO +2H+的平衡常数K=1020.6。
+2H+的平衡常数K=1020.6。
(3)反应2Fe3++3SO +6H2O
+6H2O 2Fe(OH)3↓+3H2SO3的平衡常数K的数量级为
2Fe(OH)3↓+3H2SO3的平衡常数K的数量级为__ 。由此可判断FeCl3溶液和Na2SO3溶液发生__ (填“双水解”或“氧化还原”)反应的趋势更大。
已知:K3[Fe(CN)6]可以和Fe2+生成蓝色沉淀,常用于Fe2+的检验。请回答相关问题。
[实验1]分别将100mL1.0mol·L-1的FeCl3溶液和Na2SO3溶液装入两个烧杯中,按图进行实验,观察到电流计指针发生偏转。

(1)请写出左侧烧杯中的电极反应式
[实验2]在试管1中加入2mL1.0mol·L-1Na2SO3溶液,然后再滴加两滴1.0mol·L-1FeCl3溶液,溶液中立刻变成红褐色。对试管1进行加热至沸腾,产生红褐色沉淀。取出几滴混合液,加K3[Fe(CN)6]溶液,无蓝色沉淀出现。整个过程中未观察到明显的气泡产生。
[实验3]在试管2中加入5mL1.0mol·L-1FeCl3溶液,然后再滴加1mL1.0mol·L-1Na2SO3溶液,溶液立刻变成红褐色。取出几滴混合液,加K3[Fe(CN)6]溶液,产生蓝色沉淀。
(2)实验3中生成蓝色沉淀的离子方程式为
 被氧化
被氧化[反思与研讨]
资料显示:H2SO3的Ka1=1.7×10-2Ka2=6.0×10-8;Fe(OH)3的Ksp=4×10-38;反应2Fe3++ SO
 +H2O
+H2O 2Fe2++SO
2Fe2++SO +2H+的平衡常数K=1020.6。
+2H+的平衡常数K=1020.6。(3)反应2Fe3++3SO
 +6H2O
+6H2O 2Fe(OH)3↓+3H2SO3的平衡常数K的数量级为
2Fe(OH)3↓+3H2SO3的平衡常数K的数量级为
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】(1)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。

①正极反应为_________ 。
②当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少______ mol离子。
(2)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+
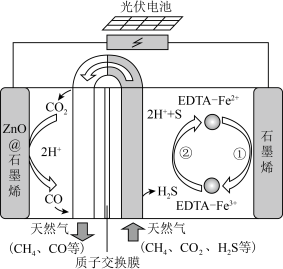
该装置工作时,阴极的电极反应:_________ ;协同转化总反应:___________ ;若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为_______ 性(碱性、中性、酸性)
(3)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池正极极增重______ g。
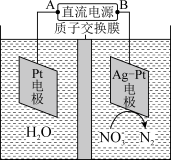
(4)电化学降解法可用于处理酸性硝酸盐污水,设计一电解池(如图所示)。 若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为____ g。

①正极反应为
②当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少
(2)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+

该装置工作时,阴极的电极反应:
(3)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池正极极增重
(4)电化学降解法可用于处理酸性硝酸盐污水,设计一电解池(如图所示)。 若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为

您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】LiCoO2是锂离子电池最早使用的电极材料,利用原钴矿(含Cr2O3、NiS等杂质)制备LiCoO2的工艺流程如下:
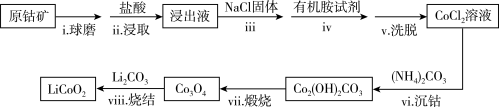
资料:i. 在含一定量Cl−的溶液中,钴离子以CoCl42-形式存在:Co2++4Cl− CoCl42−
CoCl42−
ii. CoCl42−溶于有机胺试剂,有机胺不溶于水。
iii. 盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:
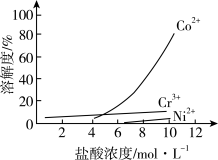
(1)步骤ii选用盐酸的浓度应为__________ 。
a. 4 mol/L b. 6 mol/L c. 10 mol/L
(2)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的_____________ 。
(3)步骤iv的操作是_______ 。
(4)步骤vi用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钴(Co2(OH)2CO3)。实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因____________ 。
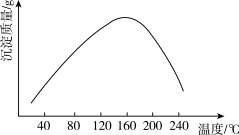
(5)步骤viii中Co3O4 和Li2CO3 混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是_____________ 。
(6)锂离子电池的工作原理如图,充、放电过程中,Li+在LiCoO2电极和碳电极之间传递。电池的总反应为:LixC + Li1-xCoO2 C+LiCoO2
C+LiCoO2
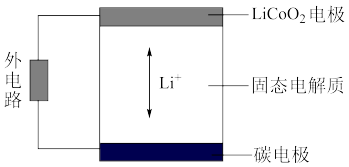
①放电时,电池的负极是______ 。
②充电时,电池的阴极反应式是______ 。

资料:i. 在含一定量Cl−的溶液中,钴离子以CoCl42-形式存在:Co2++4Cl−
 CoCl42−
CoCl42−ii. CoCl42−溶于有机胺试剂,有机胺不溶于水。
iii. 盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:

(1)步骤ii选用盐酸的浓度应为
a. 4 mol/L b. 6 mol/L c. 10 mol/L
(2)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的
(3)步骤iv的操作是
(4)步骤vi用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钴(Co2(OH)2CO3)。实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因

(5)步骤viii中Co3O4 和Li2CO3 混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是
(6)锂离子电池的工作原理如图,充、放电过程中,Li+在LiCoO2电极和碳电极之间传递。电池的总反应为:LixC + Li1-xCoO2
 C+LiCoO2
C+LiCoO2
①放电时,电池的负极是
②充电时,电池的阴极反应式是
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】(1)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。

①正极反应为_________ 。
②当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少______ mol离子。
(2)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+

该装置工作时,阴极的电极反应:_________ ;协同转化总反应:___________ ;若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为_______ 性(碱性、中性、酸性)
(3)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池正极极增重______ g。
(4)电化学降解法可用于处理酸性硝酸盐污水,设计一电解池(如图所示)。 若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为____ g。


①正极反应为
②当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少
(2)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+

该装置工作时,阴极的电极反应:
(3)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池正极极增重
(4)电化学降解法可用于处理酸性硝酸盐污水,设计一电解池(如图所示)。 若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为

您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】(1)能源危机是当前全球问题,开源节流是应对能源危机的重要举措。下列做法有助于能源“开源节流”的是________ (填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如下图所示。
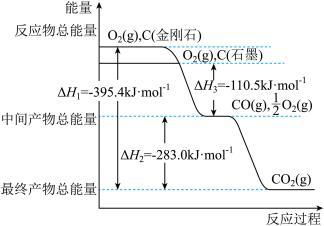
①在通常状况下,金刚石和石墨中_______ 更稳定,石墨的燃烧热为__________ 。
②12 g石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量为_______ 。
(3)由石墨转变成金刚石的反应的ΔS=+1.6J·mol-1·K-1,则为了保持此反应自发进行,温度应______ (填“低于”或“高于”)______ K。
(4)已知熔融碳酸盐燃料电池的工作原理如下图所示:
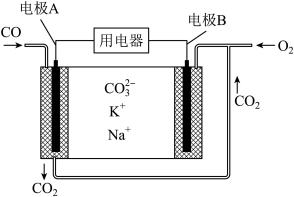
①放电过程中K+和Na+向电极_______ (填“A”或“B”)移动。
②该电池的负极反应式为_________________________ 。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如下图所示。

①在通常状况下,金刚石和石墨中
②12 g石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量为
(3)由石墨转变成金刚石的反应的ΔS=+1.6J·mol-1·K-1,则为了保持此反应自发进行,温度应
(4)已知熔融碳酸盐燃料电池的工作原理如下图所示:

①放电过程中K+和Na+向电极
②该电池的负极反应式为
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极 接通电源,经过一段时间后,乙中c电极质量增加
接通电源,经过一段时间后,乙中c电极质量增加 据此回答问题:
据此回答问题:
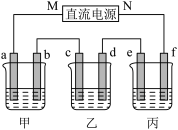
(1)电源的M端为_____________ 极;
(2)电极d上发生的电极反应式为__________ ; 乙池溶液PH__________ 填(“增大”、“减小”或“不变”)
(3)甲池中的总反应式为___________________________________ ;
(4)当电路中有0.04mol电子通过时,a、b、c、d电极上产生的气体或固体的物质的量之比是____________ ;
(5)若利用丙池实现铁上镀铜,则“e-f-x” 溶液是
溶液是__________________________ ;(要求e、f、x用具体物质回答,下同),若利用丙池实现电解精炼铜,则f电极材料是_______________________
(6) 实验测得, 1g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出22.68kJ的热量,则表示甲醇燃烧热的热化学方程式为:_____________________________________________________
(7)亚硝酸氯 结构式为
结构式为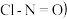 是有机合成中的重要试剂,可由
是有机合成中的重要试剂,可由 和
和 在通常反应条件下制得,反应方程式为
在通常反应条件下制得,反应方程式为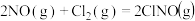 。已知几种化学键的键能数据如下表所示:
。已知几种化学键的键能数据如下表所示:
当 与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为
与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为______ kJ。(用数字和字母表示)
 接通电源,经过一段时间后,乙中c电极质量增加
接通电源,经过一段时间后,乙中c电极质量增加 据此回答问题:
据此回答问题: 
(1)电源的M端为
(2)电极d上发生的电极反应式为
(3)甲池中的总反应式为
(4)当电路中有0.04mol电子通过时,a、b、c、d电极上产生的气体或固体的物质的量之比是
(5)若利用丙池实现铁上镀铜,则“e-f-x”
 溶液是
溶液是(6) 实验测得, 1g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出22.68kJ的热量,则表示甲醇燃烧热的热化学方程式为:
(7)亚硝酸氯
 结构式为
结构式为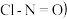 是有机合成中的重要试剂,可由
是有机合成中的重要试剂,可由 和
和 在通常反应条件下制得,反应方程式为
在通常反应条件下制得,反应方程式为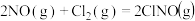 。已知几种化学键的键能数据如下表所示:
。已知几种化学键的键能数据如下表所示:| 化学键 | 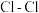 | 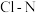 |  | 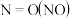 |
键能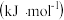 | 243 | a | 607 | 630 |
 与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为
与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为______________ 。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①该反应的平衡常数表达式为_____________ 。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如右图所示。
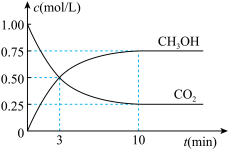
试回答:0~10 min内,氢气的平均反应速率为______________ mol/(L·min)。
(3)脱硫。
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。
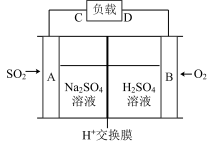
A极的电极反应式为_____________ 。
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液中的NO3-和NH4+的物质的量浓度相等,则溶液的pH__________ 7(填写“>”“=”或“<”)。
(4)金属冶炼和金属化合物处理常涉及氧化还原反应。
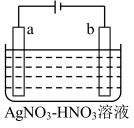
若用惰性电极电解饱和NaCl溶液一段时间当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,求所得溶液在25℃时的pH =__________ 。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3①该反应的平衡常数表达式为
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如右图所示。

试回答:0~10 min内,氢气的平均反应速率为
(3)脱硫。
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。

A极的电极反应式为
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液中的NO3-和NH4+的物质的量浓度相等,则溶液的pH
(4)金属冶炼和金属化合物处理常涉及氧化还原反应。

若用惰性电极电解饱和NaCl溶液一段时间当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,求所得溶液在25℃时的pH =
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】粉煤灰是燃煤电厂排出的主要固体废物,我国火电厂粉煤灰的主要氧化物组成为SiO2、A12O3、Fe2O3、CaO、MgO等、利用粉煤灰可制备污水处理的混凝剂(PAFC)及其他化工产品,其下艺流在如下:
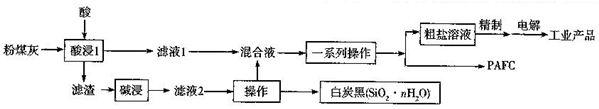
(1)PAFC名称是聚合氧化铝铁,其化学式为[Al2(OH)nCl6-n][Fe2(OH)NCl6-N]M,化学式中n、m、N、M均为整数。已知碱式氯化镁[Mg(OH)2·MgCl2],]可改写为氧化物和氯化物形式2MgO·2HCl,则PAFC改写为氧化物和氯化物形式为__________________ 。
(2)“酸浸”操作中加入的酸为_______ (填字母)
a.稀硫酸 b.浓硫酸 c.稀盐酸 d.稀硝酸
为了提高“酸浸”速率,可采取的措施为___________________ 。(填两种即可)。
(3)“碱浸"用的是NaOH溶液。该反应的离子方程式为_______________ 。
(4)“粗盐溶液”“精制”后的“电解”操作中,阴极反应为________________ 。
(5)常温时,测得流程图中“粗盐溶液”中c(Ca2+)=c(Mg2+)=0.01mol/L,若溶液中阳离子的浓度为1.0×10-5mol/L时可认为该离子除去干净,则Mg2+除干净时的pH=___ ,此时Ca2+的浓度___ 。{忽略加入碱液所导致的溶液体积变化;Ksp[Ca(OH)2] =6.0×10-6,Ksp[Mg(OH)2]=2.0×10-11,1g2=0.31}

(1)PAFC名称是聚合氧化铝铁,其化学式为[Al2(OH)nCl6-n][Fe2(OH)NCl6-N]M,化学式中n、m、N、M均为整数。已知碱式氯化镁[Mg(OH)2·MgCl2],]可改写为氧化物和氯化物形式2MgO·2HCl,则PAFC改写为氧化物和氯化物形式为
(2)“酸浸”操作中加入的酸为
a.稀硫酸 b.浓硫酸 c.稀盐酸 d.稀硝酸
为了提高“酸浸”速率,可采取的措施为
(3)“碱浸"用的是NaOH溶液。该反应的离子方程式为
(4)“粗盐溶液”“精制”后的“电解”操作中,阴极反应为
(5)常温时,测得流程图中“粗盐溶液”中c(Ca2+)=c(Mg2+)=0.01mol/L,若溶液中阳离子的浓度为1.0×10-5mol/L时可认为该离子除去干净,则Mg2+除干净时的pH=
您最近半年使用:0次
【推荐1】半湿法处理铜阳极泥回收贵金属银、铂、金的工艺如下图:
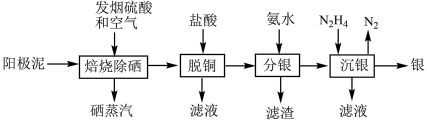
已知:①“焙烧除硒”过程中硒、铜和银转化为相应的氧化物;②“分银”工艺中银转化为[Ag(NH3)2]+。
回答下列问题:
(1)CuAgSe中铜的化合价为___________ ;Cu的价层电子轨道表达式为___________ ,位于周期表___________ 区。
(2)“脱铜”工艺中,与银元素相关的离子反应方程式为___________ 。
(3)“分银”得到滤渣的主要成分有Pt和___________ 。
(4)“沉银”过程中肼(N2H4)的作用是___________ 。
(5)经上述工艺得到的粗银还需进行电解精炼:纯银作阴极,电解液为硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是___________ (用化学语言解释)。
(6)某研究性学习小组为探究Ag与Fe3+的反应,按图装置进行实验(盐桥中的物质不参与反应)。
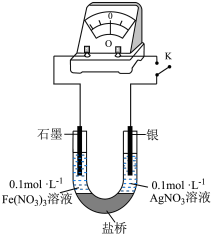
①K闭合时,电流表指针偏转,石墨作___________ (填“正极”或“负极”)。
②当指针归零后,向U形管左侧滴加几滴Fe(NO3)2浓溶液,发现指针向反方向偏转,写出此时银电极的反应式:___________ 。
③结合上述实验分析,写出Fe3+和Ag反应的离子方程式:___________ 。

已知:①“焙烧除硒”过程中硒、铜和银转化为相应的氧化物;②“分银”工艺中银转化为[Ag(NH3)2]+。
回答下列问题:
(1)CuAgSe中铜的化合价为
(2)“脱铜”工艺中,与银元素相关的离子反应方程式为
(3)“分银”得到滤渣的主要成分有Pt和
(4)“沉银”过程中肼(N2H4)的作用是
(5)经上述工艺得到的粗银还需进行电解精炼:纯银作阴极,电解液为硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是
(6)某研究性学习小组为探究Ag与Fe3+的反应,按图装置进行实验(盐桥中的物质不参与反应)。

①K闭合时,电流表指针偏转,石墨作
②当指针归零后,向U形管左侧滴加几滴Fe(NO3)2浓溶液,发现指针向反方向偏转,写出此时银电极的反应式:
③结合上述实验分析,写出Fe3+和Ag反应的离子方程式:
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。请回答下列问题:
(1)KIO3的化学名称是___________ 。
(2)KIO3具有一定的氧化性,能与H2S反应生成淡黄色沉淀,请配平该离子反应方程式: +H2S=I-+S↓+H2O,
+H2S=I-+S↓+H2O,___________ 。
(3)炒菜使用加碘盐,最好等出锅时再放盐,理由是___________ (请用化学反应方程式表示)。
(4)KIO3可采用“电解法”制备,某同学查阅资料,设计将NO2、O2和熔融盐组成的燃料电池(装置1)与装置2相连,主要原理如图所示。电解前,在a极区先将一定量的碘溶于过量KOH溶液,发生反应3I2+6KOH=5KI+KIO3+3H2O,电解后在该区获得KIO3。

①装置1,熔融盐中NO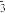 移向
移向___________ (填“石墨I”或“石墨II”);在使用过程中石墨I电极反应生成一种氧化物Y,请写出该氧化物Y的化学式是___________ 。
②请写出装置1中石墨II的电极反应式是___________ 。
③装置2,用惰性电极和不锈钢两种作为电极材料,请写出电极a可采用的材料是___________ (填“石墨”或“不锈钢”或“两者皆可”),该电极上发生的电极反应式是___________ 。
④装置2,电解过程中通过离子交换膜的离子主要是___________ ;电解后,b极区周围的pH会___________ (填“升高”或“降低”)。
(1)KIO3的化学名称是
(2)KIO3具有一定的氧化性,能与H2S反应生成淡黄色沉淀,请配平该离子反应方程式:
 +H2S=I-+S↓+H2O,
+H2S=I-+S↓+H2O,(3)炒菜使用加碘盐,最好等出锅时再放盐,理由是
(4)KIO3可采用“电解法”制备,某同学查阅资料,设计将NO2、O2和熔融盐组成的燃料电池(装置1)与装置2相连,主要原理如图所示。电解前,在a极区先将一定量的碘溶于过量KOH溶液,发生反应3I2+6KOH=5KI+KIO3+3H2O,电解后在该区获得KIO3。

①装置1,熔融盐中NO
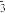 移向
移向②请写出装置1中石墨II的电极反应式是
③装置2,用惰性电极和不锈钢两种作为电极材料,请写出电极a可采用的材料是
④装置2,电解过程中通过离子交换膜的离子主要是
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】(1)天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
①以甲烷、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为___________________________ 。
②将质量相等的铁棒和石墨棒分别插入CuCl2溶液中,铁棒接甲烷燃料电池负极,石墨棒接该电池正极,一段时间后测得铁棒比石墨棒增加了6.4克。写出铁棒电极上发生的电极反应式________ ;则理论上消耗CH4的体积在标准状况下为_____ 。
(2)如图所示的实验装置中,丙为用碘化钾溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹;丁为直流电源,x、y为电源的两极;G为电流计;A、B、C、D四个电极均为石墨电极。若在两试管中充满H2SO4溶液后倒立于H2SO4溶液的水槽中,闭合K2,断开K1。

①丙电解时反应的离子方程式为______________ 。
②继续电解一段时间后,甲池中A、B极均部分被气体包围,此时断开K2,闭合K1,电流计G指针发生偏转,则B极的电极反应式为__________________ ,C极的电极反应为__________________ 。
①以甲烷、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为
②将质量相等的铁棒和石墨棒分别插入CuCl2溶液中,铁棒接甲烷燃料电池负极,石墨棒接该电池正极,一段时间后测得铁棒比石墨棒增加了6.4克。写出铁棒电极上发生的电极反应式
(2)如图所示的实验装置中,丙为用碘化钾溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹;丁为直流电源,x、y为电源的两极;G为电流计;A、B、C、D四个电极均为石墨电极。若在两试管中充满H2SO4溶液后倒立于H2SO4溶液的水槽中,闭合K2,断开K1。

①丙电解时反应的离子方程式为
②继续电解一段时间后,甲池中A、B极均部分被气体包围,此时断开K2,闭合K1,电流计G指针发生偏转,则B极的电极反应式为
您最近半年使用:0次



