名校
解题方法
1 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
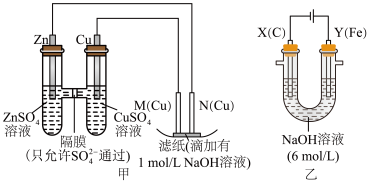
Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,
________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________________ 。
(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和_________________ 。
II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:
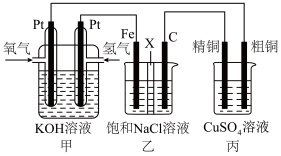
(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为____
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用________ 交换膜(填“阳离子”或“阴离子”)
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减 小”或“不变”)
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.
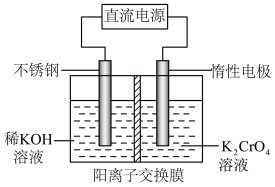
(1)不锈钢作_________ 极
(2)分析阳极区能得到重铬酸钾溶液的原因________________________________________________ 。

Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,

(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:

(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.

(1)不锈钢作
(2)分析阳极区能得到重铬酸钾溶液的原因
您最近一年使用:0次
名校
2 . 如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
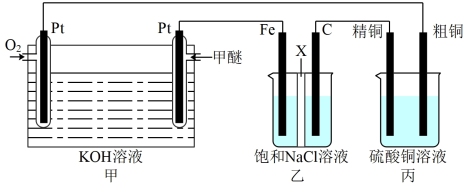
根据要求回答相关问题:
(1)通入氧气的电极为_______ (填“正极”或“负极”),写出负极的电极反应式_______ 。
(2)铁电极为_______ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______ 。反应一段时间后,乙装置中生成氢氧化钠主要在_______ (填“铁极”或“石墨极”)区。
(3)如果粗铜中含有锌、银等杂质,反应一段时间,丙装置中硫酸铜溶液浓度将_______ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,反应一段时间,丙装置中硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
您最近一年使用:0次
名校
解题方法
3 . 利用氧化还原反应可以解决很多实际问题:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O
(1)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L盐桥中装有饱和溶液。K2SO4回答下列问题:
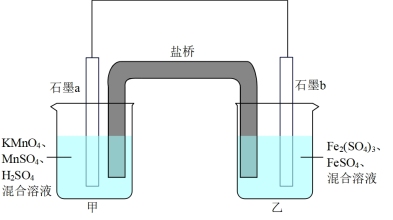
①发生氧化反应的烧杯是_______ (填“甲”或“乙”)。
②外电路的电流方向为:从_______ 。(用“a”“b”表示)
③电池工作时,盐桥中的SO 移向
移向_______ (填“甲”或“乙”)烧杯。
④甲烧杯中发生的电极反应_______ 。
(2)工业上处理含Cr2O 的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。
的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。
①电解时的电极反应:阳极_______ ,阴极_______ 。
②Cr2O 转变成Cr3+的离子反应方程式:
转变成Cr3+的离子反应方程式:_______ 。
(3)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。
①放电时负极的电极反应为:_______ ;放电时电解质溶液的pH逐渐_______ ;(填“增大”或“减小”)
②充电时有CH3OH生成的电极为_______ 极; 填“阴极”或阳极
填“阴极”或阳极 充电时每生成1 molCH3OH转移
充电时每生成1 molCH3OH转移_______ mol电子
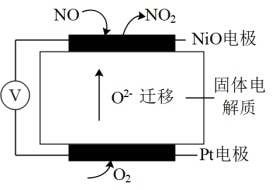
(4)通过NOx传感器可监测NOx的含量,工作原理示意图如图所示,Pt电极上发生的是_______ 反应(填“氧化”或“还原”)。写出NiO电极的电极反应式:_______ 。
(1)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L盐桥中装有饱和溶液。K2SO4回答下列问题:

①发生氧化反应的烧杯是
②外电路的电流方向为:从
③电池工作时,盐桥中的SO
 移向
移向④甲烧杯中发生的电极反应
(2)工业上处理含Cr2O
 的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。
的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。①电解时的电极反应:阳极
②Cr2O
 转变成Cr3+的离子反应方程式:
转变成Cr3+的离子反应方程式:(3)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。
①放电时负极的电极反应为:
②充电时有CH3OH生成的电极为
 填“阴极”或阳极
填“阴极”或阳极 充电时每生成1 molCH3OH转移
充电时每生成1 molCH3OH转移(4)通过NOx传感器可监测NOx的含量,工作原理示意图如图所示,Pt电极上发生的是

您最近一年使用:0次
名校
解题方法
4 . 如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
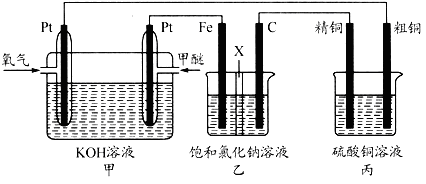
(1)通入氧气的电极为_____ (填“正极”或“负极”),写出负极的电极反应式_____ .
(2)铁电极为_____ (填“阳极”或“阴极”),石墨电极的电极反应式为_____ .
(3)反应一段时间后,乙装置中生成NaOH主要在_____ (填“铁极”或“石墨极”)区.
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_____ ,反应一段时间,硫酸铜溶液浓度将_____ (填“增大”“减小”或“不变”).
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为_____ ;丙装置中阴极析出铜的质量为_____ .

(1)通入氧气的电极为
(2)铁电极为
(3)反应一段时间后,乙装置中生成NaOH主要在
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为
您最近一年使用:0次
2017-10-14更新
|
301次组卷
|
3卷引用:宁夏银川市六盘山高级中学2017-2018学年高二上学期第一次月考化学试题



