名校
1 . 下面是常见的电化学装置图,①③④中均为惰性电极,下列说法不正确的是
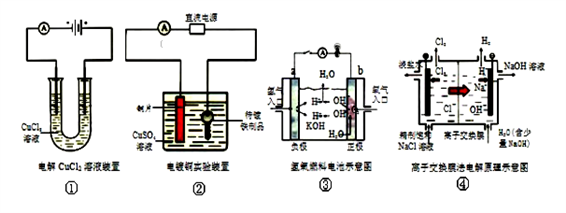

| A.装置①中正极反应式为:2Cl--2e-=Cl2,负极反应式为:Cu2++2e-=Cu |
| B.装置②中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时此时铜片和铁制品的质量差128g |
| C.装置③中b极为正极,该极的电极反应方程式为O2+2H2O+4e-=4OH- |
| D.装置④阴极的纯水中加入NaOH的作用是:增大离子浓度,增强溶液的导电性 |
您最近一年使用:0次
名校
2 . 某小组为研究电化学原理,设计如图装置。下列叙述正确的是
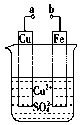

| A.a和b不连接时,铁片上会发生氧化反应而质量减少 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu-2e-===Cu2+ |
| C.无论a和b是否连接,铁片均会被氧化,溶液均有Fe2+生成 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
您最近一年使用:0次
名校
3 . 高铁电池是一种新型可充电电池,能长时间保持稳定的放电电压。其电池总反应为:3Zn + 2K2FeO4 + 8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述错误 的是
 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述| A.放电时负极反应为:Zn-2e-+2OH-= Zn(OH)2 |
| B.充电时阳极发生氧化反应,附近溶液碱性增强 |
| C.充电时每转移3mol电子,阴极有1.5molZn生成 |
| D.放电时正极反应为:FeO42- + 3e- + 4H2O = Fe(OH)3 + 5OH- |
您最近一年使用:0次
2018-03-19更新
|
725次组卷
|
10卷引用:宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题
宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题安徽省淮北市第一中学2017-2018学年高二下学期第一次月考化学试题2【全国百强校】福建省厦门外国语学校2017-2018学年高二下学期期中考试化学试题【全国百强校】福建省师范大学附属中学2018-2019学年高二(理)上学期期中考试化学试题福建省惠安惠南中学2018-2019学年高二上学期期中考试化学试题【全国百强校】河南省实验中学2018-2019学年高二上学期期中考试化学试题广东省汕头市2018届高三第一次(3月)模拟考试理综化学试题2020届高三化学知识点强化训练----化学能与电能(已下线)【浙江新东方】绍兴qw135江西省龙南中学2022-2023学年高一下学期6月期末考试化学试题
名校
解题方法
4 . 如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.根据要求回答相关问题:
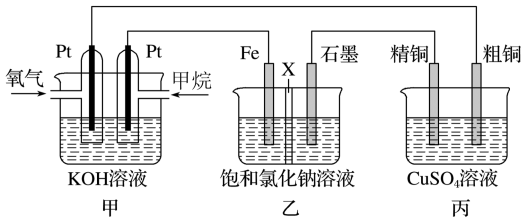
(1)甲烷燃料电池的负极反应式______ .
(2)石墨电极(C)的电极反应式为______ .
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将______ (填“增大”“减小”或“不变”).
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成标况下气体的的体积为______ ;丙装置中阴极析出铜的质量为______ .

(1)甲烷燃料电池的负极反应式
(2)石墨电极(C)的电极反应式为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成标况下气体的的体积为
您最近一年使用:0次
名校
5 . 如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )
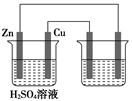

| A.铜在原电池中作负极,在电镀池中作阳极 |
| B.原电池溶液增加的质量比电镀池阴极增加的质量大 |
| C.锌棒每减少0.65 g,导线上转移的电子就为0.02 mol |
| D.电镀池中的电解质溶液可用ZnSO4溶液 |
您最近一年使用:0次
2017-12-20更新
|
452次组卷
|
5卷引用:宁夏育才中学孔德校区2017-2018学年高二12月月考化学试题
名校
解题方法
6 . 铝—空气燃料电池具有原料易得、能量密度高等优点,装置如图所示,电池的电解质溶液为KOH溶液。下列说法正确的是
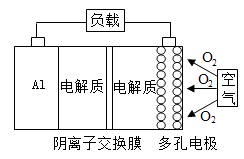

| A.放电时,消耗氧气22.4 L(标准状况),有4 mol OH-从左往右通过阴离子交换膜 |
| B.充电时,电解池阳极区的电解质溶液中c(OH-)逐渐增大 |
| C.放电过程的负极反应式:Al+3OH--3e-=Al(OH)3↓ |
| D.充电时,铝电极上发生还原反应 |
您最近一年使用:0次
2017-12-06更新
|
1271次组卷
|
6卷引用:宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题
14-15高三上·山东济南·期末
名校
7 . 将如图所示实验装置的K闭合,下列判断正确的是
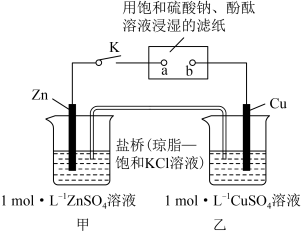

| A.Cu 电极上发生氧化反应 | B.电子沿 Zn→a→b→Cu 路径流动 |
| C.片刻后可观察到滤纸a点变红色 | D.片刻后甲池中c(SO42-)增大 |
您最近一年使用:0次
2017-07-29更新
|
254次组卷
|
5卷引用:宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】
名校
8 . 如图所示:
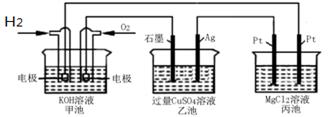
下列说法正确的是

下列说法正确的是
| A.甲池通入O2的电极反应为O2 + 4e-+ 4H+=2H2O |
| B.乙池 Ag电极增重6.4g,溶液中将转移0.2mol电子 |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 |
| D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体 |
您最近一年使用:0次
2016-12-09更新
|
854次组卷
|
5卷引用:宁夏石嘴山市第三中学2022-2023学年高二下学期第一次月考化学(理)试题
名校
9 . 锌溴液流电池用溴化锌溶液作电解液,并在电池间不断循环。下列有关说法正确的是
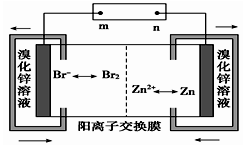

| A.充电时Zn2+通过阳离子交换膜由左侧流向右侧 |
| B.放电时每转移2mol电子负极增重130g |
| C.充电时阴极的电极反应式为Br2+2e-=2Br- |
| D.若将电解液改为氯化锌溶液放电效果更好更安全 |
您最近一年使用:0次
2016-12-09更新
|
245次组卷
|
4卷引用:宁夏银川市第一中学2016-2017学年高二下学期期中考试化学试题
宁夏银川市第一中学2016-2017学年高二下学期期中考试化学试题2016届安徽省安庆市高三第二次模拟考试理综化学试卷(已下线)二轮复习 专题10 电化学及其应用 押题专练(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(押题专练)
名校
解题方法
10 . 下图是一个化学过程的示意图。
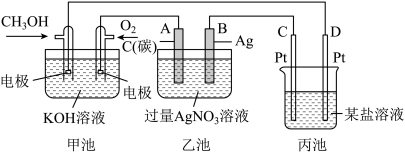
(1)图中甲池中OH-移向_________ 极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式:_____________________ 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为___________ 极(填“A”或"B”),并写出此电极的反应式:________________________ 。
(4)乙池中总反应的离子方程式:_________________________ 。
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是_______________ (若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是__________ (填序号)。

(1)图中甲池中OH-移向
(2)写出通入CH3OH的电极的电极反应式:
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为
(4)乙池中总反应的离子方程式:
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是
| A.MgSO4 | B.CuSO4 | C.AgNO3 | D.AlCl3 |
您最近一年使用:0次
2016-12-09更新
|
386次组卷
|
4卷引用:宁夏银川市第一中学2016-2017学年高二下学期期中考试化学试题



