名校
1 . 化学能和电能的相互转化应用于各个领域。回答下列问题:
(1)硫酸是铅酸蓄电池的电解质,在铅酸蓄电池中负极的电极反应式是___________ 。
(2)“反应2”是2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5CO↑+7H2O,其中体现氧化性和还原性的反应物的物质的量之比为___________ 。
(3)利用LiFePO4作电极的电池稳定、安全、对环境友好,放电时工作原理如图所示。
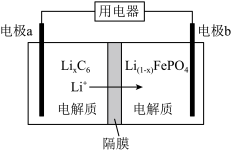
①电极a是该电池的___________ (填“正极”或“负极”),
②充电时电极a的电极反应式为___________ 。
③放电时电极b的电极反应式为___________ 。
(1)硫酸是铅酸蓄电池的电解质,在铅酸蓄电池中负极的电极反应式是
(2)“反应2”是2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5CO↑+7H2O,其中体现氧化性和还原性的反应物的物质的量之比为
(3)利用LiFePO4作电极的电池稳定、安全、对环境友好,放电时工作原理如图所示。

①电极a是该电池的
②充电时电极a的电极反应式为
③放电时电极b的电极反应式为
您最近半年使用:0次
名校
2 . 大气中过量的 和水体中过量的
和水体中过量的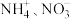 均是污染物。利用钒电池电解含
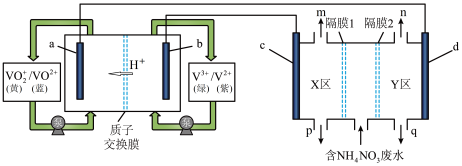
均是污染物。利用钒电池电解含 的废水制备硝酸和氨水的原理如下图所示,
的废水制备硝酸和氨水的原理如下图所示,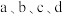 均为惰性电极。下列说法中正确的是
均为惰性电极。下列说法中正确的是
 和水体中过量的
和水体中过量的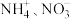 均是污染物。利用钒电池电解含
均是污染物。利用钒电池电解含 的废水制备硝酸和氨水的原理如下图所示,
的废水制备硝酸和氨水的原理如下图所示,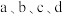 均为惰性电极。下列说法中正确的是
均为惰性电极。下列说法中正确的是
A.用钒电池处理废水时, 电极区溶液由绿色变成紫色 电极区溶液由绿色变成紫色 |
B. 为阴极, 为阴极, 为阳极 为阳极 |
| C.隔膜1为阴离子交换膜 |
D.当钒电池有 通过质子交换膜时,共处理含 通过质子交换膜时,共处理含 的废水 的废水 |
您最近半年使用:0次
名校
3 . Ⅰ.化学电源在生产生活中有着广泛的应用,请回答下列问题。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是______。
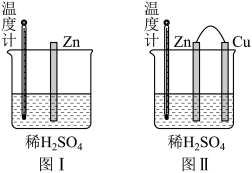
(2)为了探究化学反应能量变化,某同学设计了两个实验(如图Ⅰ,Ⅱ)。有关实验现象,说法正确的是:_______。
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为:___________ 。
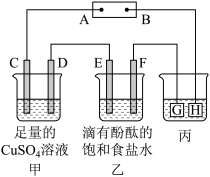
(4)以上述氨燃料电池接下图(甲乙丙) A、B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:_____ ,C电极反应式:_____ ,乙池中发生的离子反应方程式为:_____ ,丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在_____ 处(填G或H)。为证明铁被保护,可先取少量电解后溶液于试管中,向溶液中加入_____ 溶液观察颜色变化。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是______。
A.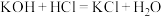 | B. |
C.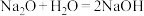 | D. |
(2)为了探究化学反应能量变化,某同学设计了两个实验(如图Ⅰ,Ⅱ)。有关实验现象,说法正确的是:_______。

| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 | B.图Ⅰ和图Ⅱ中温度计示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ中的气泡均产生于锌棒表面 | D.图Ⅱ中产生气体的速率比Ⅰ慢 |
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:
 ,该电池负极的电极反应为:
,该电池负极的电极反应为:(4)以上述氨燃料电池接下图(甲乙丙) A、B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:

您最近半年使用:0次
名校
4 . 下图是一个化学过程的示意图,请回答下列问题:
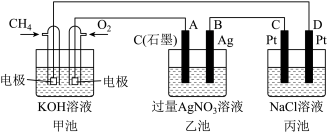
(1)图中甲池是___________ 装置,乙池是___________ 装置。
(2)通入O2的电极的电极反应式为___________ ,通入CH4的电极的电极反应式为___________ 。
(3)乙池中反应的化学方程式为___________ 。
(4)一段时间后,当丙中共产生112ml(标准状况)气体时,均匀搅拌丙池,所得溶液在室温时的pH=___________ (已知NaCl溶液足量,电解后溶液体积为500ml),若要使丙池恢复电解前的状态,应向丙池通入___________ (填化学式)
(5)在A、B、C、D各电极上析出生成物的物质的量之比为___________ 。

(1)图中甲池是
(2)通入O2的电极的电极反应式为
(3)乙池中反应的化学方程式为
(4)一段时间后,当丙中共产生112ml(标准状况)气体时,均匀搅拌丙池,所得溶液在室温时的pH=
(5)在A、B、C、D各电极上析出生成物的物质的量之比为
您最近半年使用:0次
名校
5 . 能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。如图所示的装置,X、Y都是惰性电极。丙为电解精炼铜的装置。试回答下列问题:
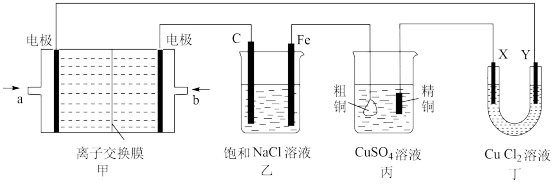
(1)甲装置是甲烷燃料电池(电解质溶液为 溶液)的结构示意图,则a处通入的是
溶液)的结构示意图,则a处通入的是___________ (填“ ”或“
”或“ ”),电极上发生的电极反应是
”),电极上发生的电极反应是___________ 。
(2)在乙装置中,总反应的离子方程式是___________ 。向乙中滴入酚酞溶液,___________ 电极附近溶液先变红(填“C”或“Fe”)。
(3)如果丙装置中精铜电极的质量增加了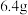 ,则甲装置中消耗的
,则甲装置中消耗的 的质量为
的质量为___________ g。
(4)丁装置中在电解初期,Y电极上发生的电极反应是___________ 。
(5)燃料电池是一种绿色环保、高效的化学电源。若用甲装置电解 硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体
硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体 ,则电路中共转移
,则电路中共转移___________  电子。
电子。

(1)甲装置是甲烷燃料电池(电解质溶液为
 溶液)的结构示意图,则a处通入的是
溶液)的结构示意图,则a处通入的是 ”或“
”或“ ”),电极上发生的电极反应是
”),电极上发生的电极反应是(2)在乙装置中,总反应的离子方程式是
(3)如果丙装置中精铜电极的质量增加了
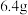 ,则甲装置中消耗的
,则甲装置中消耗的 的质量为
的质量为(4)丁装置中在电解初期,Y电极上发生的电极反应是
(5)燃料电池是一种绿色环保、高效的化学电源。若用甲装置电解
 硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体
硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体 ,则电路中共转移
,则电路中共转移 电子。
电子。
您最近半年使用:0次
名校
解题方法
6 . 化学性质类似 的盐酸羟胺
的盐酸羟胺 是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法错误的是
的酸性废水的装置。下列说法错误的是

 的盐酸羟胺
的盐酸羟胺 是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法错误的是
的酸性废水的装置。下列说法错误的是
| A.图1电池工作时,Pt电极是正极 |
B.图2中,A为 ,B为 ,B为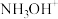 |
C.电极b接电源负极,处理 ,电路中转移 ,电路中转移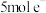 |
D.电池工作时,每消耗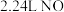 (标准状况),左室溶液质量增加 (标准状况),左室溶液质量增加 |
您最近半年使用:0次
7 . 中科大研究构建的宽温氢氯电池如图所示,能在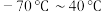 范围内使用并实现多次充放电。下列说法
范围内使用并实现多次充放电。下列说法错误 的是
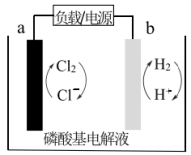
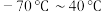 范围内使用并实现多次充放电。下列说法
范围内使用并实现多次充放电。下列说法
| A.磷酸基电解液具有抗冻性 |
B.放电时,电子从 极经导线流向 极经导线流向 极 极 |
| C.电极具有多孔结构,能够实现气体循环使用 |
D.充电时,阳极电极反应式为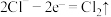 |
您最近半年使用:0次
8 . 甲烷燃料电池采用铂做电极材料,两个电极上分别通入 和
和 ,电解质溶液为
,电解质溶液为 溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀的实验,如图所示,其中乙装置中X为离子交换膜。下列说法错误的是
溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀的实验,如图所示,其中乙装置中X为离子交换膜。下列说法错误的是

 和
和 ,电解质溶液为
,电解质溶液为 溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀的实验,如图所示,其中乙装置中X为离子交换膜。下列说法错误的是
溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀的实验,如图所示,其中乙装置中X为离子交换膜。下列说法错误的是
A.甲烷燃料电池负极电极反应式是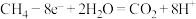 |
| B.乙中X为阳离子交换膜 |
| C.用丙装置给铜镀银,b应是Ag |
D.当电路中通过 时,乙中Fe电极上产生氯气 时,乙中Fe电极上产生氯气 (标准状况) (标准状况) |
您最近半年使用:0次
9 . 锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为 ,含少量
,含少量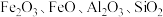 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
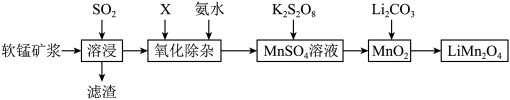
(1)溶浸生产中为提高 吸收率可采取的措施有___________(填序号)。
吸收率可采取的措施有___________(填序号)。
(2)X可选择的最佳试剂是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
(3)由硫酸锰与 (过硫酸钾,结构为
(过硫酸钾,结构为 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。 中
中 原子的化合价为
原子的化合价为___________ ,S原子的杂化方式为___________ 。
(4)将 和
和 按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。该反应的化学方程式为
并生两种气体。该反应的化学方程式为___________ 。
(5)锰酸锂可充电电池的总反应为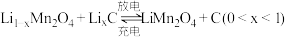
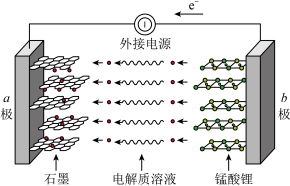
①放电时,电池正极的电极反应式为___________ 。
②充电时, 向
向___________ 极移动(填“a”或“b”)。
 ,含少量
,含少量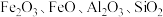 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
(1)溶浸生产中为提高
 吸收率可采取的措施有___________(填序号)。
吸收率可采取的措施有___________(填序号)。A.不断搅拌,使 和软锰矿浆充分接触 和软锰矿浆充分接触 | B.减小通入 的流速 的流速 |
| C.减少软锰矿浆的进入量 | D.增大通入 的流速 的流速 |
(2)X可选择的最佳试剂是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液(3)由硫酸锰与
 (过硫酸钾,结构为
(过硫酸钾,结构为 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。 中
中 原子的化合价为
原子的化合价为(4)将
 和
和 按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。该反应的化学方程式为
并生两种气体。该反应的化学方程式为(5)锰酸锂可充电电池的总反应为
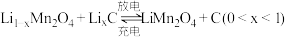

①放电时,电池正极的电极反应式为
②充电时,
 向
向
您最近半年使用:0次
名校
10 . 2023年星恒电源发布“超钠F1”开启钠电在电动车上产业化元年。该二次电池的电极材料为 (普鲁士白)和
(普鲁士白)和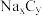 (嵌钠硬碳)。下列说法错误的是
(嵌钠硬碳)。下列说法错误的是
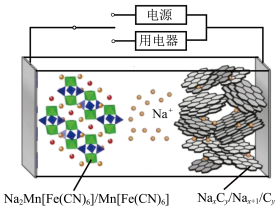
 (普鲁士白)和
(普鲁士白)和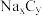 (嵌钠硬碳)。下列说法错误的是
(嵌钠硬碳)。下列说法错误的是
| A.放电时,左边电极电势高 |
B.放电时,负极的电极反应式可表示为: |
C.充电时,用铅酸蓄电池作电源,负极质量增重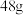 ,则阳极质量增加 ,则阳极质量增加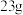 |
| D.其他条件相同时,锂离子电池比能量高于钠离子电池 |
您最近半年使用:0次



