1 . 一种可充放电的铝离子电池工作原理如图所示,电解质为AlxCly离子液体,CuS在电池反应后转化为Cu2S和Al2S3。下列说法错误的是


| A.若CuS从电极表面脱落,则电池单位质量释放电量减少 |
B.放电时电池负极的电极反应中,消耗1molAl的同时消耗7molAlCl |
C.该电池充电时,阳极反应为: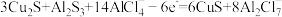 |
| D.为提高电池效率,可以向CuS@C电极附近加入适量AlCl3水溶液 |
您最近一年使用:0次
解题方法
2 . 《X-MOL》报道了一种两相无膜锌/吩噻嗪电池,其放电时的工作原理如图所示( 在水系/非水系电解液界面上来回穿梭,维持电荷守恒)。
在水系/非水系电解液界面上来回穿梭,维持电荷守恒)。
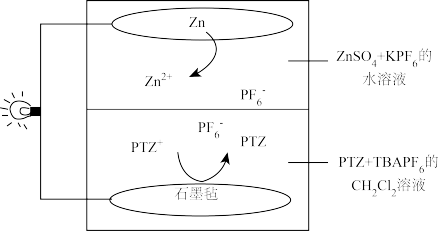
已知: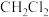 的密度为
的密度为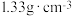 ,难溶于水。下列说法错误的是
,难溶于水。下列说法错误的是
 在水系/非水系电解液界面上来回穿梭,维持电荷守恒)。
在水系/非水系电解液界面上来回穿梭,维持电荷守恒)。
已知:
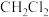 的密度为
的密度为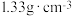 ,难溶于水。下列说法错误的是
,难溶于水。下列说法错误的是| A.电池使用时不能倒置 |
B.充电时,石墨毡上的电极反应式为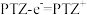 |
C.放电时, 由 由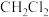 层移向水层 层移向水层 |
| D.放电时,Zn板每减轻6.5g,水层增重29g |
您最近一年使用:0次
2021-12-30更新
|
630次组卷
|
4卷引用:山东省临沂市临沭县2021-2022学年高三上学期期末考试化学试题
3 . 电解原理在化学工业中有广泛应用。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
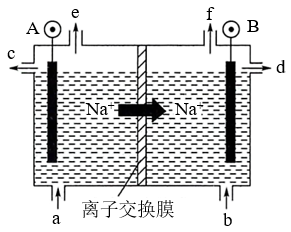
①电解饱和食盐水的总反应的离子方程式是___________ 。
②精制饱和食盐水在b口加入的物质为___________ (写化学式)
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
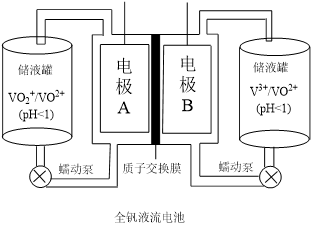
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是___________ 。
②当完成储能时,阴极溶液的颜色是___________
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
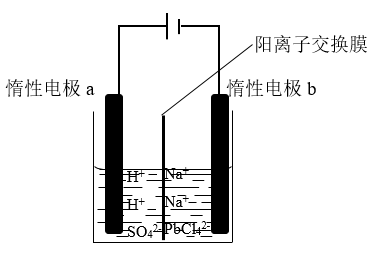
①写出电解时阴极的电极反应式___________
②电解过程中通过阳离子交换膜的离子主要为___________
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向___________ 极室(填“阴”或者“阳”)加入___________ (填化学式)。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

①电解饱和食盐水的总反应的离子方程式是
②精制饱和食盐水在b口加入的物质为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
| 离子种类 | VO | VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |

①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是
②当完成储能时,阴极溶液的颜色是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近一年使用:0次
2021-11-10更新
|
1575次组卷
|
8卷引用:山东省嘉祥县第一中学2022-2023学年高二上学期期末考试化学试题
山东省嘉祥县第一中学2022-2023学年高二上学期期末考试化学试题山东省实验中学2021-2022学年高二上学期期中化学试题山东省枣庄滕州市第一中学2022-2023学年高二上学期10月月考化学试题山东省新泰市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)4.3.1 电解原理-2021-2022学年高二化学课后培优练(人教版选修4)第四章化学反应与电能福建省厦门集美中学2022-2023学年高二上学期第一次月考(10月)化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
4 . 在如图串联装置中,通电片刻即发现乙装置左侧电极表面出现红色固体,则下列说法不正确的是


| A.标准状况下当甲中产生4.48L气体时,丙中Cu电极质量增加21.6g |
| B.电解过程中丙中溶液酸碱性无变化 |
| C.向甲中加入适量的盐酸,可使溶液恢复到电解前的状态 |
D.乙中左侧电极反应式: |
您最近一年使用:0次
2021-10-23更新
|
615次组卷
|
6卷引用:山东省枣庄一中分校2021-2022学年高二上学期期末考试化学试题
山东省枣庄一中分校2021-2022学年高二上学期期末考试化学试题安徽省六安第一中学2021-2022学年高二上学期期末考试化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)专题31 多池串联的模型-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)黑龙江省大庆市东风中学2022-2023学年高二10月月考化学试题(已下线)专题09 串联电解池(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
名校
解题方法
5 . 新能源汽车是国家战略产业的重要组成部分, 电池是能源汽车关键部件之一,其工作原理如图所示,电池工作时的总反应为
电池是能源汽车关键部件之一,其工作原理如图所示,电池工作时的总反应为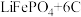


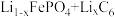 。下列说法错误的是
。下列说法错误的是
 电池是能源汽车关键部件之一,其工作原理如图所示,电池工作时的总反应为
电池是能源汽车关键部件之一,其工作原理如图所示,电池工作时的总反应为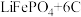


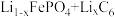 。下列说法错误的是
。下列说法错误的是
| A.充电时,电极a与电源负极连接,电极b与电源正极连接 |
B.电池工作时,正极的电极反应为 |
| C.电池工作时,负极材料质量减少1.4g,转移0.4mol电子 |
| D.电池进水将会大大降低其使用寿命 |
您最近一年使用:0次
2021-10-13更新
|
1172次组卷
|
9卷引用:山东省枣庄一中分校2021-2022学年高二上学期期末考试化学试题
名校
解题方法
6 . 相同金属在其不同浓度盐溶液中可形成浓差电池。如下图所示装置是利用浓差电池电解 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和NaOH。下列说法正确的是
和NaOH。下列说法正确的是
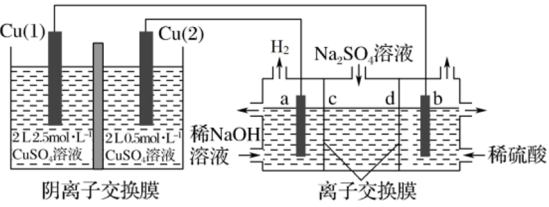
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和NaOH。下列说法正确的是
和NaOH。下列说法正确的是
A.a电极的电极反应为: |
| B.c、d离子交换膜依次为阴离子交换膜和阳离子交换膜 |
C.电池放电过程中,Cu(2)电极上的电极反应为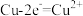 |
D.电池从开始工作到停止放电,电解池阳极区理论上可生成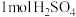 |
您最近一年使用:0次
2021-08-07更新
|
912次组卷
|
5卷引用:山东省淄博市2020-2021学年高二下学期期末考试化学试题
山东省淄博市2020-2021学年高二下学期期末考试化学试题山东省滕州第一中学2021-2022学年高二上学期第一学段模块考试(期中)化学试题山东省枣庄滕州市第一中学2022-2023学年高二上学期10月月考化学试题山东省青岛超银高级中学2023-2024学年高二下学期期初考试化学试卷(已下线)1.2.3 电解池的工作原理及应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)
7 . 如图所示,某同学以酸性介质的甲醇-氧气燃料电池,在钢材上电镀铝。下列说法正确的是
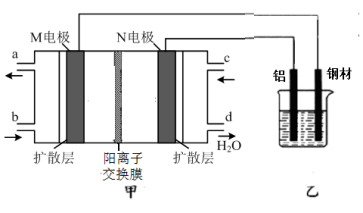

| A.甲装置放电时,电池中的H+向左槽移动 |
| B.M电极的电极反应式为CH3OH-6e-+H2O=CO2+6H+ |
| C.通电前铝和钢材的质量相等,电解一段时间后铝和钢材的质量差增大到5.4g,则理论上甲装置中消耗氧气的体积为1.12 L(标准状况下) |
| D.乙装置中的电解液可以选用氯化铝溶液 |
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组在实验室中设计如图所示装置(a、b、c、d均为惰性电极),以去离子水和氧气为原料通过电解法制备双氧水。下列分析错误的是
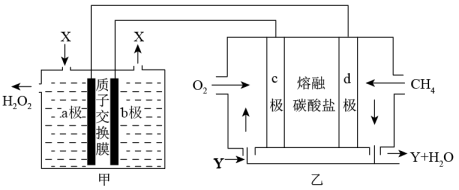

| A.气体X为O2,气体Y为CO2 |
| B.一段时间后,甲装置中生成的X与消耗的X等量 |
C.乙装置中,d极上发生氧化反应,CO 移向该电极 移向该电极 |
D.乙装置中,c极的电极反应式为:O2+4e-+2CO2=2CO |
您最近一年使用:0次
名校
解题方法
9 . 电化学知识在生产、科技研究中应用广泛。
(1)可采用电化学防护技术减缓海水中钢铁设施的腐蚀,下图是钢铁桥墩部分防护原理示意图。

①K 与 M 连接时钢铁桥墩的电化学防护方法为______ 。
②K与N连接时,钢铁桥墩为______ 极(填"正"、"负"、"阴"或"阳"),电极反应式为______ 。
(2) 燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示。
燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示。
电池工作时,A极区 NaOH浓度不变,则离子交换膜为______ (填"阳离子交换膜"或"阴离子交换膜");电极 B的电极反应式为______ ;电池工作时参加反应的 =
=______ 。
(1)可采用电化学防护技术减缓海水中钢铁设施的腐蚀,下图是钢铁桥墩部分防护原理示意图。

①K 与 M 连接时钢铁桥墩的电化学防护方法为
②K与N连接时,钢铁桥墩为
(2)
 燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示。
燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示。
电池工作时,A极区 NaOH浓度不变,则离子交换膜为
 =
=
您最近一年使用:0次
2021-02-01更新
|
293次组卷
|
3卷引用:山东省聊城市2020-2021学年高二上学期期末考试化学试题
山东省聊城市2020-2021学年高二上学期期末考试化学试题四川省成都市大弯中学校2022届高三9月月考化学试题(已下线)第四章第四节 金属的电化学腐蚀与防护(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)
解题方法
10 . 水体中的含氮化合物是引起富营养化的主要污染物,控制水体中的含氮污染物,对水资源的循环利用意义重大。
25℃时,亚硝酸( )和连二次硝酸(
)和连二次硝酸( )的电离常数如下表所示:
)的电离常数如下表所示:
(1)下列不能说明 是弱电解质的是
是弱电解质的是___________ (填序号)。
A.室温下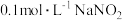 溶液的
溶液的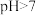
B.用一定浓度的 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗
C.等pH、等体积的盐酸和 溶液分别与足量锌反应,
溶液分别与足量锌反应, 溶液放出的氢气较多
溶液放出的氢气较多
(2) 溶液呈
溶液呈___________ 性(填“酸”“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)室温下,物质的量浓度相同的溶液: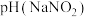
___________ 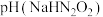 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)25℃时,用 的
的 溶液滴定
溶液滴定 溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为
溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为___________ 。
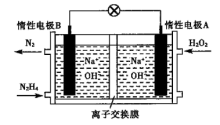
(5)亚硝酸盐对人体健康的损害不亚于农药,可采用电解含 、
、 废水的方法除去
废水的方法除去 (生成物为
(生成物为 ,同时再生
,同时再生 ,其原理如图所示。
,其原理如图所示。
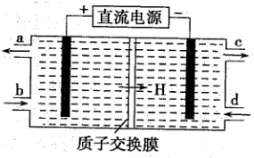
① 从电解槽的
从电解槽的___________ (填字母)口流出。
②写出阴极的电极反应式___________ 。
(6)新的研究表明,将含 的废水与含
的废水与含 的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为
的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为___________ 。
25℃时,亚硝酸(
 )和连二次硝酸(
)和连二次硝酸( )的电离常数如下表所示:
)的电离常数如下表所示:| 化学式 |  |  |
| 电离常数 | 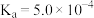 | 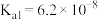 、 、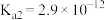 |
(1)下列不能说明
 是弱电解质的是
是弱电解质的是A.室温下
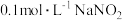 溶液的
溶液的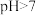
B.用一定浓度的
 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗C.等pH、等体积的盐酸和
 溶液分别与足量锌反应,
溶液分别与足量锌反应, 溶液放出的氢气较多
溶液放出的氢气较多(2)
 溶液呈
溶液呈(3)室温下,物质的量浓度相同的溶液:
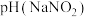
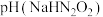 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)25℃时,用
 的
的 溶液滴定
溶液滴定 溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为
溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为(5)亚硝酸盐对人体健康的损害不亚于农药,可采用电解含
 、
、 废水的方法除去
废水的方法除去 (生成物为
(生成物为 ,同时再生
,同时再生 ,其原理如图所示。
,其原理如图所示。
①
 从电解槽的
从电解槽的②写出阴极的电极反应式
(6)新的研究表明,将含
 的废水与含
的废水与含 的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为
的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为
您最近一年使用:0次



