17. 氮及其化合物是氮肥工业等无机化工的重要原料。
(1)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1molN
2和3molH
2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如表:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则从反应开始到25min时,以N
2表示的平均反应速率=
_______。
(2)一定温度下,向一个容积为2L的密闭容器中通入2molN
2和7molH
2,达到平衡时测得容器的压强为起始时的7/9倍,在同一温度,同一容器中,将起始物质改为amolN
2,bmolH
2,cmolNH
3(a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,且反应在起始时向逆反应方向进行,c的取值范围是
_______。
(3)工业上利用氨气生产氢氰酸(HCN)的反应为:CH
4(g)+NH
3(g)⇌HCN(g)+3H
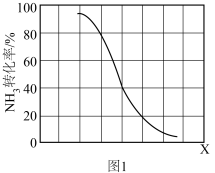
2(g) ∆H>0,在其他条件一定,该反应达到平衡时NH
3转化率随外界条件X变化的关系如图1所示,X代表_______(填字母代号)。
(4)在容积为1.00L的容器中,通入一定量的N
2O
4,发生反应N
2O
4(g)⇌2NO
2(g),随温度升高,混合气体的颜色变深。100℃时达到平衡后,改变反应温度为T,c(N
2O
4)逐渐减小,经10s又达到平衡。T
_______100℃(填“大于”“小于”)。温度T时反应达平衡后,将反应容器的容积减少一半,平衡向
_______(填“正反应”或“逆反应”)方向移动,判断理由是
_______。
(5)已知2NO(g)+O
2(g)⇌2NO
2(g)∆H的反应历程分两步:
①2NO(g)⇌N
2O
2(g)(快) ∆H
1<0,v
1正=k
1正c
2(NO),v
1逆=k
1逆c
2(N
2O
2)
②N
2O
2(g)+O
2(g)⇌2NO
2(g)(慢) ∆H
2<0,v
2正=k
2正c
2(N
2O
2)·c(O
2),v
2逆=k
2逆c
2(NO
2)
比较反应①的活化能E
1与反应②的活化能E
2的大小:E
1_______E
2(填“>”、“<”或“=”)其判断理由是
_______;2NO(g)+O
2(g)⇌2NO
2(g)的平衡常数K与上述反应速率常数k
1正、k
1逆、k
2正、k
2逆的关系式为
_______。
(6)以乙烯(C
2H
4)作为还原剂脱硝(NO),其脱硝机理如图2所示,若反应中n(NO):n(O
2)=2:1,则总反应的化学方程式为
_______。
