名校
1 . 某蓄电池的反应为:NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)该蓄电池充电时,发生还原反应的物质是________ (填选项字母)。放电时生成Fe(OH)2的质量为18 g,则外电路中转移的电子数是________________ 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常在船体上镶嵌Zn块,该电化学防护法称为________________ 。
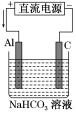
(3)以该蓄电池作电源,用如图所示的装置在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是_________ (用相关的电极反应式和离子方程式表示)。
(4)精炼铜时,粗铜应与直流电源的________ (填“正”或“负”)极相连。
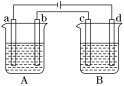
(5)如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05 mol·L-1的CuCl2溶液,B池中加入0.1 mol·L-1的AgNO3溶液,进行电解。a、b、c、d四个电极上所析出的物质的物质的量之比是____________ 。
 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2 (1)该蓄电池充电时,发生还原反应的物质是
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常在船体上镶嵌Zn块,该电化学防护法称为
(3)以该蓄电池作电源,用如图所示的装置在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是

(4)精炼铜时,粗铜应与直流电源的
(5)如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05 mol·L-1的CuCl2溶液,B池中加入0.1 mol·L-1的AgNO3溶液,进行电解。a、b、c、d四个电极上所析出的物质的物质的量之比是

您最近一年使用:0次
解题方法
2 . 如图装置闭合电键K时,电流计A的指针将发生偏转。试回答:
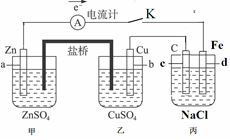
(1) 丙池是____________ (填“原电池”或“电解池”),甲中a极电极名称是________________ ,丙中c极电极名称是_____________________ ;
(2)乙中Cu极的电极反应式是__________ ,若电路中有0.02mol电子通过,则甲中a电极溶解的质量为__________ g;
(3)闭合电键K一段时间后,丙池中生成两种气体和一种碱,则丙池中发生的总的化学方程式是_________________ ;
(4)丙池中反应进行较长时间后,收集到标准状况下氢气2.24L,此时测得丙池溶液质量实际减少4.23 g,含有碱0.100mol(不考虑气体在水中的溶解),则实际放出气体的物质的量是______________ mol;
(5)如果要给丙中铁片上镀上一层Cu,则丙池应作何改进_________________________ 。

(1) 丙池是
(2)乙中Cu极的电极反应式是
(3)闭合电键K一段时间后,丙池中生成两种气体和一种碱,则丙池中发生的总的化学方程式是
(4)丙池中反应进行较长时间后,收集到标准状况下氢气2.24L,此时测得丙池溶液质量实际减少4.23 g,含有碱0.100mol(不考虑气体在水中的溶解),则实际放出气体的物质的量是
(5)如果要给丙中铁片上镀上一层Cu,则丙池应作何改进
您最近一年使用:0次
2016-12-09更新
|
716次组卷
|
3卷引用:海南省海南枫叶国际学校2019-2020学年高二上学期期末考试化学试题
海南省海南枫叶国际学校2019-2020学年高二上学期期末考试化学试题(已下线)2011-2012学年湖北省公安三中高二3月考试化学试卷四川省邛崃市高埂中学2019-2020学年度高二下学期期中考试化学试题



