1 . 半湿法处理铜阳极泥回收贵金属银、铂、金的工艺如下图:
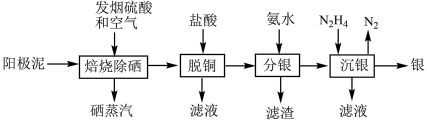
已知:①“焙烧除硒”过程中硒、铜和银转化为相应的氧化物;②“分银”工艺中银转化为[Ag(NH3)2]+。
回答下列问题:
(1)CuAgSe中铜的化合价为___________ ;Cu的价层电子轨道表达式为___________ ,位于周期表___________ 区。
(2)“脱铜”工艺中,与银元素相关的离子反应方程式为___________ 。
(3)“分银”得到滤渣的主要成分有Pt和___________ 。
(4)“沉银”过程中肼(N2H4)的作用是___________ 。
(5)经上述工艺得到的粗银还需进行电解精炼:纯银作阴极,电解液为硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是___________ (用化学语言解释)。
(6)某研究性学习小组为探究Ag与Fe3+的反应,按图装置进行实验(盐桥中的物质不参与反应)。
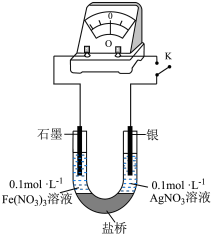
①K闭合时,电流表指针偏转,石墨作___________ (填“正极”或“负极”)。
②当指针归零后,向U形管左侧滴加几滴Fe(NO3)2浓溶液,发现指针向反方向偏转,写出此时银电极的反应式:___________ 。
③结合上述实验分析,写出Fe3+和Ag反应的离子方程式:___________ 。

已知:①“焙烧除硒”过程中硒、铜和银转化为相应的氧化物;②“分银”工艺中银转化为[Ag(NH3)2]+。
回答下列问题:
(1)CuAgSe中铜的化合价为
(2)“脱铜”工艺中,与银元素相关的离子反应方程式为
(3)“分银”得到滤渣的主要成分有Pt和
(4)“沉银”过程中肼(N2H4)的作用是
(5)经上述工艺得到的粗银还需进行电解精炼:纯银作阴极,电解液为硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是
(6)某研究性学习小组为探究Ag与Fe3+的反应,按图装置进行实验(盐桥中的物质不参与反应)。

①K闭合时,电流表指针偏转,石墨作
②当指针归零后,向U形管左侧滴加几滴Fe(NO3)2浓溶液,发现指针向反方向偏转,写出此时银电极的反应式:
③结合上述实验分析,写出Fe3+和Ag反应的离子方程式:
您最近一年使用:0次
名校
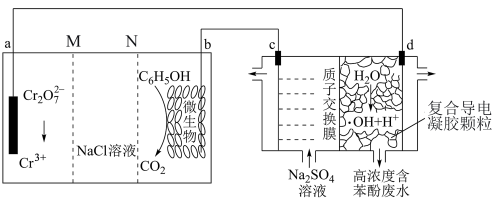
2 . 我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池组合装置,实现了发电、环保两位一体(如图所示)。已知羟基自由基(
的原电池—电解池组合装置,实现了发电、环保两位一体(如图所示)。已知羟基自由基( )具有强氧化性,能氧化苯酚。左侧装置为原电池。下列说法错误的是
)具有强氧化性,能氧化苯酚。左侧装置为原电池。下列说法错误的是
 和
和 的原电池—电解池组合装置,实现了发电、环保两位一体(如图所示)。已知羟基自由基(
的原电池—电解池组合装置,实现了发电、环保两位一体(如图所示)。已知羟基自由基( )具有强氧化性,能氧化苯酚。左侧装置为原电池。下列说法错误的是
)具有强氧化性,能氧化苯酚。左侧装置为原电池。下列说法错误的是
| A.电池工作时,b极附近pH增大 |
| B.电极电势的高低:a>b |
C.d极区苯酚被氧化的化学方程式为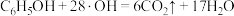 |
| D.右侧装置中,c、d两极产生气体的体积比(相同条件下)为7∶3 |
您最近一年使用:0次
名校
解题方法
3 . 某实验小组对 分别与
分别与 、
、 的反应进行探究。
的反应进行探究。
【甲同学的实验】
(1)甲同学探究实验Ⅰ的电极产物。
①取少量 溶液电极附近的混合液,加入
溶液电极附近的混合液,加入___________ ,产生白色沉淀,证明产生了 。
。
②该同学又设计实验探究另一电极的产物,所需检验试剂及现象分别是___________ 、___________ 。
(2)实验Ⅰ中负极的电极反应式为___________ 。
【乙同学的实验】
乙同学进一步探究 溶液与
溶液与 溶液能否发生反应,设计、完成实验并记录如下:
溶液能否发生反应,设计、完成实验并记录如下:
(3)查阅资料:溶液中 、
、 、
、 三种微粒会形成红色配合物并存在如下转化:
三种微粒会形成红色配合物并存在如下转化:

从反应速率和化学平衡两个角度解释1~30min的实验现象:___________ 。
(4)解释30min后上层溶液又变为浅红色的可能原因:___________ 。
【实验反思】
(5)分别对比Ⅰ和Ⅱ、Ⅱ和Ⅲ, 能否与
能否与 或
或 发生氧化还原反应和
发生氧化还原反应和___________ 有关(写出两条)。
 分别与
分别与 、
、 的反应进行探究。
的反应进行探究。【甲同学的实验】
| 装置 | 编号 | 试剂X | 实验现象 |
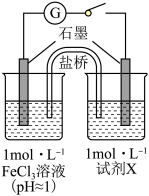 | Ⅰ |  溶液( 溶液(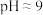 ) ) | 闭合开关后灵敏电流计指针发生偏转 |
| Ⅱ |  溶液( 溶液( ) ) | 闭合开关后灵敏电流计指针未发生偏转 |
①取少量
 溶液电极附近的混合液,加入
溶液电极附近的混合液,加入 。
。②该同学又设计实验探究另一电极的产物,所需检验试剂及现象分别是
(2)实验Ⅰ中负极的电极反应式为
【乙同学的实验】
乙同学进一步探究
 溶液与
溶液与 溶液能否发生反应,设计、完成实验并记录如下:
溶液能否发生反应,设计、完成实验并记录如下:| 装置 | 编号 | 反应时间 | 实验现象 |
 | Ⅲ | 0~1min | 产生红色沉淀,有刺激性气味气体逸出 |
| 1~30min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 | ||
| 30min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
 、
、 、
、 三种微粒会形成红色配合物并存在如下转化:
三种微粒会形成红色配合物并存在如下转化:
从反应速率和化学平衡两个角度解释1~30min的实验现象:
(4)解释30min后上层溶液又变为浅红色的可能原因:
【实验反思】
(5)分别对比Ⅰ和Ⅱ、Ⅱ和Ⅲ,
 能否与
能否与 或
或 发生氧化还原反应和
发生氧化还原反应和
您最近一年使用:0次
名校
解题方法
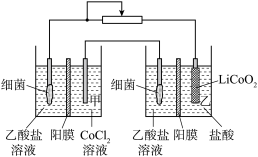
4 . 设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料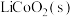 转化为
转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法
,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法不正确 的是
 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料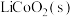 转化为
转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法
,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法
| A.装置工作时,甲室溶液pH最终升高 |
| B.装置工作一段时间后,乙室应补充盐酸 |
C.乙室电极反应式为 |
D.若甲室 减少 减少 ,乙室 ,乙室 增加 增加 ,则此时已进行过溶液转移 ,则此时已进行过溶液转移 |
您最近一年使用:0次
5 . 全钒液流储能电池是一种新型的绿色环保储能系统(工作原理如下图,电解液含硫酸)。
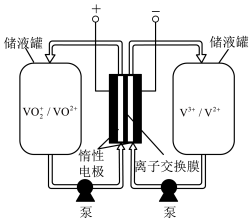
下列说法不正确 的是
| 离子种类 |  |  |  |  |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |

下列说法
A.该电池总反应的离子方程式是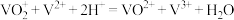 |
| B.当完成储能时,正极溶液的颜色是黄色 |
C.电池工作时, 透过离子交换膜向负极区移动 透过离子交换膜向负极区移动 |
| D.该电池能提供稳定的输出功率,原因是电解液循环,保持各离子浓度稳定 |
您最近一年使用:0次
6 . 电化学在化工、冶金、机械、电子、航空、航天、轻工、仪表、医学、材料、能源、金属腐蚀与防护、环境科学等科技领域获得了广泛的应用。
Ⅰ.电解精炼镓的装置如图所示,粗镓含 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为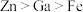 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
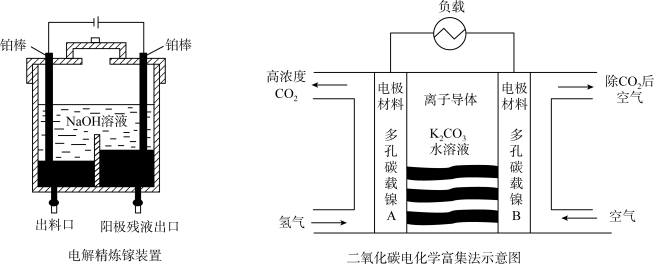
(1)电解后,电解槽底部阳极泥中所含的金属有_____ 。
(2)电解过程中阴极的电极反应式是_____ 。
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中, 向多孔碳载镍
向多孔碳载镍_____ (填“A”或“B”)电极移动。
(4)负极的电极反应式是_____ 。
(5)在多孔碳载镍A电极上消耗1
 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是_____ L。
Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。
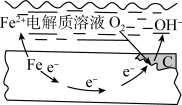
(6)钢铁吸氧腐蚀的正极反应式是_____ 。
(7)下列关于金属腐蚀的防护说法正确的是_____ 。
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
Ⅰ.电解精炼镓的装置如图所示,粗镓含
 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为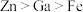 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
(1)电解后,电解槽底部阳极泥中所含的金属有
(2)电解过程中阴极的电极反应式是
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中,
 向多孔碳载镍
向多孔碳载镍(4)负极的电极反应式是
(5)在多孔碳载镍A电极上消耗1

 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。

(6)钢铁吸氧腐蚀的正极反应式是
(7)下列关于金属腐蚀的防护说法正确的是
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
您最近一年使用:0次
名校
解题方法
7 . 电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
(1)某空间站局部能量转化系统如图所示,其中氢氧燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为___________ 。
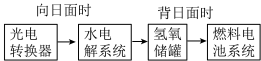
(2)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为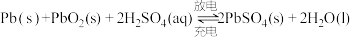 。
。
①放电时,正极的电极反应式:___________ ,
当外电路通过0.5 mole-时,理论上负极板的质量增加___________ g。
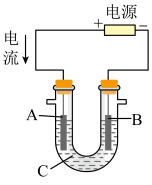
②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如下图所示,电解液c选用___________ 溶液,A电极的材料是___________ ,B电极反应式是___________ 。
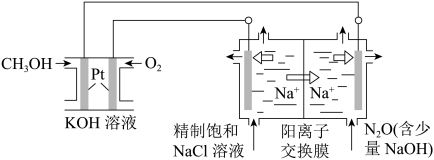
(3)以CH3OH燃料电池为电源电解法制取ClO2,二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①CH3OH燃料电池放电过程中,负极反应式为___________ 。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为___________ 。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多3.36 L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为___________ mol(精确到小数点后两位)。
(1)某空间站局部能量转化系统如图所示,其中氢氧燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为

(2)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
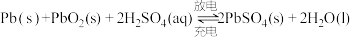 。
。①放电时,正极的电极反应式:
当外电路通过0.5 mole-时,理论上负极板的质量增加
②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如下图所示,电解液c选用

(3)以CH3OH燃料电池为电源电解法制取ClO2,二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。

①CH3OH燃料电池放电过程中,负极反应式为
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多3.36 L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
您最近一年使用:0次
名校
解题方法
8 . 下列装置可分离废水中的Co2+和Ni2+。已知Ni2+和Co2+性质相似,Co2+和乙酰丙酮不反应。下列说法正确的是

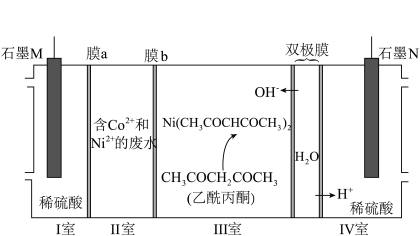


| A.M电极接太阳能电池的P电极 |
| B.通电一段时间后,I、IV室内溶液pH均减小 |
| C.膜a、膜b分别为阳离子交换膜和阴离子交换膜 |
D.每生成1molSO ,理论上双极膜至少解离7molH2O ,理论上双极膜至少解离7molH2O |
您最近一年使用:0次
2023-03-03更新
|
1387次组卷
|
3卷引用:山东省淄博市2022-2023学年高三第一次模拟考试化学试题
名校
解题方法
9 . 水系钠离子电池有望代替锂离子电池和铅酸电池,工作原理如图所示,以 光电极作辅助电极,充电时
光电极作辅助电极,充电时 光电极受光激发产生电子和空穴,空穴作用下NaI转化为
光电极受光激发产生电子和空穴,空穴作用下NaI转化为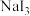 。下列说法错误的是
。下列说法错误的是
 光电极作辅助电极,充电时
光电极作辅助电极,充电时 光电极受光激发产生电子和空穴,空穴作用下NaI转化为
光电极受光激发产生电子和空穴,空穴作用下NaI转化为 。下列说法错误的是
。下列说法错误的是
| A.放电时,电极N为正极,发生还原反应 |
B.充电时,电极M的电极反应式为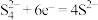 |
C.放电时, 电极产生的电子转移给 电极产生的电子转移给 |
D.充电时,每生成 ,有 ,有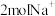 通过交换膜进入M电极室 通过交换膜进入M电极室 |
您最近一年使用:0次
2023-02-12更新
|
438次组卷
|
2卷引用:山东省德州市2022-2023学年高二上学期期末考试化学试题
10 . 科学家近日发明了一种无污染、无需净化高效产氢的可充电电池,电池示意图如下。电极为金属锌和选择性催化材料,实现了阴极析氢和 氧化两个独立的反应,可稳定循环600次。下列说法错误的是
氧化两个独立的反应,可稳定循环600次。下列说法错误的是
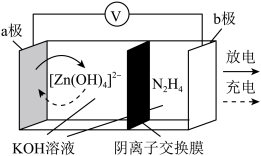
 氧化两个独立的反应,可稳定循环600次。下列说法错误的是
氧化两个独立的反应,可稳定循环600次。下列说法错误的是
A.充电时,阴极区溶液 减小 减小 |
B.放电时, 由b极区向a极区迁移 由b极区向a极区迁移 |
| C.充电时,b极反应式为N2H4-4e-+4OH-=N2+4H2O |
D.产生 ,a极质量增大 ,a极质量增大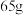 |
您最近一年使用:0次



