名校
1 . 分别利用如图装置(夹持装置略)进行相应实验,不能达到实验目的的是


| A.用甲装置制备并收集NH3 | B.用乙装置制备溴苯并验证有HBr产生 |
| C.用丙装置制备无水FeCl3 | D.用丁装置制备Fe(OH)2并能较长时间观察其颜色 |
您最近一年使用:0次
2020-11-10更新
|
240次组卷
|
5卷引用:黑龙江省大庆铁人中学2022届高三上学期开学考试化学试题
名校
解题方法
2 . 苯胺(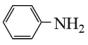 )是重要的化工原料,其制备原理为:
)是重要的化工原料,其制备原理为:
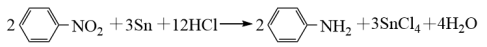
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐 。
。
乙醚为极易挥发的液体,是用途广泛的有机溶剂,与空气接触会形成易爆混合物。部分物质物理性质见表:
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为_______ 。
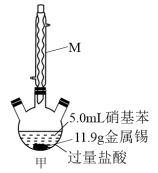
(2)图甲中 装置的名称为
装置的名称为_______ ,往硝基苯中加入 和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量
和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量 溶液得碱化液。加
溶液得碱化液。加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为_______ 。
(3)分离提纯:
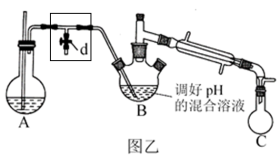
步骤i.如图乙,加热装置 产生水蒸气,采用水蒸气蒸馏的方法,用
产生水蒸气,采用水蒸气蒸馏的方法,用热的水蒸气 将 中的苯胺逐渐吹出至
中的苯胺逐渐吹出至 中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
步骤ⅱ.步骤i所得水溶液中加 至饱和,用乙醚萃取得萃取液与粗苯胺合并。
至饱和,用乙醚萃取得萃取液与粗苯胺合并。
步骤ⅲ.合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度T时的馏分得到苯胺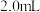 。
。
①图乙中T型管 处方框区域玻璃导管不宜过长,原因是
处方框区域玻璃导管不宜过长,原因是_______ 。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是_______ 。步骤ⅲ中干燥剂可以选用_______ (填序号)
a.浓硫酸 b.五氧化二磷 c.碱石灰
③步骤ⅲ中蒸馏获得苯胺需控制温度为_______ 左右。
④该实验中所得苯胺的产率为_______ (保留三位有效数字)。
 )是重要的化工原料,其制备原理为:
)是重要的化工原料,其制备原理为: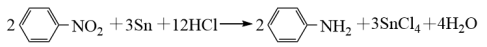
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐
 。
。乙醚为极易挥发的液体,是用途广泛的有机溶剂,与空气接触会形成易爆混合物。部分物质物理性质见表:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 溶解性 | 密度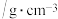 |
| 苯胺 | 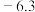 | 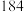 |  | 微溶于水,易溶于乙醚 |  |
| 硝基苯 | 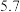 | 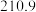 | 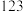 | 难溶于水,易溶于乙醚 | 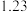 |
| 乙醚 | 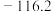 | 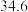 |  | 微溶于水 | 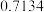 |
(1)实验室用苯制取硝基苯的化学方程式为
(2)图甲中
 装置的名称为
装置的名称为 和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量
和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量 溶液得碱化液。加
溶液得碱化液。加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为
(3)分离提纯:

步骤i.如图乙,加热装置
 产生水蒸气,采用水蒸气蒸馏的方法,用
产生水蒸气,采用水蒸气蒸馏的方法,用 中的苯胺逐渐吹出至
中的苯胺逐渐吹出至 中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。步骤ⅱ.步骤i所得水溶液中加
 至饱和,用乙醚萃取得萃取液与粗苯胺合并。
至饱和,用乙醚萃取得萃取液与粗苯胺合并。步骤ⅲ.合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度T时的馏分得到苯胺
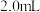 。
。①图乙中T型管
 处方框区域玻璃导管不宜过长,原因是
处方框区域玻璃导管不宜过长,原因是②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是
a.浓硫酸 b.五氧化二磷 c.碱石灰
③步骤ⅲ中蒸馏获得苯胺需控制温度为
④该实验中所得苯胺的产率为
您最近一年使用:0次
3 . 实验室制备硝基苯的实验装置如图所示(夹持装置已略去)。下列说法不正确的是


| A.水浴加热的优点为使反应物受热均匀、容易控制温度 |
| B.浓硫酸、浓硝酸和苯混合时,应先向浓硝酸中缓缓加入浓硫酸,待冷却至室温后,再将苯逐滴滴入 |
| C.仪器a的作用是冷凝回流,提高原料的利用率 |
| D.反应完全后,可用仪器a、b蒸馏得到产品 |
您最近一年使用:0次
2021-12-15更新
|
259次组卷
|
2卷引用:黑龙江省实验中学2021-2022学年高三上学期第五次月考化学试题
名校
解题方法
4 . 某科学小组制备硝基苯的实验装置如下,有关数据列如下表:
实验步骤如下:
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混和酸,将混合酸小心地加入B中。把18mol(15.6g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混和均匀。在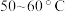 下发生反应,直至反应结束。
下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、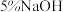 溶液和水洗涤。分出的产物加入无水
溶液和水洗涤。分出的产物加入无水 颗粒,静置片刻,弃去
颗粒,静置片刻,弃去 ,进行蒸馏纯化,收集
,进行蒸馏纯化,收集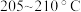 馏分,得到纯硝基苯18g。
馏分,得到纯硝基苯18g。
回答下列问题:

(1)图中B仪器的名称___ ,图中装置C的作用是____ 。
(2)制备硝基苯的化学方程式____ 。
(3)为了使反应在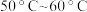 下进行,常用的加热方式是
下进行,常用的加热方式是____ 。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是___ (用化学方程式说明),实验室常用氢氧化钠溶液除去该有色物质,涉及的离子方程式为___ 。
(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在___ (填“上”或“下”)层,步骤中加入的无水 的作用是除去硝基苯中的水分,若实验过程中省略该步操作,实验的产率
的作用是除去硝基苯中的水分,若实验过程中省略该步操作,实验的产率___ (填“偏高”“偏低”或“不变”)。
(5)本实验所得到的硝基苯产率是__ 。(结果保留3位有效数字)
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g∙cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 不溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混和酸,将混合酸小心地加入B中。把18mol(15.6g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混和均匀。在
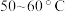 下发生反应,直至反应结束。
下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、
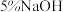 溶液和水洗涤。分出的产物加入无水
溶液和水洗涤。分出的产物加入无水 颗粒,静置片刻,弃去
颗粒,静置片刻,弃去 ,进行蒸馏纯化,收集
,进行蒸馏纯化,收集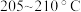 馏分,得到纯硝基苯18g。
馏分,得到纯硝基苯18g。回答下列问题:

(1)图中B仪器的名称
(2)制备硝基苯的化学方程式
(3)为了使反应在
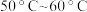 下进行,常用的加热方式是
下进行,常用的加热方式是(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在
 的作用是除去硝基苯中的水分,若实验过程中省略该步操作,实验的产率
的作用是除去硝基苯中的水分,若实验过程中省略该步操作,实验的产率(5)本实验所得到的硝基苯产率是
您最近一年使用:0次
2021-04-13更新
|
312次组卷
|
2卷引用:黑龙江省大庆实验中学2020-2021学年高二下学期4月月考化学试题



