1 . 硝基苯是重要的化工原料,用途广泛。
I.制备硝基苯的化学反应方程式如下:
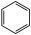 +HO-NO2
+HO-NO2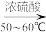
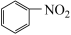 +H2O
+H2O
II.可能用到的有关数据列表如下:
III.制备硝基苯的反应装置图如下:
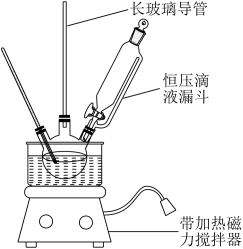
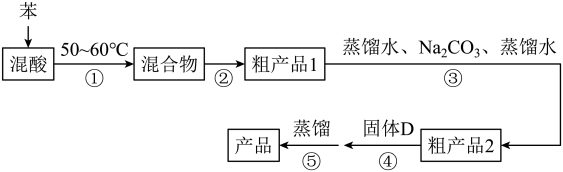
IV .制备、提纯硝基苯的流程如下:
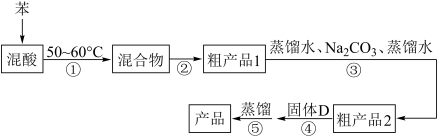
请回答下列问题:
(1)配制混酸时,应在烧杯中先加入___________ ;反应装置中的长玻璃导管最好用___________ 代替(填仪器名称);恒压滴液漏斗的优点是___________ 。
(2)步骤①反应温度控制在50~60°C的主要原因是___________ ;步骤②中分离混合物获得粗产品1的实验操作名称是___________ 。
(3)最后一次水洗后分液得到粗产品2时,粗产品2应___________ (填“a” 或“b”)。
a.从分液漏斗上口倒出 b.从分液漏斗下口放出
b.从分液漏斗下口放出
(4)粗产品1呈浅黄色,粗产品2为无色。粗产品1呈浅黄色的原因是___________ 。
(5)步骤④用到的固体D的名称为___________ 。
(6)步骤⑤蒸馏操作中,锥形瓶中收集到的物质为___________ 。
I.制备硝基苯的化学反应方程式如下:
 +HO-NO2
+HO-NO2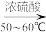
 +H2O
+H2OII.可能用到的有关数据列表如下:
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | ___ | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | ___ | 338 | 1.84 | 易溶于水 |

IV .制备、提纯硝基苯的流程如下:

请回答下列问题:
(1)配制混酸时,应在烧杯中先加入
(2)步骤①反应温度控制在50~60°C的主要原因是
(3)最后一次水洗后分液得到粗产品2时,粗产品2应
a.从分液漏斗上口倒出
 b.从分液漏斗下口放出
b.从分液漏斗下口放出(4)粗产品1呈浅黄色,粗产品2为无色。粗产品1呈浅黄色的原因是
(5)步骤④用到的固体D的名称为
(6)步骤⑤蒸馏操作中,锥形瓶中收集到的物质为
您最近一年使用:0次
2021-03-14更新
|
2135次组卷
|
5卷引用:吉林省长春市普通高中2021届高三质量监测(二)(二模)理综化学试题
吉林省长春市普通高中2021届高三质量监测(二)(二模)理综化学试题宁夏石嘴山市2021届高三下学期3月高考质量监测(一模) 化学试题(已下线)第30讲 常见的烃——甲烷、乙烯、苯(精练)-2022年高考化学一轮复习讲练测(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)第二节 研究有机化合物的一般方法 第1课时 有机化合物的分类、提纯
名校
解题方法
2 . 在各类化学实验中常常用到导管,如实验室制备硝基苯,装置如图。下列关于长导管的用途的叙述中错误的是
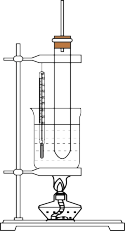

| A.实验室制备硝基苯,长导管的主要作用是:冷凝和回流 |
| B.加热密闭装置,防止容器内压力过高,可用导管进行导气减压 |
| C.长导管冷凝时,冷却剂是空气 |
| D.长导管可以代替玻璃棒进行使用 |
您最近一年使用:0次
2012·上海奉贤·二模
3 . 在各类化学实验中常常用到导管,如实验室制备硝基苯,装置如图。下列关于长导管的用途的叙述中错误的是
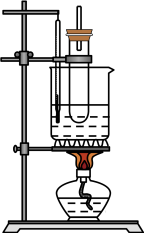

| A.实验室制备硝基苯,长导管的主要作用是:冷凝和回流 |
| B.加热密闭装置,防止容器内压力过高,可用导管进行导气减压 |
| C.长导管也可以用来对热气体进行冷凝,冷却剂可以是空气 |
| D.长导管可以代替玻璃棒进行使用 |
您最近一年使用:0次
名校
4 . 如图为实验室制溴苯的装置图。完成下列填空:

(1)该反应的化学方程式:___ 。
(2)双球U形管中盛放CCl4的用途:___ 。
(3)A中铁丝的作用:___ 。
(4)分液漏斗中液体滴入A中的实验现象___ 。
(5)若A中混合液倒入冷水,则有黄色液体产生,原因是溴苯中混有___ (填化学式),如何除去该杂质需加入的试剂是___ ,相应操作为___ 。
(6)B试管中若加入硝酸银溶液,则实验现象是:___ 。加入硝酸银溶液的目的是为了检验___ (填化学式)的生成,从而证明该反应为___ (填反应类型)。

(1)该反应的化学方程式:
(2)双球U形管中盛放CCl4的用途:
(3)A中铁丝的作用:
(4)分液漏斗中液体滴入A中的实验现象
(5)若A中混合液倒入冷水,则有黄色液体产生,原因是溴苯中混有
(6)B试管中若加入硝酸银溶液,则实验现象是:
您最近一年使用:0次
5 . 硝基苯是重要的化工原料,用途广泛。制备反应如下:
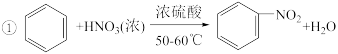
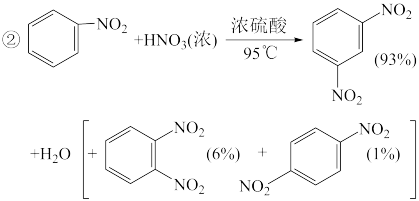
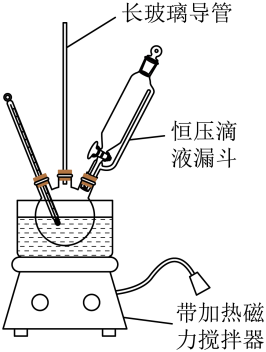
组装如右上图反应装置。 制备、提纯硝基苯流程如下:
可能用到的有关数据列表如下:
请回答下列问题:
(1)配制混酸应在烧杯中先加入__ ;实验装置中长玻璃管最好用________ 代替(填仪器名称);恒压滴液漏斗的优点是__________________ 。
(2)反应温度控制在50~60 ℃的原因是______________ ;反应结束后产物在___ 层(填“上”或者“下”),步骤②分离混酸和产品的操作名称是_____ 。
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?_____________ 。
(4)固体D的名称为_____ 。
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为______________________________________ 。
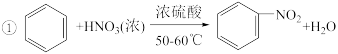


组装如右上图反应装置。 制备、提纯硝基苯流程如下:

可能用到的有关数据列表如下:
| 物 质 | 熔点/℃ | 沸点/℃ | 密度(20 ℃)/g · cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | — | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | — | 338 | 1.84 | 易溶于水 |
(1)配制混酸应在烧杯中先加入
(2)反应温度控制在50~60 ℃的原因是
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?
(4)固体D的名称为
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为
您最近一年使用:0次



