1 . 几种短周期元素的原子半径及主要化合价如图所示,下列叙述正确的是
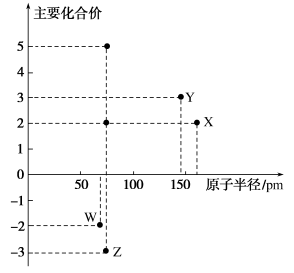

| A.X、Y的最高价氧化物都是两性氧化物 |
B.Y的最高价氧化物对应的水化物能溶于 溶液 溶液 |
| C.Z的非金属性强于W |
| D.X的单质在第三周期中还原性最强 |
您最近一年使用:0次
2 . 下列关于元素周期表的叙述正确的是
| A.原子的最外层电子数都等于该元素所在的族序数 |
| B.目前使用的元素周期表中,最长的周期含有32种元素 |
| C.短周期元素是指1~20号元素 |
| D.现行元素周期表是按照相对原子质量的大小顺序对元素进行排列的 |
您最近一年使用:0次
解题方法
3 . 元素周期律
(1)元素周期律的内容:随着元素核电荷数的递增,元素的______ (除稀有气体元素外)、元素的________ 、元素的________ 和________ 都呈现周期性变化。元素周期律是指元素的性质随着核电荷数的递增_______ 的规律。
(2)元素周期律的实质:元素周期律是_______ 的必然结果。
(1)元素周期律的内容:随着元素核电荷数的递增,元素的
(2)元素周期律的实质:元素周期律是
您最近一年使用:0次
4 . 元素化合价的变化规律
(1)1~18号元素的最高正化合价的变化规律是______ ,其中_______ 元素没有最高正化合价,最低负化合价的变化规律是_______ 。
(2)元素的最高化合价与最低负化合价的数值与原子最外层电子数的关系是:最高正化合价=_______ (_______ 除外)、最低负化合价=________ 、最高正化合价+|最低负化合价|=________ 。
(3)元素主要化合价呈现周期性变化的根本原因是:随着核电荷数的递增,原子的______ 呈周期性变化。
(1)1~18号元素的最高正化合价的变化规律是
(2)元素的最高化合价与最低负化合价的数值与原子最外层电子数的关系是:最高正化合价=
(3)元素主要化合价呈现周期性变化的根本原因是:随着核电荷数的递增,原子的
您最近一年使用:0次
5 . 原子结构的变化规律
(1)原子最外层电子排布的规律性变化
除H、He外,元素随着原子序数的递增,原子最外电子层数重复出现从_______ 递增到_______ 的变化,说明元素原子的最外层电子数出现_______ 变化。
(2)元素原子半径的变化规律
随着核电荷数的递增,元素的原子半径呈现_______ 变化,原子序数为3~9号及11~17号的元素的原子半径依次________ 。
(1)原子最外层电子排布的规律性变化
除H、He外,元素随着原子序数的递增,原子最外电子层数重复出现从
(2)元素原子半径的变化规律
随着核电荷数的递增,元素的原子半径呈现
您最近一年使用:0次
2022-08-17更新
|
43次组卷
|
2卷引用:课前-5.1.1 元素周期律-苏教版2020必修第一册
6 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用相应的化学用语回答下列问题:
(1)③的单质的电子式为_______ ,结构式为_______ 。
(2)④、⑥、⑧的原子半径由小到大的顺序为_______ (用元素符号作答)。
(3)金属性最强的是_______ ,非金属性最强的是_______ ,(用元素符号答)②、③、⑨的最高价氧化物的水化物的酸性由弱到强的顺序是_______ (用化学式答)。
(4)写出⑦元素的最高价氧化物对应水化物分别与元素⑥的最高价氧化物对应水化物的水溶液反应的离子方程式_______ 。
(5)①和④形成的气态氢化物与①和⑧形成的气态氢化物相比较,_______ 的稳定性强;_______ 的沸点高(填化学式),理由是_______ 。
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)④、⑥、⑧的原子半径由小到大的顺序为
(3)金属性最强的是
(4)写出⑦元素的最高价氧化物对应水化物分别与元素⑥的最高价氧化物对应水化物的水溶液反应的离子方程式
(5)①和④形成的气态氢化物与①和⑧形成的气态氢化物相比较,
您最近一年使用:0次
7 . 如下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
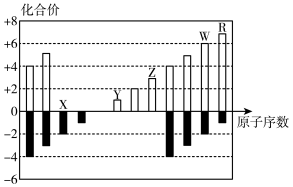

| A.气态氢化物的稳定性:X<W |
| B.X与Y可以形成阴阳离子个数比为1:1和1:2的两种离子化合物 |
| C.由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2- |
| D.Y和W可以形成离子化合物 |
您最近一年使用:0次
8 . 随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)z在元素周期表中的位置是_______ 。
(2)写出化合物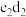 的电子式:
的电子式:_______ ,将少量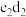 投入水中,剧烈反应,写出反应的化学方程式:
投入水中,剧烈反应,写出反应的化学方程式:_______ 。
(3)g与h的简单氢化物的稳定性由强到弱的顺序为_______ (用化学式表示)。
(4)d、e、f、g这四种元素分别形成的简单离子,离子半径由小到大的顺序是_______ (用离子符号表示)。
(5)e和f两元素相比较,金属性较强的是_______ (填元素符号),请设计一个实验验证该结论(简要描述实验步骤和现象):_______ 。

(1)z在元素周期表中的位置是
(2)写出化合物
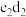 的电子式:
的电子式: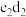 投入水中,剧烈反应,写出反应的化学方程式:
投入水中,剧烈反应,写出反应的化学方程式:(3)g与h的简单氢化物的稳定性由强到弱的顺序为
(4)d、e、f、g这四种元素分别形成的简单离子,离子半径由小到大的顺序是
(5)e和f两元素相比较,金属性较强的是
您最近一年使用:0次
9 . 下图是部分短周期元素的常见化合价与原子序数的关系图,下列说法正确的是

①元素C与G对应单质的氧化性:G>C
②简单离子半径大小:
③最高价氧化物对应水化物酸性:
④简单氢化物沸点:
⑤单质与氢气化合的剧烈程度:C>G

①元素C与G对应单质的氧化性:G>C
②简单离子半径大小:

③最高价氧化物对应水化物酸性:

④简单氢化物沸点:

⑤单质与氢气化合的剧烈程度:C>G
| A.②④ | B.②⑤ | C.①③ | D.③⑤ |
您最近一年使用:0次
10 . 元素性质周期性变化的根本原因是
| A.原子半径 | B.化合价 | C.金属性和非金属性 | D.原子核外电子排布 |
您最近一年使用:0次



