名校
解题方法
1 . M、W、X、Y、Z是同周期主族元素,X原子的最外层电子数是W原子次外层电子数的3倍,R元素是无机非金属材料的主角。M、W、X、Y、Z形成的化合物的结构如图所示。下列说法正确的是
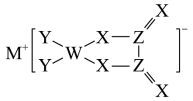
| A.M的单质通常保存在煤油中 | B.R的氧化物能溶于Y的氢化物的水溶液 |
| C.图中W原子不满足8电子稳定结构 | D.X、Y、Z的最简单氢化物的沸点:Y>X>Z |
您最近半年使用:0次
名校
2 . 一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大,且总和为24,下列有关叙述正确的是


| A.该化合物中,W、X、Y之间存在离子键 | B.Y的氧化物的水化物不一定为强酸 |
| C.原子半径:Y>X | D.Z的单质只能与水反应,不与乙醇反应 |
您最近半年使用:0次
解题方法
3 . X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,X+是一个裸露的质子,X和Z处于同一主族,Y、Z的最外层电子数之和与Q的最外层电子数相等,W的最内层电子数和最外层电子数之和等于次外层电子数。下列说法正确的是
| A.Q的单质与水反应可生成两种酸 |
| B.原子半径:r(Q)>r(W)>r(Z)>r(Y)>r(X) |
| C.化合物XQ和ZQ中化学键的类型相同 |
| D.Y分别与X、Z以及W形成的化合物都只有一种 |
您最近半年使用:0次
2021-08-21更新
|
185次组卷
|
2卷引用:2013全国高中化学素质和实验能力竞赛(河南赛区)试题
解题方法
4 . a在常温下为离子晶体,由X、Y两元素构成,a中的Xm+和Yn-的电子层结构相同。已知下列反应:
(1)a+H2O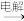 H2+b+c
H2+b+c
(2)H2+c→d(气)
(3)b+c→a+e+H2O
(4)e+d→a+f
则a、e、f依次是
(1)a+H2O
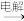 H2+b+c
H2+b+c(2)H2+c→d(气)
(3)b+c→a+e+H2O
(4)e+d→a+f
则a、e、f依次是
| A.NaCl NaClO HCl | B.CaCl2 Ca(ClO)2 HClO |
| C.Na2S Na2SO3 H2SO3 | D.K2S K2SO3 H2SO4 |
您最近半年使用:0次
5 . 短周期元素A、B、C、D、E的原子序数依次增大,它们的原子最外层电子数之和为17.A、C同主族,A、C的单质在常温下的状态不同,D原子最外层电子数与电子层数相等,E的原子半径在同周期元素中最小,则下列说法不正确的是
| A.A、B两种元素可组成化学式为B2A4的化合物 |
| B.A或C与氧元素形成的化合物均可能含有非极性键 |
| C.C、D、E的最高价氧化物对应的水化物能两两反应 |
| D.工业中常用电解熔融DE3制备单质D |
您最近半年使用:0次
6 . 元素A、B、C、D、E的原子序数逐渐增大。A原子核外电子只有一种运动状态;B原子第二能层电子数等于该能层轨道数,B、C、D核电荷数依次增加1;E基态原子核外第四能级组有11个电子分布于两个能级轨道之中,其中一个能级全充满,一个半充满。
(1)A、B、C、D原子半径由小到大的顺序为(写元素符号)_______ 与E同副族的第六周元素符号是_______ ,其基态原子的电子排布式:_______ 。
(2)由元素A、B、C、D构成微粒结构简式如下,请分别画出它们的Lewis结构式并命名。(要求:画出所有未共享电子对)。
①ADBC:_______
②ABCD:_______
③ADCB:_______
④CD :
:_______
(3)指出下列配合物(或配离子)中心体的配位数和价态:
①[PtCl3(C2H4)]-:_______
②trans-[Co(en)2C12]+:_______ [en:H2NCH2CH2NH2]。
(4)回答下列问题:
①在通常状况下,He、Ne、Ar、Kr、Xe在水中溶解度[mol/1kgH2O]递增,其原因是_______ 。
②在水溶液中,邻-羟基苯甲酸的酸性(Ka1=105×10-5)大于间-羟基苯甲酸的酸性(Ka1=8.3×10-5),其原因是_______ 。
③在一定条件下,强路易斯酸AsF5能诱导溴元素发生归中反应:4Br2+BrF3+3AsF5=3Br AsFf
AsFf ,产物阳离子空间构型为
,产物阳离子空间构型为_______ ,产物阴离子中心原子的轨道采用_______ 杂化。
(5)B的常见单质的两种结构如下图所示,左、右分别为立方和六方的骨架结构。
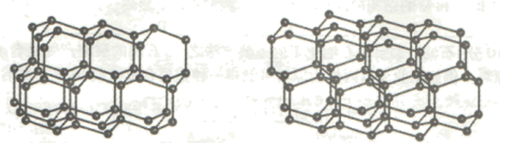
该单质的名称为_______ ;两种骨架结构中每个B原子都以“B-B”键与另外四个B原子相连,每个B原子参与形成_______ 个六元环;两种骨架结构不相同之处是六元环的构型,请说明有何不同:_______ 。
(1)A、B、C、D原子半径由小到大的顺序为(写元素符号)
(2)由元素A、B、C、D构成微粒结构简式如下,请分别画出它们的Lewis结构式并命名。(要求:画出所有未共享电子对)。
①ADBC:
②ABCD:
③ADCB:
④CD
 :
:(3)指出下列配合物(或配离子)中心体的配位数和价态:
①[PtCl3(C2H4)]-:
②trans-[Co(en)2C12]+:
(4)回答下列问题:
①在通常状况下,He、Ne、Ar、Kr、Xe在水中溶解度[mol/1kgH2O]递增,其原因是
②在水溶液中,邻-羟基苯甲酸的酸性(Ka1=105×10-5)大于间-羟基苯甲酸的酸性(Ka1=8.3×10-5),其原因是
③在一定条件下,强路易斯酸AsF5能诱导溴元素发生归中反应:4Br2+BrF3+3AsF5=3Br
 AsFf
AsFf ,产物阳离子空间构型为
,产物阳离子空间构型为(5)B的常见单质的两种结构如下图所示,左、右分别为立方和六方的骨架结构。

该单质的名称为
您最近半年使用:0次
解题方法
7 . 短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10。A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数。则下列叙述正确的是
| A.D元素处于元素周期表中第3周期第IV族 |
| B.四种元素的原子半径:A<B<D<C |
| C.B、D的最高价氧化物中,B、D与氧原子之间均为双键 |
| D.一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
您最近半年使用:0次
8 . 短周期元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,且原子最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素。下列叙述正确的是
| A.在地壳中,C元素的含量位于第一位 |
| B.C元素位于元素周期表中的第3周期第ⅠA族 |
| C.A、B、D三种元素形成的化合物一定是强酸 |
| D.B元素与氢元素形成化合物的化学式一定为H2B |
您最近半年使用:0次
2016-12-09更新
|
604次组卷
|
2卷引用:2013全国高中化学素质和实验能力竞赛(河南赛区)试题
9-10高一下·福建厦门·期末
解题方法
9 . A、B、C、D、E是除稀有气体以外的的5种短周期元素,原子序数依次增大并分占三个周期。B、C、D为同一周期依次相邻的3种元素,B和D的原子序数之比为3 :4,E原子的电子层数等于最外层电子数。请回答相关问题:
(1)B元素在周期表中的位置_________ ,C元素是_________ (填元素符号);
(2)比较D和E简单离子半径的大小(用离子符号表示):____________ ;
(3)A和D形成的含18电子化合物的化学式为____________ ;
(4)元素E形成的简单离子的水溶液与C的氢化物的水溶液反应的离子方程式为:_______________ ;
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2A6化合物,该物质在D2中能燃烧,写出它在D2中完全燃烧的化学方程式:____________ 。
(1)B元素在周期表中的位置
(2)比较D和E简单离子半径的大小(用离子符号表示):
(3)A和D形成的含18电子化合物的化学式为
(4)元素E形成的简单离子的水溶液与C的氢化物的水溶液反应的离子方程式为:
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2A6化合物,该物质在D2中能燃烧,写出它在D2中完全燃烧的化学方程式:
您最近半年使用:0次



