名校
解题方法
1 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
回答下列问题:
(1)W在元素周期表中的位置为_______ ,X的最高价氧化物对应水化物的化学式为_______ 。
(2)用电子式表示X2Q的形成过程:_______ 。
(3)金属性Y_______ (填“>”或“<”)X,从原子结构角度解释原因_______ 。
(4)下列对于Z及其化合物的推断中正确的是_______(填标号)。
(5)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是_______ 。
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7价 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰为紫色 |
| Z | 原子结构示意图为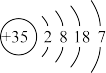 |
(1)W在元素周期表中的位置为
(2)用电子式表示X2Q的形成过程:
(3)金属性Y
(4)下列对于Z及其化合物的推断中正确的是_______(填标号)。
| A.Z的化合价中只有+7价 |
| B.Z的最高价氧化物对应水化物的酸性弱于w的最高价氧化物对应水化物的酸性 |
| C.Z元素单质的氧化性强于W元素单质的氧化性 |
| D.Z与X形成的化合物中只存在离子键 |
您最近一年使用:0次
名校
解题方法
2 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是
| A.X的简单氢化物的热稳定性比W的强 |
| B.Y的简单离子与X的具有相同的电子层结构 |
| C.Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红 |
| D.Z与X属于同一主族,与Y属于同一周期 |
您最近一年使用:0次
名校
3 . 短周期元素W、X、Y、Z的原子序数依次递增,a、 b、c、d、 e、f是由这些元素组成的化合物,d为淡黄色的离子化合物,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是
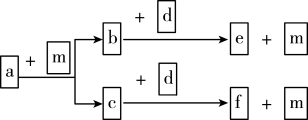

| A.原子半径: W<X<Y<Z |
| B.简单气态氢化物的热稳定性: X>Y |
| C.图中物质的转化过程均为氧化还原反应 |
| D.a 一定由W、X两种元素组成 |
您最近一年使用:0次
解题方法
4 . X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。
请回答下列问题:
(1)元素W在周期表中的位置是________ ,XR2的电子式为____ 。
(2)单质X和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为___________ 。Y、W的氢化物沸点高的是_______ (写化学式),原因是___________________ 。
(3)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为___________ 。
请回答下列问题:
(1)元素W在周期表中的位置是
(2)单质X和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为
(3)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为
您最近一年使用:0次



